Лекция №31.
реклама

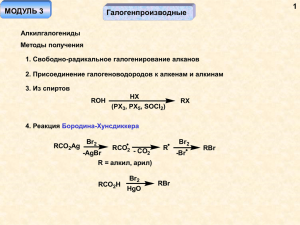
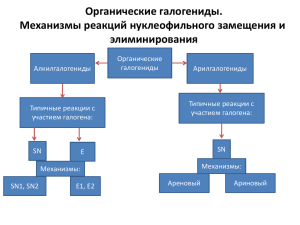
Теоретические основы органической химии Нуклеофильное замещение у насыщенного атома углерода Лекция 31 (электронно-лекционный курс) Проф. Бородкин Г.И. Нуклеофильное замещение у насыщенного атома углерода Yp + R-Xq R-Yp+1 + Xq-1 Y = H-Hal, Hal-, H-OH, OH-, ROH, RO-, CN-, RCOO-, R3N, R3P, RS-H, RS- и др. X = Hal, OH, OH2+, OR, OR2+, OCOR, OSO2R, NR3+, SR2+, N=N+ и др. Реакции, в которых нуклеофил одновременно является растворителем – реакции сольволиза Мономолекулярное нуклеофильное замещение R3C-X R3C+ + Y- k1 k-1 k2 R3C+ + X- R3CY определяет скорость определяет продукт Метод стационарных концентраций d[RX] k1k2 [RX][Y] = W = dt k-1 [X] + k2 [Y] Уменьшение константы скорости в присутствии Х- (эффект общего иона) Схема Уинстейна s s s s s R+ X- s R-X R...X s R+ s X-s s s s s тесная ИП разделенная ИП s s s s s R+ s + s X- s s s s s свободные ионы Обычно ионные пары реагируют с Х(внутренний возврат), а свободный ион и разделенная ионная пара дают продукт Доказательство существования ИП O18 O18 R-O-S-Ar R+... -O-S-Ar O O O R+ ... -O18 -S-Ar O RO18 -S-Ar O O Meтка 18О на ~20% перераспределена в непрореагировавшем реагенте Winstein et al. JACS 1968, 1904 Механизм SN1 2. Проявление свойств карбокатиона (продукты замещения, отщепления, перегруппировки) а)скорость реакции увеличивается по мере роста стабильности образующегося карбокатиона lgk25o + const +10 Ph3C+ +6 Ph2CH+ + +2 -2 PhMeCH+ Me3C+ + + -6 + Me2CH 15 20 25 30 35 40 45 50 б) потеря оптической активности на стадии ИП в) lg (kX/kH) = rs+, r (-3 -5) г) H= велико, S= близко к нулю f, êêàë/ì î ëü (â HSO3F-SbF5) Кинетичекие изотопные эффекты в сольволизе SN1 Вторичные kH/kD = 1.1 1.2 H (D) H (D) C+....X- R R R C+ R Первичные (С14, Сl37) малы Уравнение Грюнвальда-Уинстейна lg(kA/k0)= mY ko – константа скорости сольволиза t-BuCl Y – ионизирующая сила растворителя (m = 1, 80%EtOH) Y Вода MeOH EtOH MeCOOH HCOOH CF3COOH 3.49 -1.09 -2.03 -1.68 2.05 4.5 e 78.5 32.6 24.3 6.19 57.9 39 Расширенное уравнение Грюнвальда-Уинстейна lg(kA/k0)= mY + lN N – мера нуклеофильности растворителя l – чувствительность субстрата к нуклеофильности растворителя (l = 1 для сольволиза MeBr , l = 0 для t-BuCl) Критерии SN2 R C Y + R R R R sp3 X Y R C R X sp2 Y C R + X R 1. W = k [Y] [RX] нуклеофил участвует на lim стадии 2. Обращение конфигурации 3. H= обычно ниже, чем для SN1, S= отрицательна (-15 -40 э.е) 4. Акцепторы R несколько ускоряют реакцию (r невелико, 0.5 1.0 ) Кинетические изотопные эффекты в SN2 H (D) C-X R R КИЭ (вторичный) мал, часто kH/kD < 1 Первичные КИЭ С13, С14 1.1 1.15 Стереохимическое течение реакции SN2 R C Y + R R R X R Y R C X R Y C R + X R переходное состояние При Y = X 2kобмена = kрацемизации (1) Соотношение (1) можно использовать как доказательство механизма SN2 Стереохимия реакции SN2 Атака с тыла R X Y R R qY qC E = RYCe (aCaybCY)2 Y + 2 EY - ECX Атака с фронта невыгодна Y R X E = - qYqC + qYqX (aCaybCY+ aXaybXY)2 RYCe RYXe + 2 E -E Y R R s* CX Стереохимия реакции SN1 R + C R Полная рацемизация только в случае симметричного катиона R YR R C+......XR Y- В ионной паре уходящая частица Хэкранирует и катион не плоский, поэтому иногда - преимущественное обращение Оптически активный октанол-2 H2O MeOH Полное обращение конфигурации * OSO2Me MeCOMe/H2O Продукты с диоксан/H2O меньшей оптич. чистотой s H s s X- s + O s H + O s s s O Вода сольватирует и атакует с тыла, реакция с инверсией конфигурации s Диоксан сольватирует H2O с тыла, а вода атакует с фронта, продукт с s s сохранением конфигурации X- s (оптическая чистота меньше) s s Участие соседних групп Анхимерное содействие – увеличение скорости сольволиза благодаря взаимодействию соседней группы с возникающим карбокатионным центром От греческого «анхи» - близкий, «мерос» - часть + R R + Y Y - R R H H H OTS R Cl Br I NYCOPh OTS Kтранс/ kцис ~1 383 2. 106 9100 H