10 класс.химия. Вводная контрольная работа.
реклама

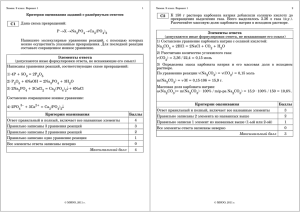
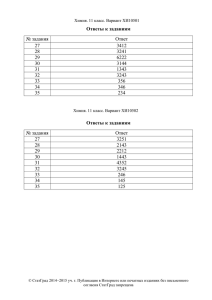
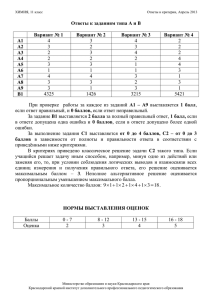
10 класс. Химия. Вводная контрольная работа. ЧАСТЬ 1 А 1. Химическому элементу, расположенному в 3-м периоде, IVА группе, соответствует схема электронного строения атома 1) 2, 8, 3 2) 2, 8, 4 3) 2, 8, 5 4) 2, 8, 8, 3 А 2. Вещество с ковалентной неполярной связью 1) Кислород 2) Хлороводород 3) Вода 4) Сульфат меди(II) А 3. Ряд элементов, расположенных в порядке увеличения высших степеней окисления в оксидах 1) N P As 2) P S Cl 3) N C B 4) Si Al Mg А 4. Кислотой называется вещество, в состав которого входят атомы 1) Металла и кислотного остатка 2) Неметалла и кислорода 3) Водорода и кислотного остатка 4) Металла и кислорода А 5. При полной диссоциации 1 моль фосфата калия в растворе образуется 1) 3 моль катионов калия и 4 моль фосфат-ионов 2) 2 моль катионов калия и 3 моль фосфат-ионов 3) 1 моль катионов калия и 3 моль фосфат-ионов 4) 3 моль катионов калия и 1 моль фосфат-ионов А 6. Реакция ионного обмена не протекает до конца между растворами 1) Сульфата калия и азотной кислоты 2) Карбоната натрия и соляной кислоты 3) Серной кислоты и гидроксида натрия 4) Сульфата натрия и нитрата свинца А 7. Наиболее активно реагирует с водой 1) Натрий 2) Цинк 3) Калий 4) Магний А 8. При взаимодействии оксида азота(V) с раствором гидроксида бария образуются А) азотная кислота Б) водород В) нитрат бария Г) оксид бария Д) вода 1) А, Г 2) Б, В 3) В, Д 4) А, В А 9. Хлорид цинка реагирует с каждым из двух веществ 1) Нитратом бария и гидроксидом калия 2) Фосфатом натрия и кислородом 3) Медью и фосфатом натрия 4) Нитратом серебра и гидроксидом натрия А 10. Для обнаружения хлорид-ионов в растворе можно использовать 1) Ca(OH)2 2) Cao 3) AgNO3 4) Ag2O ЧАСТЬ 2. В 1. В ряду элементов Si – P-- S -- Cl 1) Уменьшается атомный радиус 2) Увеличивается высшая степнь окисления 3) Увеличивается способность отдавать электроны 4) Увеличивается число электронных слоев 5) Увеличивается электроотрицательность Ответ:__________________________________ В 2. При комнатной температуре протекают реакции, уравнения которых: 1) 3Fe + 4H2O = Fe3O4 + 4H2 2) 2Na + 2H2O = 2NaOH + H2 3) Mg + 2H2O = Mg(OH)2 + H2 4) Ca + 2H2O = Ca(OH)2 + H2 5) Zn + H2O = ZnO + H2 Ответ:_________________________________ Ответ:__________________________________ В 3. Раствор сульфата алюминия реагирует с 1) Гидроксидом натрия 2) Нитратом меди(II) 3) Соляной кислотой 4) Медью 5) Хлоридом бария Ответ:_______________________________ ЧАСТЬ 3. С 1. Напишите уравнения реакций, с помощью которых можно осуществить превращения: t Cu(OH)2 A +H2 B +O2 A > > С 2. Какие массы хлорида кальция и воды необходимы для приготовления 30г 6%-ного раствора? С 3. Напишите уравнения реакций, с помощью которых можно осуществить превращения : Fe(OH)3 t X1 +H2 X2 FeCl2 > Ответы и критерий оценок: Часть 1. За каждый правильный отвкт 1 балл. Всего 10 баллов. Часть 2, за каждый правильный ответ 2 балла. Всего 8 баллов. Задание А 3 А1 2 А2 1 А3 2 А4 3 А5 4 А6 1 А7 3 А8 3 А9 4 А 10 3 В1 125 В2 24 В3 15 С1 Содержание верного ответа и указания по оцениванию Элементы ответа: Cu(OH)2 = CuO + H2O CuO + H2 = Cu + H2O 2Cu + O2 = 2CuO Правильно записаны 3 уравнения реакций Правильно записаны 2 уравнения реакций Правильно записано 1 уравнение реакции Все элементы ответа записаны неверно Максимальный балл С2 Содержание верного ответа и указания по оцениванию Элементы ответа: 1) рассчитана масса соли, необходимая для приготовления раствора 30 * 0,06 = 1,8 (г); 2) рассчитана масса воды: 30 – 1,8 = 28,2 (г); Ответ правильный и полный, включает все названные выше элементы В ответе допущена ошибка в одном из названных выше элементов Все элементы ответа записаны верно Максимальный балл С3 Содержание верного ответа и указания по Баллы 3 2 1 0 3 Баллы 2 1 0 2 Баллы оцениванию Элементы ответа: 2Fe(OH)3 = Fe2O3 = 3H2O Fe2O3 + 3H2 = 2Fe + 3H2O Fe + 2HCl = FeCl2 + H2 Правильно записаны 3 уравнения реакций Правильно записаны 2 уравнения реакций Правильно записаны 1 уравнение реакций Все элементы ответа записаны неверно Максимальный балл 3 2 1 0 3 Итого максимально 27 баллов. Менее 12 баллов «2», 13 – 17 «3», 1822 «4», 23 и более «5».