Лекция №14.
Реклама

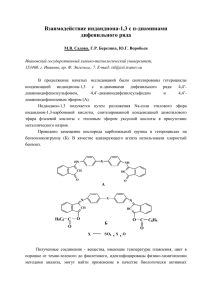
Теоретические основы органической химии Принцип ЖМКО Лекция 14 (электронно-лекционный курс) Проф. Бородкин Г.И. Кислотные и основные свойства органических соединений Бренстед: Кислота – соединение, способное отдавать протон, основание – принимать протон Льюис: Кислота – соединение, способное принимать пару электронов, основание – отдавать пару электронов Концепция Пирсона Химические соединения Кислоты Льюиса жесткое мягкое Основания Льюиса жесткое мягкое Ralph Pearson -1919, Chicago -1946, Ph.D, Northwestern University -1946-1976, University of California at Santa Barbara -1963г., концепция ЖМКО -1974, National Academy of Science -1983 г., абсолютная жесткость (R. Parr) Peter C. Ford, Coordination Chemistry Reviews v.187, p.2-15 (1999) "Interview with Ralph G. Pearson" Концепция Пирсона Жесткие кислоты более легко и с образованием более прочных связей реагируют с жесткими основаниями, а мягкие кислоты с мягкими основаниями M M Ж Ж Жесткие кислоты -низкая поляризуемость -малый объем -высокое сродство к (e) -высокая НВМО -большой (+) заряд Жесткие основания -низкая поляризуемость -малый объем -высокий потенциал Ip -низкая ВЗМО -малый (-) заряд Мягкие кислоты -высокая поляризуемость -большой объем -низкая НВМО -малое сродство к (е) -малый (+) заряд Мягкие основания -высокая поляризуемость -большой объем -высокая ВЗМО -малый IP -большой (-)заряд Поляризуемость мягких кислот и оснований: в большом атоме (или ионе с малым эффективным зарядом ядра) относительно легко «искажается» электронное облако (частица поляризуется) Жесткие кислоты Мягкие кислоты Пограничные кислоты Жесткие основания Мягкие основания Пограничные основания Жесткость = h = 1/2(Ip - EA) Мягкость = S = 1/h ~ 2(Ip – EA) Жесткость атомов или групп Атом Li C N O F Na Si P S h Катион h 6.4 + 2.4 Li+ 35.1 5.0 Mg+ 32.5 7.3 Na+ 21.1 6.1 Ca++ 19.7 7.0 Al3+ 45.8 2.3 Cu+ 6.3 3.4 Cu2+ 8.3 4.9 Fe2+ 7.3 4.1 Fe3+ 13.1 Анион h 6.8 F7.0 Cl4.7 Br4.2 I3.7 Me4.0 NH2- 5.3 OH- 5.6 SH- 4.1 CN5.3 Абсолютная жесткость: G = -[EВЗМО – EНСМО] E E электрона в вакууме GA A A GB B B Абсолютная электроотрицательность: [EВЗМО + ЕНСМО] = 2 Степень переноса заряда: Движущая сила A переноса заряда DN = B Сопротивление GA - GB переносу заряда через валентные оболочки Зарядовый контроль Орбитальный контроль ВВМО НВМО Ж кислота НЗМО Ж основание qDqA DE = rDe ВЗМО М кислота М основание 2SS(cBcAb)2 DE = EA - EB Подход Клопмана Кислоты En* = -(3Ip + EA)/4 + 14.39(q-0.5х)х Rион + 0.82 Основания Em* = -(Ip + 3EA)/4 + 14.39(q+0.5) Rион (1 - 1/e) (1 - 1/e) Ip - потенциал ионозации EA – сродство к электрону q – первоначальный заряд иона e- диэлектрическая проницаемость х – параметр, учитывающий изменение величины иона при окислении x = q-(q-1) 0.75 Орбитальные электроотрицательности кислот в воде (эв) Ip EA Eорбит. r+0.82 Eдесольв. En* Al3+ Ti4+ Mg2+ Fe3+ H+ Cu+ Ag+ Hg2+ 28.4 43.2 15.0 30.6 13.6 7.7 7.6 18.8 18.8 26.0 28.1 39.5 7.6 13.2 16 27.0 0.8 10.4 2.0 14.9 2.2 6.2 10.4 16.7 1.33 1.50 1.48 1.46 1.8 2.08 1.92 32.0 43.8 15.6 29.2 10.8 12.9 3.4 12.0 6.0 4.4 2.4 2.2 0.4 -2.4 -2.8 -4.6 Орбитальные электроотрицательности оснований в воде (эв) Ip FH2O OHClBrCNIH- 17.4 25.4 13.1 13.0 11.8 14.6 10.4 13.6 EA Eорбит. 3.5 7.0 12.6 15.8 2.8 5.4 3.7 6.0 3.5 5.6 3.2 6.0 3.2 5.0 0.7 4.0 R 1.36 (1.4) 1.40 1.81 1.95 2.60 2.2 2.1 Eдесольв. 5.2 (-5.1) 5.1 3.9 3.6 2.7 3.3 3.4 Em* -12.2 (-10.7) -10.4 -9.9 -9.2 -8.8 -8.3 -7.4 Уравнение Эдварса (1954 г.) lgK/Ko = aP + bH K – константа равновесия реакции основания B с кислотой А Ko – константа равновесия H2O c кислотой А P – поляризуемость H – относительная протонная основность основания В a,b - const Подход Яцимирского (химическая шкала) MeHg+ + BH MeHgB + H+ pKMeHg+ S2- Mягкие 20 HS- 16 R3P 12 N 3- 8 RSCN- Жесткие NH3 OH- C5H5N MeCO2- 4 F-4 4 H 2O 8 12 16 pKH+ ТЭХ, 1971, 452 1. В газовой фазе: Me-OH + H-I М-Ж Ж-М Kp = [H2O] [MeI] [HI] [MeOH] MeI + H-OH М-М Ж-Ж Kp > 109 2. Симбиоз [Co(NH3)5F]2+ более стабилен, чем [Co(NH3)5I]2+ [Co(CN)5I]2+ более стабилен, чем [Co(CN)5F]2+ 3. Алкилирование енолят-ионов Me - OEt Me Me o 20 O C H O + MeX MeC-CH-COEt + ГМФТА MeO O O С-изомер жесткий мягкий Х=I 97% X = OTs 3% OEt O H О-изомер 3% 97%