ХИМИЧЕСКИЙ СОСТАВ ЖИВОГО
реклама
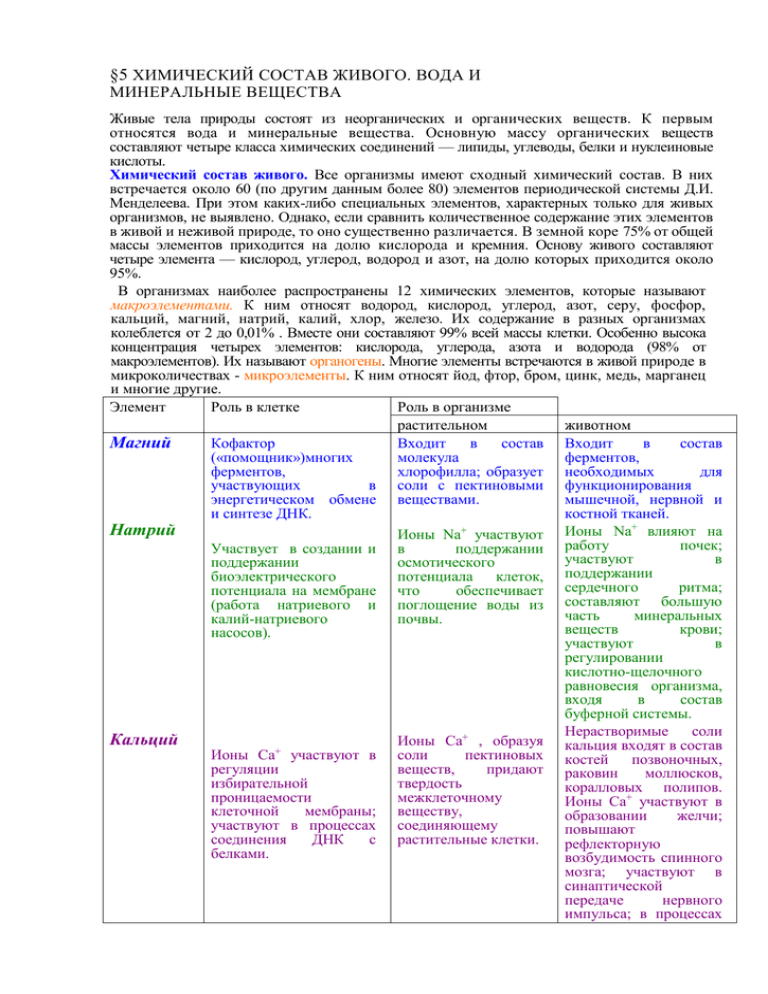
§5 ХИМИЧЕСКИЙ СОСТАВ ЖИВОГО. ВОДА И МИНЕРАЛЬНЫЕ ВЕЩЕСТВА Живые тела природы состоят из неорганических и органических веществ. К первым относятся вода и минеральные вещества. Основную массу органических веществ составляют четыре класса химических соединений — липиды, углеводы, белки и нуклеиновые кислоты. Химический состав живого. Все организмы имеют сходный химический состав. В них встречается около 60 (по другим данным более 80) элементов периодической системы Д.И. Менделеева. При этом каких-либо специальных элементов, характерных только для живых организмов, не выявлено. Однако, если сравнить количественное содержание этих элементов в живой и неживой природе, то оно существенно различается. В земной коре 75% от общей массы элементов приходится на долю кислорода и кремния. Основу живого составляют четыре элемента — кислород, углерод, водород и азот, на долю которых приходится около 95%. В организмах наиболее распространены 12 химических элементов, которые называют макроэлементами. К ним относят водород, кислород, углерод, азот, серу, фосфор, кальций, магний, натрий, калий, хлор, железо. Их содержание в разных организмах колеблется от 2 до 0,01% . Вместе они составляют 99% всей массы клетки. Особенно высока концентрация четырех элементов: кислорода, углерода, азота и водорода (98% от макроэлементов). Их называют органогены. Многие элементы встречаются в живой природе в микроколичествах - микроэлементы. К ним относят йод, фтор, бром, цинк, медь, марганец и многие другие. Элемент Роль в клетке Роль в организме растительном животном Магний Кофактор Входит в состав Входит в состав («помощник»)многих молекула ферментов, ферментов, хлорофилла; образует необходимых для участвующих в соли с пектиновыми функционирования энергетическом обмене веществами. мышечной, нервной и и синтезе ДНК. костной тканей. + Натрий Ионы Na+ участвуют Ионы Na влияют на почек; Участвует в создании и в поддержании работу участвуют в поддержании осмотического поддержании биоэлектрического потенциала клеток, ритма; потенциала на мембране что обеспечивает сердечного составляют большую (работа натриевого и поглощение воды из часть минеральных калий-натриевого почвы. веществ крови; насосов). участвуют в регулировании кислотно-щелочного равновесия организма, входя в состав буферной системы. Нерастворимые соли Кальций Ионы Ca+ , образуя кальция входят в состав Ионы Ca+ участвуют в соли пектиновых костей позвоночных, регуляции веществ, придают раковин моллюсков, избирательной твердость коралловых полипов. проницаемости межклеточному Ионы Ca+ участвуют в клеточной мембраны; веществу, образовании желчи; участвуют в процессах соединяющему повышают соединения ДНК с растительные клетки. рефлекторную белками. возбудимость спинного мозга; участвуют в синаптической передаче нервного импульса; в процессах Железо Входит в состав цитохромов-ферментов переносчиков электронов в процессах дыхания и фотосинтеза. Калий Сера Фосфор Хлор Участвует в поддержании коллоидных свойств цитоплазмы, биоэлектрического потенциала на мембране (работа натрийкалиевого насоса); активирует ферменты, участвующие в синтезе белка; входит в состав ферментов, участвующих в гликолизе. Входит в состав аминокислот, участвует в формировании третичной структуры белка, входит в состав некоторых ферментов; участвует в бактериальном фотосинтезе. Соединения серы – источник энергии при хемосинтезе. В виде остатков фосфорной кислоты входит в состав АТФ, нуклеотидов, ДНК, РНК, фосфолипидов, многих ферментов, в состав всех мембранных структур. Анионы хлора поддерживают электронейтральность клетки. Участвует в биосинтезе хлорофилла; входит в состав ферментов, участвующих в дыхании; в состав цитохромов – переносчиков электронов в ходе фотосинтеза. Участвует в регуляции водного режима; входит в состав ферментов, участвующих в фотосинтезе. Компонент клеточного сока в вакуолях. свертывания крови; активируют ферменты при сокращении поперечнополосатых мышечных волокон. Входит в состав гемма белка гемоглобина и миоглобина(белка, содержащего кислород в мышцах) Находится в железосодержащем белке феррине в печени и селезенке). Участвует в поддержании сердечного ритма, в проведении нервного импульса. Входит в состав инсулина, витамина В1, биотина. В виде фосфатов в состав костной ткани, зубной эмали. У млекопитающих в состав буферных систем. Анионы хлора участвуют в регуляции тургорного давления. Анионы хлора участвуют в формировании осмотического потенциала плазмы крови, в процессах возбуждения и торможения в нервных клетках, входят в Цинк Входит в состав ферментов, участвующих в спиртовом брожении. Входит в состав ферментов, участвующих в расщеплении угольной кислоты и в синтезе растительных гормонов – ауксинов. состав Входит в состав ферментов темновой фазы фотосинтеза. Входит в дыхательных ферментов. состав Входит в состав ферментов темновой фазы фотосинтеза. Входит в ферментов участвующих фиксации азота. состав , в Медь Входит в окислительных ферментов. Йод Фтор Марганец Бор Молибден Бром Кобальт Входит в состав витамина В1, который участвует в расщеплении пировиноградной кислоты у животных, растений, микроорганизмов. состав соляной кислоты в желудочном соке. Входит в состав фермента, участвующего в транспорте углекислого газа в крови позвоночных; фермента разрушающего пептидные связи при переваривании белков; ферментов, необходимых для нормального роста. Участвует в кроветворении,синтезе гемоглобина; у беспозвоночных входит в состав белков – переносчиков кислорода – гемоцианов. У человека входит в состав фермента, участвующего в синтезе меланина. У позвоночных входит в состав гормрна щитовидной железы – тироксина. Входит в состав костей, эмали зубов. Входит в состав ферментов, необходимых для роста костей. Влияет на ростовые процессы. Входит в состав ферментов, регулирующих работу устьичного аппарата, ферментов участвующих в синтезе аминокислот. Входит в состав витамина В12, принимает участие в синтезе гемоглобина. Вода. Самым распространенным веществом в живых телах природы является вода. Ее содержание колеблется от 60 до 98% от общей массы, что зависит от типа клеток, тканей и организмов. Биологическое значение воды связано с уникальными свойствами: полярностью и способностью ее молекул образовывать водородные связи, большим поверхностным натяжением и высокими температурами плавления и кипения. Наличием водородных связей объясняется и тот факт, что при обычных условиях вода — жидкость. Благодаря водородным связям при замерзании около 0°С расстояние между молекулами воды слегка увеличивается. В результате плотность льда уменьшается, и он оказывается легче, чем жидкая вода. Превращаясь в лед в живых клетках и увеличиваясь в объеме, вода может разорвать их стенки и разрушить клетки. С водородными связями связано и высокое поверхностное натяжение воды. Вода способна слипаться и с другими веществами, чем объясняются ее капиллярные свойства. Вода обладает высокой теплопроводностью. Благодаря этому свойству тепло быстро и равномерно распределяется по всему объему воды, находящейся в живых клетках, предотвращая перегрев в отдельных местах. При испарении воды происходит существенное охлаждение поверхности, с которой она испаряется. Участие в терморегуляции живых организмов — еще одна биологическая функция воды. Вода — универсальный растворитель. Растворимые в воде вещества называют гидрофильными (от греч. гидор — вода, филео— люблю). Неполярные вещества, например бензин, жиры, масла, в воде нерастворимы. Такие вещества называют гидрофобными (от греч. гидор — вода, фобос — страх, боязнь). Вода служит катализатором (ускорителем) многих реакций и средой, где протекают все химические реакции живого. Водные растворы веществ образуют внутреннюю среду клетки. С водой связан и тургор (от лат. тургере — быть набухшим, наполненным) клетки, т. е. напряженное состояние клеточной мембраны, создаваемое давлением внутриклеточной жидкости, которая на 70— 90% состоит из воды. Все свойства и биологические функции воды имеют важное значение для жизни на Земле. Физические свойства воды и их значение для биологических процессов. физическое свойство значение Сочетание высокой 1. Идеальная жидкость теплоемкости (благодаря для поддержания наличию водородных теплового связей) и высокой равновесия теплопроводности (из-за организма – небольших размеров самих большое количество молекул. воды в клетках придает организму термостабильность и дает возможность значительно охладиться при минимальной потере воды. 2. Круговорот воды в природе – один из элементов формирования погоды и климата. примеры Транспирация у растений, потоотделение у млекопитающих. Периодичность выпадения осадков. Исторически сложившиеся условия увлажнения в различных природных зонах. Прозрачность в видимом Возможность фотосинтеза Высокопродуктивные участке спектра. на небольшой глубине, а биогеоценозы водоемов. значит и возможность связанных с ним пищевых цепей. Практически полная Поддержание формы Тургорное давление несжимаемость (благодаря организмов. придает форму сочным силам межмолекулярного органам и тканям растений, сцепления) Подвижность молекул ( Возможность осмоса. вследствие слабости водородных связей). Вязкость (благодаря Смазывающие свойства. наличию водородных связей). Хороший (благодаря молекул) растворитель Самый распространенный полярности в природе растворитель. Среда протекания многих химических реакций. Способность образовывать Является дисперсионной гидратационную оболочку средой в коллоидной вокруг молекул (благодаря системе цитоплазмы. полярности молекул). Оптимальное для биологических систем значение силы поверхностного натяжения (определяемого силами межмолекулярного сцепления). Расширение при замерзании (благодаря образованию молекулой максимального числа-4водородных связей). Водные растворы являются средством передвижении веществ в организме. обеспечивая положение в пространстве. Гидростатический скелет у круглых червей, медуз. Амниотическая жидкость поддерживает и защищает плод млекопитающих. Поступление воды из почвы. Плазмолиз. Внутрисуставная жидкость облегчает скольжение суставов, плевральная жидкость уменьшает трение между легкими и грудной клеткой. Кровь, тканевая жидкость, клеточный сок растений и другие жидкости организмов растворы белков, сахаров, органических веществ. Водные организмы используют для дыхания растворенный в воде кислород. Гиалоплазма представляет собой коллоидный раствор белков, в котором молекулы белков окружены чехлом из определенным образом ориентированных молекул воды. Капиллярный кровоток. Восходящий и нисходящий токи растворов в растениях. Лед легче воды, выполняет Сохранение зимой функцию теплоизолятора и биоценозов замерзающих защищает от холода водоемов. находящиеся в воде организмы. Роль воды в обмене веществ. функция Участие в гидролиза. примеры 1. белки + вода = аминокислоты крахмал + вода = глюкоза жир + вода = глицерин и жирные кислоты. 2. Высвобождение энергии АТФ АТФ + H2O = АДФ + H3PO4 + Е (40 кДж) Донор электронов в световую фазу фотосинтеза Источник атомарного в темновую фазу фотосинтеза водорода Источник протонов для синтез АТФ при дыхании и синтез АТФ работы протонных насосов фотосинтезе. реакциях при Минеральные вещества. Эти вещества в клетках присутствуют в виде ионов или твердых нерастворимых солей. Они создают кислую либо щелочную реакцию среды в клетках, входят в состав некоторых структур влияют на протекание в живом различных процессов. Так, ионы кальция (Са+2) в растениях входят в состав оболочек клеток, у животных — в состав костей и зубов , влияют на свертывание крови. Ионы калия (К+) и натрия (Na+) содействуют проведению нервных импульсов, активизируют деятельность ферментов, влияют на рост растений. Ионы хлора (С1-) входят в состав желудочного сока. Ионы магния (Mg+2) содержатся в молекулах хлорофилла. Йод является компонентом гормона щитовидной железы — тироксина. Он влияет на обмен веществ в организме. Ионы железа (Fe +2) входят в состав гемоглобина и участвуют в переносе кислорода. Медь, марганец, бор участвуют в процессах кроветворения, фотосинтеза, повышают урожайность и влияют на ростовые процессы растений. Фтор входит в состав эмали зубов, при его недостатке развивается кариес, а при избытке — флюороз — размягчение костной ткани. Ионы молибдена, хрома, кобальта, цинка активизируют работу ферментов, влияют на обмен веществ. При нехватке этих элементов могут нарушаться процессы жизнедеятельности организмов.