Причины развития, диагностика, профилактика и лечение
реклама

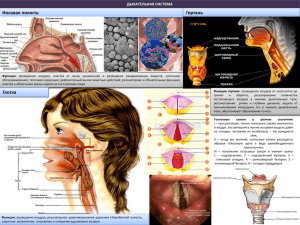
1 С.И.Леонович докт. мед. наук, профессор 1-й кафедры хирургических болезней БГМУ А.А.Татур докт. .мед. наук, доцент 1-й кафедры хирургических болезней БГМУ Причины развития, диагностика, профилактика и лечение рубцовых стенозов трахеи Трахея – это орган, по которому воздух при дыхании проходит в легкие и обратно. Частичное или полное нарушение ее проходимости приводит к дыхательной недостаточности вплоть до асфиксии или удушья. Подобное состояние может быть вызвано аспирацией крупного инородного тела, массивным легочным кровотечением, тяжелыми травматическими повреждениями, доброкачественными и злокачественными опухолями, сдавлением трахеи зобно-измененной щитовидной железой, кистами и опухолями средостения, аневризмой аорты. В настоящее время наиболее частой причиной сужения просвета трахеи является разрастание рубцовой ткани, которая замещает ее нормальные структуры. Рубцовый стеноз трахеи (РСТ) без проведения лечебных мероприятий характеризуется прогрессирующим течением. Воспалительная инфильтрация и отек тканей, а также просто закупорка суженного участка трахеи густой мокротой может привести к внезапной гибели пациента. К сожалению, многим больным с рубцовыми стенозами трахеи в связи с поздней диагностикой и угрозой асфиксии по жизненным показаниям была наложена трахеостома, т.е. оперативным путем в просвет трахеи ниже уровня сужения установлена специальная трубка-канюля, через которую пациент дышит. В последующем такие пациенты вынуждены обращаться в различные учреждения здравоохранения и нередко в связи с обширным поражением трахеи остаются инвалидами – хроническими канюленосителями. В последнее десятилетие во всем мире число пациентов с данной патологией заметно увеличилось, что объясняется развитием цивилизации и, как это ни странно, успехами медицины. В настоящее время все шире внедряются в практику сложные длительные реконструктивные хирургические вмешательства на магистральных сосудах, головном мозге, сердце, при онкологической патологии, которые требуют в послеоперационном периоде проведения продленной искусственной вентиляции легких (ИВЛ). К сожалению, рост в Республике количества автотравм и других техногенных аварий пока не имеет тенденции к снижению. Причем отмечается абсолютное увеличение числа сочетанных травм, среди которых превалируют по тяжести повреждения головного 2 мозга и органов груди, требующие в комплексе лечебных мероприятий проведения ИВЛ. Сегодня успехи в различных областях хирургии, в анестезиологии и реаниматологии позволяют оперировать и, самое главное, выхаживать после операции пациентов с очень тяжелыми травмами и заболеваниям. Но, как бы это не было прискорбно, на практике развитие рубцового стеноза трахеи нередко является «своеобразной платой» за спасенную жизнь пациента. Анатомия трахеи Трахея («дыхательное горло»)- начинается от нижней границы гортани, имеет форму трубки длиной 9-15см и шириной - 1,5-2,5 см, делится на два главных бронха, через которые воздух и поступает в легкие. Выделяют шейный и грудной отделы трахеи. По своему ходу трахея граничит со щитовидной железой, пищеводом, крупными сосудами и нервами шеи и средостения. Основу трахеи составляют 16 - 20 хрящевых полуколец, разомкнутых с задней стороны. Они обеспечивают каркасность трахеи при дыхании. В подслизистой основе и слизистой оболочке находятся трахеальные железы, вырабатывающие слизь. Слизистая оболочка бронхов и трахеи выстлана особыми реснитчатыми эпителиальными клетками. На их поверхности располагаются специальные выросты - реснички, которые совершают непрерывные колебательные движения и вместе со слизью, находящейся на ее поверхности, выводят пыль, химические вещества, микробы и вирусы вверх в гортань и глотку. Из глотки слизь выплевывается или незаметно проглатывается человеком. Средний объем суточной вентиляции взрослого человека составляет около 15–20 тыс. литров воздуха. В трахее воздух также согревается, увлажняется и подходит к альвеолам легких, где происходит газообмен, практически стерильным. Процесс этот напоминает движение ленты эскалатора в метро снизу вверх с находящимися на ней людьми и обеспечивается так называемым мукоцилиарным механизмом очистки воздуха (от лат. mucus - слизь, cilia - ресничка). Важно подчеркнуть, что нормальная анатомия трахеи и расположенных рядом кровеносных сосудов, нервов и органов при рубцовых стенозах, как-правило, значительно меняется вследствие перенесенных травм и гнойно-воспалительных процессов шеи и средостения (флегмона шеи, гнойный медиастенит, эмпиема плевры), после предшествующих операций, включая и трахеостомию. Это подчеркивает сложность проведения любых, даже небольших хирургических вмешательств на рубцово-измененной трахее в неспециализированном стационаре, поскольку возможные осложнения могут быть достаточно тяжелы, а иногда и непоправимы. 3 Причины развития рубцовых сужений трахеи многообразны. У детей врожденные стенозы трахеи крайне редки и в литературе на сегодняшний день описано только около 50 случаев. У взрослых к рубцовому сужению приводят открытая (ранения) и закрытая (удары, сдавления) травмы шеи и груди с повреждением трахеи, а также термические и химические ее ожоги, лучевая терапия по поводу онкологических, заболеваний, неспецифические и специфические воспалительные процессы (склерома, сифилис, актиномикоз, дифтерия, туберкулез). Однако в современной клинической практике, как уже подчеркивалось нами выше, наиболее часто они развиваются вследствие длительной интубации трахеи с целью искусственной вентиляции легких и как результат дефектов формирования и послеоперационного ведения называть, соответственно, трахеостомы. Такие стенозы принято постинтубационными и посттрахеостомическими. Изредка наблюдаются идиопатические стенозы, когда невозможно установить какую-либо значимую причину его развития. Частота возникновения РСТ после длительной интубации и трахеостомии по разным статистикам варьирует широко – от долей процента до 25%. Патогенез развития РСТ сегодня изучен достаточно хорошо, чтобы понимать особенности его клинического течения, задачи диагностики, лечения и, самое важное, профилактики. Большое значение в развития рубцового процесса имеют общие факторы, такие, как гипоксия, инфекция, снижение реактивности организма, индивидуальные особенности процессов регенерации. Эти факторы напрямую связаны со степенью тяжести основного заболевания или травмы, которые потребовали включения в лечебную программу искусственной вентиляции легких. Для осуществления ИВЛ в условиях отделения реанимации проводится «интубация трахеи», т.е. проведение в просвет трахеи через рот или нос специальной трубки, через которую от дыхательного аппарата кислород поступает в легкие. Чтобы создать закрытый контур «аппарат-легкие» и предотвратить сброс газа наружу, в просвете трахее раздувается специальная манжетка. Для улучшения санации трахебронхиального дерева при длительной ИВЛ пациентам нередко накладывается трахеостома. Трахеостомические трубки для проведения ИВЛ также имеют раздувную манжету. Оптимальные сроки для проведения трахеостомии в таких случаях - 3-5-е сутки ИВЛ. Среди местных факторов основное значение имеют давление раздутой манжетки интубационной трубки или канюли на стенку трахеи, методика, техника и сроки наложения трахеостомы, особенности интубационной трубки и трахеостомической канюли. Длительная компрессия раздувной манжеткой приводит к локальной ишемии стенки трахеи с 4 развитием некроза слизистой оболочки и хрящевых полуколец. С присоединением инфекции развивается гнойно-некротический трахеит, который завершается разрушением хряща (хондромаляция, хондролизис), развитием грануляционной ткани и рубцового процесса. Считается, что трахеостомию при механической асфиксии должен уметь выполнить врач любой специальности. Эта благородная задача как бы еще подчеркивает и достаточную простоту выполнения этой операции. Тем не менее, по данным отечественных и зарубежных авторов частота осложнений во время проведения трахеостомии встречается не реже, чем в 20% случаев. Особенно сложна техника повторной трахеостомии или ее выполнение после предшествующих операций на органах шеи. Трахеостомические канюли в идеале должны индивидуально подбираться пациентам до операции. С учетом особенностей формы их трахеи (коническая, веретенообразная, воронкообразная, цилиндрическая) необходимо подбирать соответствующие диаметр, длину и кривизну трубки. На практике, к сожалению, обычно учитывается только первый параметр и используются металлические или жесткие пластмассовые канюли. Своевременно не диагностированные травматические разрывы трахеи, недостаточно квалифицированное ушивание ран трахеи также могут привести к стенозу. Типичными местами развития стенозирования является шейный отдел трахеи в зоне стояния трахеостомической канюли, шейный и верхне-грудной отделы – в месте надувной манжеты интубационной трубки или конца плотной (металлической или пластмассовой) трахеостомической трубки. При стенозах в области трахеостомы рубцовая ткань в области разрушенной стенки трахеи развивается на передней и частично на боковых стенках, при постинтубационных стенозах – обычно циркулярно на уровне стояния манжетки. Клиническая картина нарушения воздухопроводности трахеи и вентиляции легких развивается постепенно, выраженность симптомов нарастает медленно в течение недель или нескольких месяцев, характер же зависит от степени развития заболевания. Диагностировать нарушения проходимости трахеи на ранних стадиях заболевания сложно и больные сегодня поступают в специализированный стационар уже в тяжелом состоянии, когда для спасения их жизни требуются срочные лечебно-диагностические мероприятия. Вот почему все пациенты, перенесшие тяжелые многочасовые операции, продленную искусственную вентиляцию легких (травма, инфаркт миокарда или мозга и др.) или трахеостомию и их врачи должны знать о потенциальной возможности развития у них рубцового сужения трахеи. Как известно, нормальная трахея имеет ширину просвета минимум 1,5 см, а у мужчин – до 2-2,5 см., что создает достаточно большой резерв 5 компенсации вохдухопроводности. При рубцовом сужении просвета трахеи более 1 см признаки нарушения дыхания полностью отсутствуют и компенсированный стеноз, не имеющий специфических симптомов, клинически, как правило, еще не выявляется. При диаметре сужения просвета трахеи в пределах 6 - 10 мм клинические проявления ограничиваются умеренной одышкой при значительной физической нагрузке, на которую с учетом тяжести перенесенного недавно (обычно 1-2 месяца) заболевания или травмы, больные редко обращают внимание. Более выраженное сужение просвета трахеи до 5-4 мм уже сопровождается одышкой при умеренной и незначительной физической нагрузке, а при увеличении нагрузки может возникать стридор – характерное шумное высокотональное дыхание. Характерны жалобы одного нашего 23-летнего пациента, который перенес тяжелую глубокую флегмону шеи, сепсис и 2 недели находился на ИВЛ. Через 4 недели после удаления из трахеи интубационной трубки он был выписан на амбулаторное лечение и дома у него постепенно начала нарастать одышка, которая резко усиливалась и появлялся стридор, когда он брал на руки годовалого сына, т.е. при минимальной нагрузке. При поступлении в клинику трахея у него была сужена до 5 мм. При сужении просвета трахеи до 3 мм и менее, когда оно приобретает вид «песочных часов», одышка остается в спокойном состоянии и практически всегда сопровождается стридором. Стридор в покое – это всегда реальная угроза асфиксии. У 10-15% больных со стенозом трахеи, которым при угрозе асфиксии была наложена трахеостома, выше ее может развиваться полное заращение ее просвета. Кроме нарастающей одышки больных беспокоят охриплость голоса, кашель с выделением мокроты. При декомпенсированных стенозах присоединяются инфекционные бронхо-легочные осложнения (гнойный бронхит, пневмония). Как видно, симптоматика при стенозах трахеи неспецифическая, поскольку одышка и кашель обычно встречаются и при другой бронхолегочной патологии. Но появление затрудненного, а тем более стридорозного, дыхания при физической нагрузке у пациента, перенесшего травму шеи или груди, длительную ИВЛ или трахеостомию, всегда должно насторожить и самого больного и его лечащего врача в отношении возможности развития стеноза трахеи. Диагностика рубцовых стенозов трахеи основывается на тщательном изучении истории заболевания, оценке симптомов в динамике и своевременном применении специальных методов исследования. Фибротрахеобронхоскопия сегодня является основным доступным и информативным методом ранней диагностики стенозирующего поражения трахеи. Она позволяет выявить рубцовый процесс, определить его локализацию, протяженность, степень сужения просвета, выраженность воспалительного 6 процесса и решить вопросы лечебной тактики. При необходимости эндоскопически можно, чтобы избежать наложения трахеостомы, произвести расширение просвета трахеи в зоне стеноза при помощи электродиатермокоагуляции или, лучше, высокоэнергетического лазера. За один сеанс просвет трахеи увеличивается на 2-4 мм. Состояние больных компенсируется при создании просвета более 6 мм. К сожалению эффект этих процедур временный, но компенсация дыхания на 10-12 дней позволяет адекватно подготовить больного к операции. После реканализации зоны стеноза эндоскопически можно осмотреть трахею и доступные бронхи, выявить выраженность эндотрахеобронхита, оценить протяженность стеноза, взять мокроту для бактериологического исследования. Рентгенологическая диагностика включает выполнение трахеотомографии, контрастной контурной томографии и компьютерной томографии. Современная компьютерная спиральная томография дает наиболее полную информацию о состоянии просвета трахеи, ее стенки и паратрахеального пространства. Она безопасна при стридоре, что делает ее методом выбора у больных с декомпенсированным дыханием. В последние 10 лет начала разрабатываться Японии и сейчас широко применяется в США, и некоторых европейских странах компьютерная спиральная томография с трехмерной реконструкцией (Spiral computed tomography with 3-dimensional reconstruction), которая позволяет неинвазивно получить наиболее точные и полные данные о рубцовой трансформации трахеи и бронхов. Лечение Методы лечения РСТ подразделяются на радикальные и паллиативные, эндоскопические и хирургические. К сожалению, сегодня выбор метода лечения этой тяжелой патологии в Республике еще нередко определяется не научно-обоснованными медицинскими показаниями и противопоказаниями, впрочем, как и в России, а профилем учреждения или специалиста к которому обратился или был направлен пациент. Это торакальные хирурги, оториноларингологи, пульмонологи, эндоскописты. Исторически так сложилось, что ЛОР-врачи, занимаясь стенозами гортани различной этиологии, лечили также и стенозы трахеи, в первую очередь воспалительного (склерома, скарлатина, сифилис) генеза своими методами. Эти методы применительно к трахее отличаются до настоящего времени отсутствием должного радикализма, большой длительностью и нередко завершаются хроническим канюленосительством. Представляется, что сегодня подход к лечению РСТ должен быть строго индивидуальным, отвечающим интересам только больного и должен быть направлен на быстрейшее его выздоровление. 7 В настоящее время лечение трахеальных рубцовых стенозов во всем мире развивается в нескольких направлениях: 1. оптимизация предоперационной подготовки с включением высокотехнологических методик (лазерная реканализация, эндоскопическое бужирование и дилятация, эндостентирование) 2. совершенствование операций, хирургической техники радикальных одномоментных включая и вовлечение в рубцовый процесс перстневидного хряща гортани, надбифуркационный отдел трахеи. 3. предупреждение развития ранних послеоперационных, в первую очередь гнойновоспалительных, осложнений 4. профилактика рестенозирования в раннем и позднем послеоперационных периодах. Основным признанным в мире радикальным высокоэффективным методом лечения рубцовых стенозов трахеи является циркулярная резекция стенозированного ее участка с формированием межтрахеального или ларинготрахеального анастомоза. При этом одномоментно удаляется и суженный патологически измененный сегмент трахеи, и восстанавливается свободное дыхание. Обычная протяженность резецируемого участка трахеи составляет 4-5 колец (2,5-3 см), но технически возможно без развития натяжения сшиваемых концов трахеи удаление и 7-8 колец. Более обширные резекции при протяженных рубцовых стенозах трахеи технически возможны, но из-за высокого риска осложнений в ведущих торакальных клиниках мира признаны нецелесообразными. При опухолях при помощи специальных приемов мобилизации гортани и главных бронхов возможно выполнение резекции до 12-13 колец трахеи. Интубационная трубка после резекции трахеи извлекается после восстановления самостоятельного дыхания и проведения санационной бронхоскопии через 2-3 часа после операции. Больные выписываются на амбулаторное лечение на 15-20 сутки. Другим методом, который ни в коем случае не должен противопоставляться циркулярной резекции трахеи, является выполнение этапных реконструктивно- пластических операций, которые применяются в различных модификациях как ЛОРврачами, так и торакальными хирургами. Пациентам выполняется продольное рассечение трахеи с максимальным иссечением рубцовой ткани и этапное моделирование ее просвета на Т-образной трубке. Такая силиконовая трубка, усовершенствованная американцем В. Монтгомери 40 лет назад, позволяет восстановить естественное носовое дыхание, а закрытие ее горизонтального колена – получить звучную речь. Пациент легко 8 обучается самостоятельной ежедневной смене и очистке трубки, и после снятия швов выписывается из отделения. В период между этапами пластики больные социально компенсированы, свободно дышат и разговаривают. Хотя длительное (10-12 мес. и более) нахождение Т-образного стента в просвете трахеи в послеоперационном периоде является отрицательным моментом данной методики, но оно необходимо для оптимизации процесса рубцевания в зоне первичного стеноза. Эта операция выполняется при неэффективности эндоскопического лечения и при очень высоком риске выполнения циркулярной резекции, причем наиболее часто у больных с функционирующей трахеостомой. В некоторых случаях после удаления стента формируется достаточный (более 10мм) просвет трахеи, в других – необходимо выполнять дополнительную пластику передней стенки трахеи. Эндоскопические методы лечения РСТ, на которые в 90-е г.г. прошлого столетия возлагались большие надежды, на практике оказались не радикальными. Эндоскопическое расширение просвета трахеи различными методами с постановкой специальных эндотрахеальных стентов приводит к развитию рецидива стеноза у 75-90% больных. Как самостоятельный метод лечения бронхоскопические, особенно лазерные, вмешательства абсолютно показаны на ранних этапах развития грануляционно-рубцовых стенозов, при которых они эффективны у 50% больных. При критических сужениях трахеи рубцовой этиологии лазерная реканализация просвета трахеи является наиболее эффективным методом подготовки пациента к радикальной операции и позволяет избежать выполнения трахеостомии, которая к сожалению в подобных случаях ввиду поздней диагностики выполняется пока неоправданно часто. Трахеостомия удлиняет сроки лечения пациентов, усложняет их предоперационную подготовку, и, что самое главное, увеличивает протяженность резецируемого патологически-измененного участка трахеи, а иногда делает радикальное лечение и вовсе невозможным. При наличии относительных противопоказаний к резекции трахеи при диаметре ее просвета менее 5 мм показано временное эндоскопическое восстановление просвета трахеи до 6-8 мм, которое позволяет восстановить дыхание и адекватно подготовить пациента к радикальной операции. В течение 1-2 недель проводится терапия, направленная на компенсацию гипоксии, стабилизацию сердечной деятельности, купирование воспалительного синдрома и интоксикации. Ежедневно проводятся санационные бронхоскопии, во время которых проводится промывание бронхов антисептическими растворами и эвакуируется их патологическое содержимое. 9 Профилактика Как и многие другие заболевания, стеноз трахеи легче предупредить, чем лечить. Для предупреждения его развития необходима система мер, включающая высокую квалификацию врачей и медицинских сестер, их высокую медицинскую культуру на базе должного материального оснащения больниц, начиная от районных и заканчивая многопрофильными клиническими. При любых манипуляциях на трахее (смена трубок, канюль, катетеризация) необходимо соблюдать правила асептики. Профилактика посттрахеостомических РСТ заключается в ограничении показаний к первичной трахеостомии в экстренных условиях, максимально заменяя ее интубацией трахеи. После интубации больного можно доставить в специализированный стационар, где после решения вопроса о необходимости продленной ИВЛ ему в условиях операционной квалифицированным хирургом будет под эндотрахеальным наркозом наложена адекватная, предпочтительнее, нижняя (на уровне 3-4 хрящевых полуколец) трахеостома. При длительной операции или продленной ИВЛ необходим контроль за давлением в манжетке, регулярное (через- 1,5-2 часа) его снижение, перемещение трубки (вверх-вниз) с чередованием уровня расположения манжетки. Эти простые мероприятия позволяют избежать развития ишемии стенки трахеи. Немаловажное значение имеет использование современных интубационных трубок. После перевода больных с управляемого на самостоятельное дыхание необходимо перед удалением интубационной трубки или трахеостомической канюли проводить обязательное фибробронхоскопическое исследование. По данным Московского НПЦ оториноларингологии (2004) после экстубации и деканюляции различные патологические изменения в гортани выявляются у 81% пациентов, в шейном отделе трахеи – у 18%, в грудном – 1%. Их ранняя диагностика позволяет назначить адекватную терапию и предупредить развитие РСТ. В заключение следует подчеркнуть, что внедрение в практику новых диагностических и лечебных технологий, выполнение хирургических вмешательств по строгим индивидуальным показаниям, коллегиальное решение сложных тактических вопросов в интересах больного торакальными хирургами, ЛОР-врачами и врачами эндоскопистами, проведение профилактических мероприятий позволяет надеяться на прогресс в реконструктивной хирургии трахеи.