Углекислотный риформинг природного газа
реклама

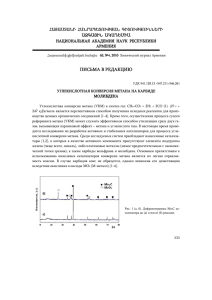
УДК 665. 644.4; 665.612.3 Г.Д.Закумбаева, Ш.С. Иткулова, Г.Ж.Елигбаева УГЛЕКИСЛОТНЫЙ РИФОРМИНГ ПРИРОДНОГО ГАЗА НА КАТАЛИЗАТОРЕ АСК-3 Введение В последнее время внимание как ученых, так и политиков приковано к глобальным проблемам человечества, связанных, в первую очередь, с изменением климата Земли, а также поиском и созданием альтернативных источников сырья для энергетики и нефтехимической промышленности в связи с неизбежным истощением нефтяных запасов /1-6/. Реальным альтернативным сырьем для нефтехимической промышленности и энергетики может служить природный газ /7-11/, переход на который можно осуществить с использованием имеющейся инфраструктуры нефтехимической промышленности. В настоящее время разведанные мировые запасы природного газа (в основном метана) составляют 150-160 трлн. м3. При существующем уровне добычи природного газа в 2,4 трлн. м3 в год этих запасов должно хватить на 65 лет. Разведанные запасы природного газа в Казахстане - 2,7 млрд м3 /9/. Природный газ состоит в основном из метана (до 98%), остальное приходится на этан, пропан, бутан и другие вещества /10/. Надо отметить, что метан наряду с диоксидом углерода является основным парниковым газом. К парниковым относят газы, создающие в атмосфере экран, который задерживает инфракрасное излучение Земли в космос, в результате чего прогревается нижний слой атмосферы /4,12/. По этой причине утилизация метана имеет также экологическое значение. В настоящее время освоено промышленное производство большого количества важных продуктов из метана, в том числе и синтез-газа, идущего далее на производство метанола или разнообразных углеводородов по методу Фишера-Тропша (промышленно-освоенные процессы) /13/. «Синтез-газ» - широко распространенное название смеси оксида углерода и водорода, в которых в зависимости от используемого метода получения мольное соотношение СО/Н2 может колебаться от 2 : 1 до 1 : 3 /14/. Существуют три основных каталитических способа получения синтез-газа разного состава: - парциальное окисление метана: СН4 + 1/2О2 → СО + 2Н2 (Н2/СО=2/1) (1) - углекислотная конверсия метана: СН4 + СО2 → 2СО + 2Н2 (Н2/СО=1/1) (2) - паровой риформинг: СН4 + Н2О → СО + 3Н2 (Н2/СО=3) (3) Первый из них, хотя и дает привлекательное отношение Н2/СО, требует особых мер предосторожности, и находится на стадии лабораторных испытаний. Паровой риформинг, промышленно-освоенный процесс, имеет недостаток, связанный с высоким соотношением Н2/СО=3, не пригодного для синтеза Фишера-Тропша. Процесс, протекающий по уравнению 2, называемый риформинг метана диоксидом углерода, «сухой» риформинг метана, или углекислотная конверсия метана, представляет особый интерес, поскольку позволяет утилизировать одновременно два парниковых газа – метан и диоксид углерода. Сухой риформинг СН4 диоксидом углерода пока не получил широкого распространения в промышленности, поскольку основной проблемой является зауглероживание катализатора, которое представляется неизбежным, особенно при использовании никелевых катализаторов. Основные усилия в данной области направлены на разработку устойчивых к коксообразованию катализаторов. В настоящей работе был синтезирован новый биметаллический катализатор на основе кобальта и металла переходного ряда - АСК-3 и изучен в процессе углекислотной конверсии метана. Экспериментальная часть Процесс проводили в проточном реакторе при атмосферном давлении в отсутствии и присутствии паров воды при соотношении СН4/СО2, равном 1:1, объемной скорости подачи сырья 1500 ч-1 и варьировании температуры опыта от 300 до 970оС и температуры прокаливания в пределах 200-400оС. Анализ исходных и конечных продуктов реакции проводился с помощью газовой хроматографии в режиме “on-line”. Результаты и их обсуждение На биметаллическом катализаторе 5%Со-M/Al2O3 – АСК-3 с равным весовым количеством металлов в активной фазе Со-М=1:1, прокаленном при (Тпрок) 200оС, конверсия СН4 составляет 8.8%, а СО2 – 32.2% при 400оС (табл. 1). При этой температуре опыта начинается образование Н2 (SH2 составляет – 27.3%), а образования СО не наблюдается. Это может быть связано с тем, что идет поглощение СО2 катализатором с образованием промежуточных адсорбированных форм (карбонатно-карбоксилатные соединения) и разработка поверхности катализатора. Образование СО начинается при 600оС, SСО составляет 4.5%. С дальнейшим повышением температуры от 400 до 780оС происходит увеличение конверсии метана от 8.8 до 35.6%. Зависимость конверсии СО2 от температуры носит экстремальный характер. Она повышается от 32.2 до 53.7% с ростом температуры от 400 до 550оС и падает до 27.3% при дальнейшем повышении температуры до 780оС. Зависимость конверсии метана и СО2 от температуры показана на рис. 1. При повышении температуры процесса от 400 до 780оС происходит увеличение выхода основных продуктов реакции Н2 и СО, резко возрастающее при tоп > 600 для СО и > 700oC для Н2. Максимальное значение селективности достигается при 780оС, равное 76.9% для Н2 и 100% для СО. Таблица 1. Влияние условий реакции на риформинг метана диоксидом углерода на катализаторе АСК-3 (СН4/СО2=1/1, Р=1атм, V=1500ч-1) tоп, оС Конверсия, % К CH 4 Селективность, % H2 CO Н2/СО 8.8 22.8 35.6 К CO2 Тпрок=200оС 32.2 27.3 30.6 64.0 27.3 76.9 0.0 92.8 100 0.5 0.6 800 20.9 Тпрок=300оС 73.6 100 58.6 0.5 900 970 62.9 100 66.9 90.0 100 100 100 100 0.9 1.3 400 750 800 Тпрок=400оС 800 8.5 68.2 94.1 100 0.4 900 970 37.9 86.7 73.8 91.0 100 100 100 100 0.6 1.1 При варьировании температуры в пределах 700о-780оС соотношение Н2/СО колеблется от 0.5 до 0.9 (рис. 1-а). Максимальное отношение Н2/СО=0.9 наблюдается при 700оС. При повышении температуры процесса от 400 до 780оС происходит увеличение выхода основных продуктов реакции Н2 и СО, резко возрастающее при tоп > 600 для СО и > 700oC для Н2. Максимальное значение селективности достигается при 780оС, равное 76.9% для Н2 и 100% для СО. При варьировании температуры в пределах 700о-780оС соотношение Н2/СО колеблется от 0.5 до 0.9 (рис. 1-а). Mаксимальное отношение Н2/СО=0.9 наблюдается при 700оС. Надо отметить, что в продуктах реакции обнаружены кислородсодержащие продукты, в основном уксусная кислота с выходом 0,9% при температуре 750оС, найдены следовые количества С2-С4 углеводородов (табл. 2). Таблица 2. Состав продуктов, образующихся при риформинге метана на катализаторе АСК3, прокаленном при разных температурах (СН4/СО2=1/1, Р=1атм, V=1500ч-1) Тпрок., °С Топ, оС Конверсия, % СН4 СО2 Селективность, % Н2 СО H2/CO Выход продуктов, % кислородс углеводороды одержащи 200 300 400 750 750 970 750 970 22.8 17.1 100 7.1 86.7 30.6 71.9 90.0 59.0 91.0 64.0 89.5 100 81.7 100 92.8 39.5 100 100 100 0.5 0.5 1.3 2.1 1.1 сл. С2-С4 сл. С2-С5 - е 0.9 4.3 1.7 - На катализаторе АСК-3, прокаленном при 3000 С, процесс начинается при температуре 5000С. В этих условиях конверсия метана составляет – 5.5%. При этом образования водорода не наблюдается. Н2 начинает появляться при температуре 550оС, селективность - 21.8%. СО образовывается при более высокой температуре 6000 С, SСО – 4.2% (табл. 1, рис. 1-б). С последующим повышением температуры конверсия метана непрерывно растет, достигая максимального значения – 100% при температуре 9700С. Для СО2 наблюдается два экстремума. В пределах 500-850 конверсия СО2 проходит через первый максимум при Т=800оС (КСО2= 73.6%), снижается до 57.0 (Топ=850оС), далее КСО2 растет до 90.0% при Топ=970оС (рис. 1-б). Зависимости конверсии СН4 и СО2 и выхода Н2 и СО от температуры показаны на рисунке 1-б. Из рисунка видно, что выходы как СО, так и Н2 непрерывно растут, причем резкое возрастание их выхода происходит при tоп>800оС. С повышением температуры от 750 до 9700С Н2/СО растет от 0.5 до 1.3. Надо отметить, что при температуре ≤7500С в продуктах реакции также содержатся кислородсодержащие продукты, выход которых составляет 4.3% (табл. 2). Причем преимущественно образуются уксусная и пропановая кислоты. Их содержание в жидкой фракции >90%. Углеводороды не образуются. На катализаторе, прокаленном при 4000С, конверсия метана заметна при температуре 5500С и составляет 1.1%. Конверсия СО2– 19.5% (рис.1-в). В этих условиях Н2 и СО не обнаружены. Их выходы наблюдаются = 600оС, SН2 =60.9% и SСО =100%. а) Тпрок.=200°С б) Тпрок.=300°С Рис. 1. Влияние температуры процесса углекислотного риформинга метана на активность и селективность катализатора 5%Со-M(1:1)/Al2O3, прокаленного при различных температурах прокаливания в) Тпрок.=400°С С дальнейшим повышением температуры от 600 до 9700С наблюдается повышение конверсии как метана (от 4.6 до 86.7%), так и СО2 (от 55.2 до 91.0%) (Рис. 1-в). С ростом температуры идет увеличение образования основных продуктов реакции Н2 и СО. Максимальное значение селективности по Н2 - 100% достигается при температуре 9000С, отношение Н2/СО равно 0.6. В интервале температур 925-9700С отношение Н2/СО достигает 1.1 (табл. 1). При t ≤ 750 0С образуются кислородсодержащие продукты, в основном уксусная кислота, выход которой составляет 1.7%, найдены следовые количества С2-С5 углеводородов. Анализ показывает, что оптимальной температурой прокаливания для катализатора 5%СоM(1:1)/Al2O3 является 3000С, при которой процесс полной конверсии метана наблюдается при 9700С, в этих условиях КСО2 равна 91,0%. Полученный синтез-газ имеет соотношение 1.3 и соответствует составу, пригодному для синтеза Фишера–Тропша (табл. 2). Заключение Полученные результаты демонстрируют, что АСК-3 катализатор является активным и селективным в процессе образования синтез-газа из СН4 путем его углекислотной конверсии. Из литературы /15/ известно, что на лучших катализаторах (Ni-содержащий катализатор) конверсия СН4 и СО2 при 800оС составляет 97,5%, при этом выход СО равен 97,1%. В процессе углекислотного риформинга на катализаторе АСК-3 степень конверсии CH4 достигает значения 90-92% при 900оС, при этом селективность по СО – 98%. Сравнение исследованных нами катализаторов с известными аналогами показывает, что они эффективны в процессе получения синтез-газа путем углекислотного риформинга метана. Полная конверсия метана происходит при температуре 970оС. При этом со 100%-селективностью образуется синтез-газ с отношением Н2/СО=1.1-1.3, которое соответствует составу синтез-газа, пригодного для синтеза ФишераТропша. Главным преимуществом синтезированного катализатора является отсутствие коксообразования, что позволяет его использование. При изучении риформинга СН4-СО2 на биметаллических катализаторах наблюдается закономерность: с повышением температуры происходит тенденция к возрастанию степени превращения СН4 и СО2 и соответственно выхода продуктов реакции. Основными продуктами углекислотной конверсии метана на биметаллическом катализаторе 5% Со-М/Al2O3 при атмосферном давлении являются водород и оксид углерода (синтез-газ), а также образуются вода и дополнительно уксусная кислота. ЛИТЕРАТУРА 1. Centi G. and Perathoner S. Catalysis: Role and Challenges for a Sustainable Energy // Topics in Catalysis, 2009. – Р.67. 2. Christensen C. H. Catalysis for Sustainability // Topics in Catalysis, 2009. – Р.94. 3. Moskovits M. Catalysis and Alternatives to Liquid Fuels // Topics in Catalysis, 2009. –Р.47. 4. Xiaoding X. and Moulijn J. A. Mitigation of CO2 by Chemical Conversion: Plausible Chemical Reactions and Promising Products. // Energy & Fuels, 1996. – V. 10. – P. 305 – 325. 5. Бернер У., Холлербах А. Каталитическая система Земли – влияние диоксида углерода? // Ж. Черные металлы. - 2002. -№3. -С. 46-51. 6. Пармон В.Н. Каталитические технологии будущего для возобновляемой и нетрадиционной энергетики / Химия в интересах устойчивого развития. -2000. -№8. -С. 556. 7. Петров А.А. Переработка природного газа в жидкие углеводороды // Катализ в химической и нефтехимической промышленности. -2002. -№2. 8. Крылов О.В. Новое в каталитической переработке природного газа // Катализ в промышленности. 2002. -№ 2. 9. Попова Н.М., Досумов К. Катализаторы селективного окисления и разложения метана и других алканов. – Алматы: Ғылым, 2007.- 208 с. 10. Булкатов А.Н. Новые направления прямой переработки метана в химическое сырье для нефтехимии // Нефтепереработка и нефтехимия. – 2009. - №10. –С.3-7. 11. Арутюнов В.С., Крылов О.В. Окислительная конверсия метана // Успехи химии. -2005. -№12. – С. 1216-1243. 12. Данилов-Данилян В.И., Лосев К.С. Экологический вызов и устойчивое развитие. – М.: ПрогрессТрадиция, 2000. – 379 с. 13. Wilhelm, D.J., Simbeck, D.R., Karp, A.D., Dickenson, R.L. Syngas production for gas-to-liquids applications: technologies, issues and outlook // Journal Fuel Processing Technology. –V. 71. -2001. –Р.139-148. 14. Шелдон Р.А. Химические продукты на основе синтез-газа // Пер.с англ. Под ред. С.М. Локтева. – М.: Химия, 1987. – 248 с. 15. Крылов О.В. Углекислотная конверсия метана в синтез-газ// Ж. Российского хим. Общества им. Д. И. Менделеева. –М., 2000. -Т. XLIV. - № 1. -С. 19-33. Резюме Құрамында СО және ауыспалы металл бар жаңа биметалды АСК-3 катализаторы синтезделді және метанның құрғақ риформингісінде сыналды. Метанның құрғақ риформингі кезінде катализатор белсенділік көрсеткені анықталды. Метанның толық конверсиясы 970 0С-та байқалды. АСК-3 катализаторында синтезгазды селективті өндіру мынадай қатынаста болды: Н2/СО=1.1-1.3, және де сірке қышқылының белгілі мөлшерінің түзілуі орын алды. Осы кезде катализатор кокспен жамылып қалмады. Summary The new bimetallic catalyst on a base of Co and containing transition metal - ACK-3 has been synthesized and tested in dry reforming of methane. It has been established that the catalyst performs activity in dry reforming of methane. Complete methane conversion is occurred at 970oC. Synthesis-gas with a ratio of H2/CO=1.1-1.3 is selectively produced over the ACK3 catalyst. Also, some amount of acetic acid is produced. There is no coke formation over the catalyst. Key words: bi-reforming of methane, catalyst, synthesis-gas КазНТУ им. К.И.Сатпаева Институт ОКиЭХ им. Д.В. Сокольского Поступила 2.107.10