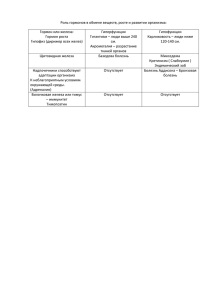
Переходные металлы Cr, Mn, Fe, Cu Термин «переходные» связан с тем, что в периодах эти элементы располагаются между s - и р-элементами. Переходные металлы выделяют на основании незавершённости внутренних электронных оболочек их атомов или ионов. Форма электронных облаков и последовательность заполнения подуровней электронами Железо 26Fe Хром 3d5 более энергетически выгодно, чем 3d4, у хрома происходит проскок (провал) электрона 24Cr Mn 25 Cu 29 провал электрона Физические свойства хром железо марганец медь Получение ✓ Карботермия (С, СО) ✓ Гидротермия (H2) ✓ Металлотермия ( Al, Mg) Химические свойства ✓ + простые вещества ! neMet, являющиеся сильными окислителями, окисляют Fe и Cr до +3 ! neMet, являющиеся слабыми окислителями, — до +2 ! Fe, Mn, Cr не реагируют с водородом и азотом ✓ + H2O 3Fe + 4H2O = Fe3O4 + 4H2 Mn + 2H2O = Mn(OH)2 + H2 Cu + H2O = не реагирует ✓ + кислоты Cr + 2HCl → CrCl2 + H2↑ 2Cr + 6H2SO4 конц → (t) Cr2(SO4)3 + 3SO2 + 6H2O ! Cr, Fe не реагирует при н.у. с HNO3конц., H2SO4конц. из-за пассивации ! Cu с H2SO4разб. не реагирует, с HNO3разб. - реакция идет ! Сu реагирует с царской водкой Cu + 4HNO3(конц.) = Cu(NO3)2 + 2NO2↑ + 2H2O 3Cu + 8HNO3(разб.) = 3Cu(NO3)2 + 2NO↑ + 4H2O 3Cu + 2HNO3 + 6HCl = 3CuCl2 + 2NO + 4H2O ✓ + соли ✓ + окислители Cr + KClO3 = Fe + KNO3 + KOH = Феррат натрия (слева) Перманганат калия (справа) Соединения хрома CrO Cr(OH)2 Cr2O3 CrO3 Cr(OH)3 H₂CrO₄ Хромовая кислота Соединения железа FeO Fe(OH)2 Fe2O3 Fe(OH)3 Химические свойства соединений Сr, Fe Оксиды: ✓ + H2O не взаимодействуют ✓ + кислоты ✓ + окислители ✓ + более активные Met Cr2O3 + Al = Al2O3 + Cr ✓ реакция вытеснения (Fe2O3 и Cr2O3 способны вытеснять летучие CO2 и SO2 из их солей) Химические свойства соединений Сr , Fe Гидроксиды: ✓ + кислоты ✓ + термическое разложение ✓ + окислители ✓ + щелочи Качественные реакции на ионы Fe +2 Взаимодействие солей железа (II) с щелочами , образуется серо-зеленый студенистый осадок Fe(OH)2 Взаимодействие солей железа (II) с красной кровяной солью K3[Fe(CN)6] образуется синий осадок «турнбулева синь») Качественные реакции на ионы Fe +3 ✓ Взаимодействие солей железа (III) с щелочами, образуется бурый осадок Fe(OH)2 ✓ Взаимодействие с желтой кровяной солью K4[Fe(CN)6] , образуется синий осадок «берлинская лазурь» ✓ Взаимодействии солей железа (III) с роданидами NaCNS раствор окрашивается в кроваво-красный цвет Соединения марганца Mn2O7 — зеленоватобурая или красная маслянистая жидкость с металлическим блеском Соединения железа