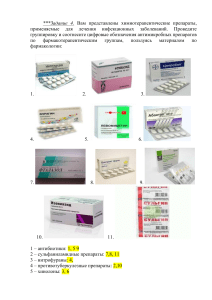
Нежданова. Учебное пособие. Соматические заболевания детей старшего возраста. Детские инфекции
реклама

Соматические заболевания детей старшего возраста и детские инфекции (клиника, диагностика, лечение) Пособие для студентов лечебного отделения, врачей-интернов, практических врачей (издание четвертое, переработанное) Саранск, 2012 г. Печатается по решению научно-методического совета медицинского института ГОУ ВПО "Мордовский государственный университет имени Н.П. Огарева" АННОТАЦИЯ В пособии представлены особенности клинических проявлений заболеваний детей старшего возраста, вопросы ранней и дифференциальной диагностики, принципы терапии и профилактики. Пособие содержит задания тестового контроля, ситуационные задачи. Пособие предназначено для студентов 5 курса специальности «Лечебное дело» медицинских вузов, интернов, клинических ординаторов, а также может быть использовано в работе врачей общей практики. Составители: Рецензенты: д.м.н. Л.А. Балыкова, к.м.н. Т.Г. Атясова, д.м.н. М.В. Нежданова, к.м.н. Л.И. Дзюбич, к.м.н. Т.И. Раздолькина, к.м.н. Е.И. Науменко, к.м.н. Самошкина, к.м.н. Л.В. Ледяйкина, д.м.н. Н.Г. Герасимова, к.м.н. В.С. Верещагина, педиатр - консультант МЗ РМ А.А. Бровкина заведующая кафедрой поликлинической терапии, доктор медицинских наук, профессор А.В. Зорькина ГОУ ВПО "Мордовский государственный университет имени Н.П. Огарева" Бумага офсетная. Формат 60х84 1/16. Гарнитура Таймс. Печать способом ризографии. Усл. печ. л. 7,67. Уч.- изд. л. 10,16. Тираж 300 экз. Заказ № . Отпечатано с оригинала-макета заказчика в ООО «Референт».. 430000, Г. Саранск, пр. Ленина, 21. тел. (8342) 48-25-33 Занятие № 1. БРОНХИАЛЬНАЯ АСТМА У ДЕТЕЙ Цель занятия: Познакомить студентов с основными литературными источниками по данной теме, научить их грамотно формулировать развернутый клинический диагноз, назначить необходимые лабораторно-инструментальные исследования и дать план обследования в зависимости от формы, степени тяжести и фазы болезни. Вопросы для самоподготовки: 1. Какое заболевание следует считать бронхиальной астмой? 2. Что является факторами риска возникновения бронхиальной астмы? 3. Что является факторами, вызывающими обострение бронхиальной астмы (триггерами)? 4. Каков патогенез этого заболевания? 5. Какова современная рабочая классификация бронхиальной астмы, предложенная И.И.Балаболкиным и М.Я.Студеникиным (1998г.)? 6. Каковы критерии оценки степени тяжести бронхиальной астмы у детей? 7. Объем базисной терапии и лечение больных в период ремиссии? 8. Какова лечебная тактика в приступный период в зависимости от тяжести приступа бронхиальной астмы? 9. Диспансеризация больных бронхиальной астмой. Бронхиальная астма (БА) – это хроническое аллергическое воспалительное заболевание бронхов, основой которого является их обратимая обструкция, приводящая к приступам удушья и возникающая вследствие их врожденной и приобретенной гиперреактивности на аллергены или неспецифические факторы. Факторами риска возникновения БА у детей являются: 1. Атопия. 2. Гиперреактивность бронхов. 3. Отягощенная аллергологическая наследственность. Причинные (сенсибилизирующие) факторы: бытовые аллергены (клещи домашней пыли), эпидермальные аллергены животных, птиц (шерсть, пух, перо), пыльцевые аллергены, грибковые, пищевые аллергены (шоколад, яйца, рыба, икра, кофе, какао, цитрусовые, клубника), лекарственные средства, предметы бытовой химии, вирусы и вакцины. Факторами, вызывающими обострение БА (триггерами) являются аллергены, указанные выше, респираторные вирусы, физические и психо-эмоциональные нагрузки, изменение метеоситуации, экологические воздействия (табачный дым, резкие запахи и т.д.). Патогенетической основой БА является хроническое аллергическое воспаление бронхов, затрагивающее все структуры и сопровождающееся их гиперреактивностью. Другим важнейшим патогенетическим механизмом является бронхиальная обструкция, которая носит диффузный характер и имеет 4 формы: 1. Бронхоконстрикция вследствие спазма гладких мышц бронхов. 2. Подострая обструкция вследствие отека их слизистой оболочки. 3. Хроническая обструкция вследствие обтурации бронхов вязким секретом. 4. Необратимая обструкция вследствие склеротического процесса в стенке бронхов. БА страдает до 8% населения, а в детской популяции этот процент повышается до 10. БА, начавшаяся в детстве, в 60-80% случаев продолжается и у взрослых. Летальность при тяжелых формах БА у детей составляет 1-3%, а при кортикостероидозависимой астме достигает 6%. Таблица 1. Классификация БА у детей (И.И.Балаболкин, М.Я.Студеникин, Москва, 1998; А.Г.Чучалин, А.А.Баранов, Москва, 2006) Форма Фаза болезни Степень Степень Осложнения болезни тяжести контроля Атопическая Обострение Легкая Контролируемая Ателектаз легких НеатопичеПриступ БА интермиттиПневмоторакс ская (легкий, средне- рующая Частично контяжелый, тяжеперсистирующая тролируемая Подкожная, мелый) диастинальная Астматическое Среднетяжелая Неконтролируеэмфизема состояние мая Легочное сердце Ремиссия Тяжелая Таблица 2 Оценка степени тяжести БА у детей Критерии Частота приступов Легкая форма Не чаще 1 раза в мес. ночные приступы реже 1 раз в мес. Среднетяжелая форма Чаще 1 раза в мес. В периоде обострения до 3 раз Степень тяжести приступов Легкие, умеренно выраженные Кашель Эпизодический, преходящий Экспираторная. Вне приступа ее нет Мало, трудно отделяемая, стекловидная В конце выдоха, сухие, исчезающие 80% и более Приступы средней степени тяжести, редко тяжелые Пароксизмальный, малопродуктивный При физической нагрузке Умеренное количество, вязкая Сухие и/или влажные Одышка Мокрота Хрипы Показатели ПСВ в период обострения Дыхательная недостаточность Ремиссия Тяжелая форма Приступы часто повторяющиеся, в периоде обострения – ежедневные. Ночные приступы более 2-х раз в мес. Приступы тяжелые Постоянный, продуктивный В покое от 60 до 80% Большое количество, слизистогнойная, вязкая По всем легочным полям сухие и влажные Менее 60% Нет Умеренная, I,II cт. Выраженная II, III ст. Полная Неполная фармакологическая Менее 3 мес. Легочное сердце, стероидозависимость Не показана Недостаточный Длительность ремиссии Осложнения 3 мес. и более Неполная или фармакологическая Менее 3-х мес. Нет Хронический бронхит Иммунотерапия Эффект бронхолитиков Использование кортикостероидов Госпитализация Суммарная длительность периодов обострения в год Эффективна Хороший Менее эффективна Высокий, но не всегда Не применяются Ингаляционные Редко Менее 3 мес. При обострении От 3 до 6 мес. Ингаляционные и системные в том числе Часто, при обострении от 6 до 12 мес. Приступ БА – это острое состояние экспираторного удушья, затрудненного или свистящего дыхания и спастического кашля при существенном снижении показателя пиковой скорости выдоха (ПСВ). Период обострения БА – это дни, недели, или месяцы в течение которых имеется клинически выраженный или скрытый синдром бронхиальной обструкции, определяемый по показателям ПСВ. В это время острые приступы БА могут повторяться. Период ремиссии – это период клинического благополучия. Ремиссия может быть полной или неполной в зависимости от показателей функции внешнего дыхания, а также ремиссия может быть фармакологической, т.к. сохраняется на фоне приема медикаментов. При эпидемиологических исследованиях выявлено, что тяжелая БА у детей диагностируется у 5% больных, среднетяжелая – у 25-30% и легкая – у 65-70%. Во время приступа удушья больные принимают вынужденное положение. Кожа становится бледно-серого цвета, отмечается периорбитальный, периоральный цианоз или акроцианоз. Кашель малопродуктивный. Выдох шумный с участием вспомогательной мускулатуры, слышны дистанционные свистящие хрипы. Выражена экспираторная одышка. Перкуторный звук высоко тимпанический, дыхание ослаблено. В обеих легких выслушиваются сухие свистящие хрипы. Пульс малого наполнения. Тоны сердца приглушены. Таблица 3 Критерии оценки тяжести приступа Легкий приступ СреднетяжеТяжелый АстматичеКритерии лый ский статус Физическая сохранена ограничена вынужденное по- отсутствует активность ложение Речь сохранена произносит речь затруднена отсутствует отдельные фразы Сознание иногда возбуж- возбуждение возбуждение, спутанное дение испуг сознание, кома Частота дыдыхание учавыраженная резко выраженная тахипноэ или ханий щено экспираторная экспираторная брадипноэ одышка одышка Участие нерезко выраВыражено резко выражено парадоксальвспомогажено ное дыхание тельной мускулатуры Свистящее в конце выдоха Выражено резко выражено «немое» легдыхание кое Частота пуль- учащена Учащена резко учащена брадикардия са Показатели более 80% 60-80% менее 60% ПСВ РО2 в норме более 60 мм менее 60 мм РСО2 Менее 45 мм рт. менее 45 мм более 45 мм рт. ст. ст. рт. ст. Лечение бронхиальной астмы Существенный прогресс в лечении БА был достигнут после внедрения базисной терапии, направленной на ликвидацию аллергического воспалительного процесса в бронхах. Она заключается: 1) в назначении нестероидных противовоспалительных препаратов: кромгликата натрия (интала) или недокромила натрия (тайледа), или кромогена или рузама; 2) в использовании ингаляционных или системных кортикостероидов; 3) в назначении специфической и неспецифической иммунотерапии. Базисная терапия проводится с учетом тяжести заболевания длительно и отменяется при достижении стойкой ремиссии. Больным с легкой и среднетяжелой формой БА назначаются такие нестероидные противовоспалительные средства, как интал, тайлед, кромоген, рузам. Интал предупреждает развитие приступов удушья. Ингаляции этого препарата производят 4 раза в день. Курс лечения не менее 1,5-2 месяцев. Тайлед в 6-8 раз сильнее интала. Его применяют по 2 ингаляции в день не менее 2 мес. Кромоген назначается по 1-2 мкг 4 раза в сутки. При среднетяжелом течении ингаляции интала производят 4 раза в сутки или ингаляции тайлед 2-4 раза в сутки. В случае недостаточной эффективности в течение 6-8 недель эти препараты заменяются ингаляционными кортикостероидами в среднетерапевтических дозах. Таблица 4 Суточные дозы ингаляционных кортикостероидов Препараты Средние дозы Высокие дозы Беклометазон 400-600 мкг > 600 мкг Будезонид 200-400 мкг > 400 мкг Флунисомед 500- 1000 мкг > 1000 мкг Флуктиказон 200-400 мкг > 400 мкг Триамцинолон ацетонид 800-1000 мкг > 1000 мкг Альдецин 50-100мкг > 100 мкг Фликсотид 100мкг > 1000 мкг Пульмикорт 100мкг > 1000 мкг При обострении одновременно с противовоспалительной терапией назначаются теофиллины пролонгированного действия до 2-х недель: теотард, теопек, ретафил, теодур, эуфиллонг в суточной дозе 12-15 мг/кг. Вместо этих препаратов можно назначить β2-агонисты пролонгированного действия: серевент в суточной дозе 100 мкг или форадил в суточной дозе 24 мкг, вольмакс, спиропент. Детям с легкой и среднетяжелой формой БА показано применение антилейкотриеновых препаратов: задитен (кетотифен) детям в возрасте старше 3-х лет назначают по 1 таблетке (1 мг) 2 раза в день. Полный терапевтический эффект от применения этого препарата наступает через 6-12 недель. К лекарствам этой же группы относятся зилетон, зафилукаст, монтелукаст (сингуляр). Для лечения используется комбинированные препараты: серитид по 4 мкг 2 раза в день и дитек по 1-2 дозы 4 раза в день и симбикорт. При тяжелом течении БА назначаются ингаляционные кортикостероиды в высоких дозах. При недостаточном эффекте можно назначить энтерально кортикостероиды (преднизолон) в дозе 1-2 мг/кг в сутки в течение 5-7 дней. Кроме этого применяются теофиллины и β2-агонисты пролонгированного действия. В период ремиссии в качестве превентивной терапии используется специфическая иммунотерапия, гистаглобулин, противоаллергический иммуноглобулин по 1-2 мл в/м через 4 дня. На курс 5 инъекций. Применяются препараты неспецифической иммунотерапии: полиоксидоний 0,1 мг/кг, ликопид 0,001 1 раз в день и препараты интерферона. При инфекционно-зависимой форме БА в период ремиссии можно использовать иммуностимуляторы бактериального происхождения: бронхомунал, бронховаксон, рибомунил, поликомпонентная вакцина, а также иммуномодуляторы: Т-активин, нуклеинат натрия, пентоксил. В период ремиссии БА назначаются различные методы физиотерапии: магнитотерапия, лазерная терапия, аэроионотерапия, иглорефлексотерапия, спелеотерапия, галотерапия. Больным назначаются массаж грудной клетки, лечебная физкультура, дыхательная гимнастика с волевым управлением дыхания. Проводится санация вторичных очагов инфекции. Значительное внимание уделяется фитотерапии с использованием растений, оказывающих противовоспалительное действие: девясил, зверобой, календула, солодка, подорожник. Всем больным рекомендуется соблюдать гипоаллергенную диету и лечение в санаториях. Для снятия приступа удушья у больных БА используют β2-агонисты короткого действия, антихолинергические препараты, теофиллины короткого действия. Предпочтение отдается ингаляционным формам этих препаратов, позволяющим получить быстрый эффект. К β2-агноистам короткого действия относятся следующие препараты: вентолин, сальбутамол – применяется в суточной дозе 400 мкг, бриканил – до 1000 мкг в сутки, беротек – до 400 мкг в сутки. Ингаляционные формы этих медикаментов назначаются не более 4 раз в сутки в течение 7-10 дней. При легких приступах БА можно использовать энтеральные формы сальбутамола и вентолина. К теофиллинам короткого действия, прежде всего, относятся эуфиллины. Парентеральная средняя терапевтическая доза его у детей до 3-х лет составляет 5-10 мг/кг/сут; от 3 до 14 лет – 10-15 мг/кг/сут. К антихолинергическим препаратам относятся такие ингаляционные средства, как ипратропиум бромид, окситропиум бромид, атровент. Бронходилатирующий эффект при применении этих медикаментов наступает через 30 минут после ингаляции. Наиболее эффективны антихолинергические препараты при приступах БА, возникающих на фоне респираторной вирусной инфекции. При тяжелом приступе БА проводятся мероприятия, направленные на устранение бронхоспазма, уменьшение вазосекреторных расстройств, разжижение и удаление мокроты, ликвидацию дыхательной, сердечной и надпочечниковой недостаточности, гипоксии и метаболических нарушений. Всем больным обязательно назначается оксигенотерапия. Основными начальными средствами для купирования приступа удушья являются β2агонисты короткого действия: сальбутамол, бриканил, беротек, вентолин. Наилучшим способом их применения является ингаляционный с использованием небулайзера. Проводятся ингаляции каждые 20 минут в течение всего первого часа. Эффект наступает через 5-10 минут и длительность действия сохраняется 4-6 часов. При недостаточной эффективности ингаляционных препаратов в течение первого часа дополнительно назначается парентеральное введение бриканила, орципреналина, гексапренолина или адреналина. Действие адреналина, введенного подкожно или внутримышечно, начинается через 15-20 минут и длится 1-2 часа. Для лечения тяжелого приступа удушья (астматический статус, асфиктический синдром) используются теофиллины короткого действия (эуфиллины и теофиллины). Нагрузочная доза их составляет 4,5-5 мг/кг в течение 20-30 минут. В последующем эуфиллины вводятся при непрерывной инфузии в дозе 0,6-1 мг/кг/час или дробно через каждые 4-6 часов. В лечении тяжелого приступа БА важнейшее место занимают системные кортикостероидные гормоны. Препаратом выбора является преднизолон (метилпреднизолон), который вводится каждые 4-6 часов в/мышечно или в/венно в суточной дозе 8-10 мг/кг до выведения больного из астматического состояния. Для получения быстрого эффекта 1/4-1/5 рассчитанной дозы преднизолона вводится в/венно струйно, а оставшаяся доза вводится в/венно капельно. Если приступ не купируется, преднизолон назначается и внутрь: детям до 1 года – в суточной дозе 1-2 мг/кг; 1-5 лет – 20 мг в сутки, старше 5 лет – 20-60 мг в сутки коротким курсом в 3-10 дней. Абсолютным показанием для назначения преднизолона в таблетках является асфиктический синдром. До стабилизации состояния суточная доза препарата распределяется равномерно в течение суток, а в дальнейшем он назначается с учетом циркадного ритма функции коры надпочечников. При улучшении состояния дозу энтерального преднизолона уменьшают, добавляя ингаляционные кортикостероиды в повышенной дозе (800-1000 мкг в сутки), а затем постепенно переводят больных только на ингаляционные кортикостероиды. В комплекс лечебных мероприятий включается гепарин. В крайне тяжелых случаях больным назначаются поднаркозная бронхоскопия, плазмоферез и гемосорбция. При появлении симптомов дегидратации назначается регидратационная терапия. При проведении в/венной инфузионной терапии в качестве базисных растворов используются физиологический раствор пополам с 5% р-ром глюкозы в дозе 10-20 мл/кг. Скорость введения не должна превышать 12-14 капель в 1 минуту. Для улучшения окислительных процессов в/венно вводятся аскорбиновая кислота, кокарбоксилаза. Для разжижения мокроты назначаются бронхолитин, мукалтин, отвары отхаркивающих трав. При улучшении состояния назначаются ингаляции с муколитическими средствами (мукосальвин, N-ацетилцистеин, лазолван). При наличии инфекционно-воспалительных изменений в бронхолегочной системе назначаются антибиотики (цефалоспориновые производные, аминогликозиды, полусинтетические пенициллины). Дети, страдающие БА, наблюдаются диспансерно аллергологом и участковым педиатром. Аллерголог осматривает в период проведения специфической гипосенсибилизации и подбора диеты не реже 1 раза в неделю, а в остальное время – 1 раз в квартал. В период ремиссии ребенок должен осматриваться участковым педиатром: при тяжелом течении БА не реже 1 раза в 1-2 месяца; при легкой и среднетяжелой астме – не реже 1 раза в квартал. Отоларинголог и стоматолог должны осматривать больных БА не реже 2-х раз в год. В процессе диспансерного наблюдения участковый педиатр следит за общим состоянием ребенка, за физикальными изменениями в легких, за функциональным состоянием внешнего дыхания, за гематологическими показателями, выявляет и лечит очаговую инфекцию. Один раз в 3-6 месяцев исследуется кал на гельминты. Вопросы для тестового контроля № п/п 1 2 3 4 5 6 7 8 9 10 Содержание вопросов Патоморфологической основой бронхиальной астмы является: а) аллергический бронхит, б) хроническое аллергическое воспаление бронхов, в) хроническое аллергическое воспаление бронхов с их гиперреактивностью, Какие формы бронхиальной астмы выделены в классификации И.И.Балаболкина и М.Я.Студеникина: а) хроническая, б) атопическая, в) неатопическая, г) инфекционно-аллергическая, д) вирусная Какие фазы болезни указаны в классификации бронхиальной астмы, предложенной И.И.Балаболкиным и М.Я.Студеникиным: а) обострение, б) приступы бронхиальной астмы, в) астматический статус, г) ремиссия, д) период предвестников Триггерами при бронхиальной астме являются: а) поликистоз, б) аллергены, в) вирусы, г) метеоситуация, д) экологические факторы С помощью пикфлоуметра можно установить: а) жизненную емкость легких, б) резервный воздух, в) пиковую скорость выдоха, г) максимальный объем вдоха, д) все перечисленное Какие лекарственные средства составляют базисную терапию: а) недокромил натрия (тайлед), б) кромгликат натрия (интал), в) ингаляционные кортикостероиды (беклометазон, будезонид, флуктиказон), г) пролонгированные теофиллины (теотард, теопек, теодур, ретафил), д) бета-2-агонисты короткого действия (вентолин, брикантил, беротек, сальбутамол) Какие лекарственные препараты назначаются для снятия приступа бронхиальной астмы: а) эуфиллин, б) тайлед, в) вентолин, г).беротек, д) преднизолон При лечении астматического статуса используют: а) преднизолон, б) задитен, в) гепарин, г) эуфиллин, д) адреналин В период ремиссии БА применяются: а) фитотерапия, б) специфическая иммунотерапия, в) иглорефлексотерапия, г) УВЧ, д) лазерная терапия, е. эуфиллин. Профилактические прививки у детей с бронхиальной астмой проводятся: а) по календарю, б) по индивидуальному плану, в) по индивидуальному плану на фоне гипосенсибилизирующей терапии Эталоны ответов г б, в а, б, г б, в, г, д в а, б, в а, в, г, д а, в, г, д а, б, в, г, д в Ситуационные задачи № п/п 1 2 Содержание задач Саша С., 10 лет. Болен бронхиальной астмой с 5 лет. Приступы удушья возникают ежемесячно, иногда и ночью. Для снятия приступа достаточно сделать 1-2 вдоха ингаляционного беротека. Наблюдается диспансерно у участкового педиатра и аллерголога. В течение 2-х недель приступов затрудненного дыхания не было. Обратился к педиатру за советом по поводу лечения, т.к. уезжает в гости. Какие следует дать рекомендации по лечению ребенка? Вася Л., 5 лет, жалуется на кашель и приступы удушья. С 2-х месяцев страдал экссудативным диатезом, не переносит яйца, Эталоны ответов 1. Необходимо соблюдать гипоаллергенную диету. 2. Продолжить базисную противовоспалительную терапию: тайлед 2 ингаляции в сутки, задитен по 1 мг, отвар корня солодки. 3. Дыхательная гимнастика. 4. Лечебная физкультура. 1.Предварительный диагноз: бронхиальная астма, атопическая, средней степени тяжести, фаза обострения. цитрусовые и некоторые лекарственные препараты (анальгин, сульфаниламиды). С 3-х лет ежемесячно возникают приступы затрудненного дыхания: ребенок синеет, принимает вынужденное положение, дыхание становится частым с удлиненным свистящим выдохом. Приступы возникают преимущественно во время цветения растений. В настоящее время сохраняются кашель, дыхание с удлиненным выдохом. Грудная клетка вздута, при перкуссии легких определяется тимпанический оттенок перкуторного звука, прослушиваются жесткое дыхание и рассеянные «музыкальные хрипы». Вопросы: 1. Поставить предварительный диагноз. 2. Составить план обследования. 3.Назначить лечение. 2.План обследования: общ. ан. крови и мочи в 7-10 дней, посев мокроты на флору с определением чувствительности к антибиотикам. Ан. крови на белковые фракции, иммунограмма. Ан. кала на яйца глистов, лямблии. Реакция Манту. Функциональные пробы: определение соотношения частоты пульса и дыхания, измерение объема грудной клетки на вдохе и на выдохе, спирография, ЭКГ. ФКГ, определение жизненной емкости легких. Рентгенография органов грудной клетки. Консультация аллерголога, стоматолога, отоларинголога. 3.Во время приступа: 2 агонисты короткого действия (вентолин, сальбутамол- в суточной дозе 400мкг), эуфиллин внутривенно. В дальнейшем ингаляции интала 4 раза в сутки или тайлед 2-4 раза в сутки. В случае недостаточной эффективности в течение 6-8 недель эти препараты необходимо заменить ингаляционными кортикостероидами в среднетерапевтических дозах. Рекомендуемая литература: Основная: 1. Шабалов Н.П. Детские болезни. Изд-е 5-е. В двух томах. Т. 1., Ст.- Пб: Питер, 2006.-829 с. Дополнительная: 1. Бронхиальная астма у детей: диагностика, лечение и профилактика. Москва, 2004. 64 с. 2. Национальная программа «Бронхиальная астма у детей. Стратегия лечения и профилактика» Москва, 2008, 93 с. 3 И.И. Балаболкин «Аллергические болезни у детей», Москва, 2008, 288 с. Занятие № 2. ЛЕЙКОЗЫ У ДЕТЕЙ Цель занятия: изучить клинико - эпидемиологические особенности лейкозов у детей, критерии диагностики; ознакомиться с современными принципами лечения. Вопросы для самоподготовки: 1. Основные отличия в патогенезе острого и хронического лейкозов. 2. Какие изменения регистрируются в анализе крови и лейкоцитарной формуле при остром лейкозе (ОЛ). 3. Какие исследования необходимо провести прежде, чем больному с подозрением на ОЛ будет начата терапия. 4. Какова выживаемость при ОЛ у детей. 5. Каковы современные программы лечения острого лейкоза. Лейкозы (лейкемии) стоят на первом месте по частоте встречаемости онкологических заболеваний у детей и представляют собой группу опухолей, характеризующихся бесконтрольной пролиферацией кроветворных клеток. Традиционно все лейкемии делятся на острые (ОЛ) и хронические (ХЛ). Выделение ОЛ и ХЛ основано ни в коем случае не на течении, а на способности опухолевых клеток дифференцироваться (созревать). Хронический вариант лейкемии диагностируется в случае, когда опухолевая клетка на определенном этапе болезни способна к дифференцировке. Поэтому в гемограмме и миелограмме кроме наличия бластных и зрелых форм практически в равном количестве регистрируются все промежуточные формы (промиелоциты, метамиелоциты, миелоциты и др.). В случае, когда первично мутировавшая гемопоэтическая клетка не способна к дифференцировке, а может лишь воспроизводить саму себя, диагностируется ОЛ. Эти злокачественные клетки, именуемые бластными клетками, постепенно замещают и ингибируют рост и созревание нормальных гемопоэтических предшественников и, благодаря способности к миграции, инфильтрируют различные органы и ткани. В гемограмме и миелограмме при этом наблюдается так называемый "лейкемический провал", т.е. при наличии бластных и единичных зрелых клеток полное отсутствие промежуточных. Таким образом, острый лейкоз у детей – это системное злокачественное заболевание кроветворной ткани, морфологическим субстратом которого являются незрелые атипичные клетки, поражающие костный мозг. Среди острых лейкозов у детей отмечается резкое преобладание случаев острого лимфобластного лейкоза, частота которого, по данным различных авторов, составляет 7585%, миелобластный лейкоз в 15-20%. Установлено, что пик заболеваемости приходится на возраст от 2-х до 5 лет с постепенным уменьшением числа заболевших в возрасте 7 лет и старше. Следующий пик заболевания приходится на возраст 10-13 лет. Мальчики болеют чаще, чем девочки. Частота лейкозов у детей составляет 3,2-4,4 на 100 тыс. Этиология. Лейкоз в настоящее время рассматривается как частная форма опухолевого процесса и возникает по общим законам канцерогенеза. Острый лейкоз является следствием повреждения – мутации в генетическом материале клоногенной кроветворной клетки. В результате этого на молекулярном уровне происходят события, приводящие к нарушению контроля за клеточным циклом, изменению процесса транскрипции и продукции ряда ключевых белков-регуляторов. В качестве основных этиологических факторов в настоящее время рассматриваются несколько факторов: 1. Генетическая предрасположенность и хромосомная нестабильность. Установлено, что нестабильность хромосомного аппарата, имеющая место при ряде врожденных заболеваний, сопровождается повышенным риском развития острых лейкозов (врожденный агранулоцитоз, целиакия, анемия Фанкони, синдром Дауна, синдром Вискотта-Олдрича, Клайнефельтера, нейрофиброматоз Реклингхаузена и др). 2. Вирусы. Роль вирусов в развитии лейкозов доказана в отношении птиц и некоторых животных: в частности, приматов, коров. Причем в качестве этиологических факторов рассматриваются РНК-ретровирусы и ДНК-вирусы. У населения Японии и жителей Карибского бассейна доказано происхождение Т-клеточного лейкоза/лимфомы, вызываемого HTLV-1. Из ДНК-вирусов вирус Эпштейн-Барра участвует в онкогенезе лимфомы Беркита и В-клеточного ОЛЛ и В-клеточных лимфом, ассоциированных с приобретенным иммунодефицитом. 3. Ионизирующая радиация. Доказана связь между частотой встречаемости острого лейкоза и интенсивностью радиационного облучения. В настоящее время установлено, что высокодозная лучевая терапия онкологических больных в 5-10% случаев вызывает вторичные опухолевые заболевания, в том числе острые лейкозы. 4. Химиотерапия. В качестве серьезного этиологического фактора лейкозов в настоящее время рассматривается высокодозная химиотерапия, обладающая, как известно, мутагенным эффектом. К препаратам, относящимся к сильным мутагенам, относятся прокарбазин, хлорбутин, циклофосфамид, ломустин, тенипозид, этопозид. Частота развития вторичных лейкозов у взрослых через 2-10 лет после достижения ремиссии достигает от 5 до 15%. 5. Химические вещества. Бензол при длительном воздействии на организм может оказывать лейкемогенный эффект. Перечисленные факторы в конечном итоге приводят к таким изменениям генома клетки, которые сопровождаются нарушением функции протоонкогенов, генов-супрессоров, образованием онкогенов, что приводит к злокачественной трансформации и преимущественной пролиферации определенного клона гемопоэтических клеток. К середине 70-х годов были получены исчерпывающие доказательства клоновой природы лейкозной инфильтрации, свидетельствующей о том, что в момент клинически выраженной стадии болезни большинство клеток лейкозной опухоли являются потомками одной генетически измененной клетки-предшественницы, являющейся родоначальницей данного клона. На более поздних стадиях лейкозогенеза формируются вторичные опухолевые клоны. Хромосомные нарушения выявляются у 70-80% больных острыми лейкозами. У 20% больных выявляются точечные изменения генома, приводящие к изменению процессов транскрипции. Классификация. В 1976 г была принята франко-американо-британская (FAB) классификация острых лейкозов, пересмотренная и дополненная в 1991 году. Согласно этой классификации на основании морфологических и цитохимических исследований бластных клеток выделяют острый лимфобластный лейкоз трех типов бластных клеток: L1, L2, L3 и нелимфобластный лейкоз, подразделяющийся на несколько типов от М0 до М7 варианта, среди которых наиболее часто встречается М1 и М2, т.е. миелобластный лейкоз. К настоящему моменту FABклассификация во многом утратила свое основополагающее значение в виду создания современных классификаций. Общепринятой является классификация Европейской группы по иммунологическому изучению лейкозов (EGIL-95), согласно которой выделяют 4 основных группы острых лейкозов: 1) Острые лимфобластные лейкозы (ОЛЛ); 2) Острые миелобластные лейкозы (ОМЛ); 3) Бифенотипические лейкозы (БОЛ), содержащие в равной степени как миелоидные, так и лимфоидные маркеры; 4) Недифференцированные острые лейкозы. В 2001 году международной группой экспертов была создана новая классификация гематологических опухолей – классификация ВОЗ, переработанная в 2008 году, основанная на учете цитоморфологических, цитохимических, иммунофенотипических особенностей трансформированных клеток и данных цитогенетического и молекулярно-генетического анализа. FAB-классификация стала ее составной частью. По ВОЗ-классификации острым лейкозом считается заболевание, характеризующееся наличием 25% и более бластных клеток в миелограмме. Причем острые лимфобластные лейкозы согласно ВОЗ-классификации подразделяются на три группы: Острые лимфобластные лейкозы из предшественников В-клеток (цитогенетические подгруппы) t(9;22)(q34;q11); BCR/ABL t (v; 11q23) реаранжировка MLL t(1;19)(q23;p13); E2A/PBX1 t(12;21)(q23;p13); ETV/CBF Острый лимфобластный лейкоз из предшественников Т-клеток Острый лейкоз Бёркита В группе ОЛЛ выделяют методом иммунофенотипирования четыре подтипа Влинейных (Ранний пре-В, Пре-В, Common и В-вариант) и четыре подтипа Т-линейных лейкозов (Про-Т-тип, Пре-Т-тип, кортикальный Т-тип, зрелый Т-ОЛЛ), а также ОЛЛ с экспрессией миелоидных маркеров. Среди иммунологических вариантов ОЛЛ у детей чаще всего встречается Common - 40-45% и Пре-B варианты– 20%, которые являются прогностически наиболее благоприятными. К неблагоприятным в плане прогноза можно отнести ранний преВ (про-В) вариант – 5-10% и Т-линейный лейкоз. ОМЛ в этой классификации подразделяется на четыре категории: ОМЛ с характерными цитогенетическими транслокациями - ОМЛ с t(8;21)(q22;q22), (AML1/ETO) - Острый промиелоцитарный лейкоз (ОМЛ с t(15;17)(q22;q12), (PML/RAR) - ОМЛ с патологической костномозговой эозинофилией (inv(16)(p13q22) или t(16;16)(p13;q22), CBF/MYX11X) - ОМЛ с 11q23 (MLL) дефектами ОМЛ с мультилинейной дисплазией на фоне предшествующего миелодиспластического синдрома, миелопролиферативного заболевания, либо как первичные лейкозы Вторичные ОМЛ, связанный с проводимым ранее лечением: алкилирующими препаратами или облучением ингибиторами топоизомеразы II и другими препаратами ОМЛ, никак более не категоризованные (соответствует FAB-классификации) + Острый базофильный лейкоз Острый панмиелоз с миелофиброзом Миелоидная саркома Клиника. ОЛ начинается не остро, а постепенно, лишь его манифестация является острой. Характер начала заболевания у разных больных вариабелен. И именно в этот период у каждого доктора должна быть онкологическая настороженность. Как правило, ОЛ диагностируется либо при лечении, либо обследовании другой патологии. Лейкоз может протекать некоторое время под маской железодефицитной анемии, интеркуррентного заболевания (ОРЗ, ангина, грипп, пневмония, стоматит), острой дизентерии, брюшного тифа, энтеровирусной инфекции, различного рода лимфаденитов, ревматизма, туберкулеза и это часто служит причиной поздней диагностики. Однако, несмотря на различие масок, каждому врачу важно знать некоторые общие клинические признаки начала ОЛ: - выраженная вялость, слабость, адинамия, снижение аппетита в течение длительного периода; длительный субфебрилитет, особенно в вечернее время, выраженная бледность, нарушение сна, потеря в весе, потеря интереса к играм, интересным занятиям, плохое усвоение школьного материала. Важное значение приобретают нетипичное течение заболевания, не поддающееся традиционной терапии. В клинике ОЛ выделяют, таким образом, по Воробьеву стадию развернутых клинических проявлений, полную ремиссию, выздоровление (состояние полной ремиссии на протяжении 5 лет и более), частичную ремиссию, рецидив с указанием, какой по счету и уточнением очага локализации при локальном рецидиве, терминальная стадия. Критерием диагноза развернутой стадии острого лейкоза считается обнаружение в костном мозге 25% и более бластных клеток. В период манифестации заболевания или развернутой стадии не существует какоголибо клинического признака, который являлся бы патогномоничным для острого лейкоза в целом, и для его отдельных вариантов. Основными клиническими синдромами, встречающимися при ОЛ, являются: интоксикационный, анемический, геморрагический, гиперпластический, болевой. - интоксикационный, имеющий место у большинства больных различными формами ОЛ проявляется головной болью, вялостью, адинамией, лихорадкой или субфебрилитетом особенно в вечернее время, нарушением сна; - анемический, характеризующийся бледностью кожных покровов, вялостью, слабостью, снижением аппетита, болями в животе и сердце; - пролиферативный, характерный более для ОЛЛ и проявляющийся увеличением периферических л/ф узлов в пределах от 1 до 5-6- см, образующих нередко конгломераты, не спаянных между собой, безболезненных при пальпации и также увеличением печени и селезенки у 90% больных ОЛЛ; - геморрагический синдром, характерный более для нелимфобластных лейкозов, особенно для миелобластного и промиелоцитарного лейкоза (66% больных), возникает из-за выраженной тромбоцитопении. Проявляется петехиально-пятнистой сыпью на коже, носовыми, маточными и желудочно-кишечными кровотечениями, гематурией; - костно-суставной синдром, проявляющийся болями (оссалгии) различной интенсивности в костях и суставах (спины, рук, ног, грудины и нижней челюсти), которые могут быть летучими или быть постоянными, носят ноющий, распирающий, колющий, пульсирующий характер, усиливаются в ночное время; - поражение нервной системы (нейролейкоз) в начале заболевания встречается в 5-20% случаев и более характерен для рецидива, что относится и к поражению яичек и яичников, и связано это с тем, что химиотерапевтические препараты в стандартных дозах не проникают через гематоэнцефалический барьер и гематоорхический барьер - поражение кожи и слизистых чаще всего появляется в ходе проведения химиотерапии и очень редко в период манифестации. К атипичным клиническим признакам относятся: двустороннее увеличение в размерах околоушных и слюнных желез (синдром Микулича), увеличение размеров почек, появление лейкемидов (подкожных узелков), явления гингивита (чаще при нелимфобластных лейкозах). В стадии полной ремиссии в пунктате костного мозга находят не более 5% бластных клеток, в периферической крови бластных клеток не должно быть, должен быть нормальным состав спинномозговой жидкости и отсутствовать клинические признаки лейкозной пролиферации. Частичная ремиссия может характеризоваться гематологическим улучшением, уменьшением бластных клеток в костном мозге, спинномозговой жидкости при ликвидации клинических признаков нейролейкоза и подавлении очагов лейкозной инфильтрации в других органах, вне костного мозга. Рецидив ОЛ бывает сверхранним – возникающий в течение 18 мес. от момента постановки диагноза, ранним, возникающий в течение 6 мес. после окончания лечения и поздним – спустя 6 мес. после окончания лечения. Рецидивы бывают также: изолированным: костно-мозговым, ЦНС - рецидив (нейролейкоз), тестикулярный рецидив (в яички) и комбинированным при наличии поражения экстрамедуллярных органов и более 5% бластных клеток в костном мозге. Терминальная стадия подразумевает некурабельный этап опухолевой прогрессии лейкоза. Можно отметить условность этой стадии, поскольку она отражает лишь современный уровень терапевтических возможностей. Диагностика. Наличие такой клинической симптоматики диктует необходимость проведения комплексного гематологического исследования, а именно: 1. Исследование периферической крови. Встречаются два варианта по данным гемограммы: лейкемический, когда бластные клетки выходят в кровь из костного мозга (проявляется обычно выраженным лейкоцитозом более 30 тыс. в общем анализе крови; наличием бластных клеток) и алейкемический – когда бластные клетки не выходят из костного мозга и не обнаруживаются в общем анализе крови (обычно характерна лейкопения). Но для обоих вариантов будет характерно наличие лейкемического провала в лейкоформуле, т.е. отсутствие промежуточных форм, малое количество зрелых форм клеток; чаще всего регистрируется тромбоцитопения, анемия. Следует обращать также внимание на увеличение СОЭ более 20 мм/ч. 2. Исследование пунктата костного мозга. Костно-мозговая пункция проводится из грудины или подвздошной кости. Для постановки диагноза острого лейкоза количество бластных клеток в миелограмме должно быть 25% и более. Однако, даже после постановки диагноза ОЛ лечить ребенка можно только после дальнейшей диагностики. 3. Цитохимическое исследование. Лейкозные клетки, произошедшие из разных клетокпредшественников, отличаются между собой способностью откладывать гликоген, липиды, проявлять активность ферментов – пероксидазы, альфанафтилэстеразы и др. т.е. проводя так называемые цитохимические реакции, мы устанавливаем тип лейкозных клеток и, значит, вариант лейкоза. 4. Иммунофенотипирование. Является обязательным методом в диагностике лейкозов. К задачам иммунофенотипирования как современного метода диагностики можно отнести следующие: 1) подтверждение диагноза; 2) установление варианта ОЛ в том случае, когда цитоморфологический метод не достаточно информативен; 3) определение бифенотипических и билинейных вариантов острых лейкозов; 4) выделение прогностических групп. 5. Цитогенетическое и молекулярно-генетическое исследование для определения количества хромосом и их структурных изменений (транслокация, инверсия, делеция), а также определение ДНК-индекса – цитометрического показателя, отражающего количественные хромосомные аномалии в опухолевых клетках. Цитогенетическое исследование имеет важное значение для определения прогноза заболевания, группы риска развития рецидива, и, следовательно, выбора тактики и интенсивности терапии. Так, наличие филадельфийской хромосомы (Рh-хромосома) у больных с ОЛ в виде транслокации t[9;22] имеет плохой прогноз, выживаемость составляет менее 25-30% у детей. Еще одним известным неблагоприятным фактором является наличие транслокации t[1;19]. Несмотря на интенсивную терапию, выживаемость этих больных составляет около 40%. Транслокация t[4; 11 ] выявляется у 68-81% детей в возрасте до года с помощью молекулярно-биологических методов и является неблагоприятным признаком. ДНК-индекс или плоидию измеряют методом проточной цитофлюориметрии. Гиперплоидия или ДНК-индекс более 50 хромосом в опухолевой клетке встречается у 20% детей старше года независимо от инициального лейкоцитоза и возраста и ассоциируется с хорошим прогнозом. Неблагоприятными прогностическими факторами течения ОЛ являются: возраст менее 1 года, наличие Рh-хромосомы, раннее поражение ЦНС, распространение опухолевого процесса, Т-клеточный вариант ОЛ, Из дополнительных исследований, направленных на выявление степени вовлечения различных органов и систем в патологический процесс проводят: - спинно-мозговую пункцию, которая позволяет выявить поражение центральной нервной системы (нейролейкоз) специфического характера; - рентгенологическое исследование, которое имеет важное значение при наличии болевого синдрома в трубчатых костях, суставах, по ходу позвоночника. - исследование иммунологического статуса ребенка как в момент диагностики ОЛ, так и в процессе проведения противолейкозной терапии и во время ремиссии - биохимическое исследование сыворотки крови осуществляется в динамике болезни на фоне проведения активной противолейкозной терапии, что позволяет вносить своевременно коррективы в лечение при развитии таких состояний, как гиперурикемия, токсикоаллергическое поражение печени, почек и т.д. - исследование свертывающей и противосвертывающей систем крови важно, особенно в период проведения индукционной химиотерапии у больных с НеОЛ; - методы, направленные на контроль за функциональным состоянием кардио-респираторной системы, почек, печени, ЖКТ, эндокринной системы также применяются в различные периоды ОЛ. Диагностика минимальной резидуальной болезни. Минимальной резидуальной (остаточной) болезнью (МОБ, MRD) принято называть популяцию лейкозных клеток, которая на фоне установленной полной клинико-гематологической ремиссии (количество бластных клеток в миелограмме составляет менее 5%) может быть определена только с помощью специальных методов исследования и существенно влияет на развитие рецидива. Лечение больных ОЛ длительное время у детей являлось абсолютно бесперспективным. До 1990 года в нашей стране не было организовано программного лечения. При этом лишь 6,7% детей, больных лейкозом, жили 10 лет и более. Применение современных протоколов лечения острого лейкоза у детей позволило преодолеть 70% барьер 5-летней безрецидивной выживаемости при ОЛЛ у детей, К лучшим протоколам, применяемым в настоящее время, относятся созданный группой BFM (Германия), а также целый ряд американских протоколов. Основа всех этих протоколов заключена в максимальной эрадикации лейкозного клона клеток. Это достигается применением полихимиотерапии, которая является базисным методом терапии заболевания. Главные ее принципы: 1. Использование химиопрепаратов различного механизма действия в адекватных дозах с целью воздействия на определенные фазы клеточного цикла. 2. Концепция риск-адаптированной терапии, согласно которой интенсивность и, следовательно, токсичность терапии должны соответствовать группе риска, т.е. пациенты с прогностически благоприятными исходными характеристиками должны получать минимально токсичную терапию и не подвергаться риску развития тяжелых осложнений, в то время как пациенты с неблагоприятными формами заболевания получают высокоинтенсивную терапию (в том числе и трансплантацию костного мозга), что увеличивает шансы на излечение. 2. Использование высокодозных режимов терапии, а также интенсивная профилактика нейролейкемии. 3. Осуществление сопроводительной терапии, в комплексное понятие которой входит рациональная инфузионная, антибактериальная, микостатическая, симптоматическая терапия и т.д.. 4. Проведение лечения в специализированных детских гематологических стационарах с соблюдением особого санитарно-гигиенического режима (частая смена постельного и нательного белья, отсутствие кондиционеров, цветов в палатах, только жидкое мыло, определенные виды продуктов, игрушек, исключающие проникновение в организм ребенка инфекций, которые при химиотерапии смертельно опасны и т.д.). Существенное значение в лечении ОЛ имеет непрерывность до завершения всей лечебной программы. В большинстве современных протоколов можно выделить три основных этапа терапии: индукция ремиссии, интенсивная постремиссионная терапия и поддерживающая терапия, суммарная длительность которых составляет от 24 до 36 мес. Индукции ремиссии (первичная терапия), которая направлена на уничтожение большей части опухолевых клеток и на достижение полной клинико-гематологической ремиссии. В период индукционной терапии разрушается 90% бластных клеток. В соответствии с результатом индукционной терапии уточняется прогностическая стратификация, пациенты с плохим ранним ответом на терапию переводятся в группу высокого риска, пациенты, не достигшие ремиссии к контрольному сроку, становятся кандидатами на выполнение аллогенной трансплантации вне зависимости от исходных прогностических факторов. По достижении клинико-гематологической ремиссии наступает этап постремиссионной терапии, который в разных протоколах обозначается как интенсификация или реиндукция. За интенсивной фазой терапии следует этап поддерживающей терапии. Залогом успеха поддерживающей терапии является ее непрерывность, что подтверждено рядом исследований, согласно которым выполнение поддерживающей терапии в объеме менее 80% от требуемого (при вынужденных перерывах из-за осложнений или неадекватной дозировки) является неблагоприятным прогностическим фактором для развития рецидива Благодаря современным программам лечения практически решена проблема получения ремиссий: при ОЛЛ у детей - 90-95% полных ремиссий, а при ОНЛЛ в 55-65%. При этом пятилетней безсобытийной (безрецидивной) выживаемости лечения при ОЛЛ по программе ALL-BFM-90-95 - 75-87%, а по программе лечения ОМЛ AML-BFM 87-93 - около 50-65 %. На современном этапе основными проблемами в лечении ОЛ являются увеличение числа пациентов с мутантными клонами опухолевых клеток, резистентными к химиотерапии, поздние побочные эффекты терапии (нарушения роста, нейроэндокринные проблемы, вторые опухоли) и высокая стоимость лечения. Поэтому главной задачей терапии ОЛ является излечение пациента и возвращение его к нормальной социальной жизни и хорошему самочувствию при минимуме побочных эффектов, связанных с лечением. Вопросы для тестового контроля № п/п 1 2 3 4 5 6 7 8 9 Содержание вопросов Вариант острого лейкоза устанавливается на основании: а) клинических данных, б) результата миелограммы, в) цитохимического исследования, г) иммунофенотипирования, д) результата общего анализа крови Понятие острый и хронический лейкоз предусматривает: а) течение заболевания, б) степень тяжести, в) склонность к развитию вторичных опухолей, г) состояние костного мозга, д) наличие геморрагического синдрома В клинике острого лейкоза преобладают следующие клинические синдромы: а) анемический, б) общеинтоксикационный, в) обструктивный, г) пролиферативный, д) геморрагический Диагноз острого лейкоза устанавливается при наличии в миелограмме: а) 10% и более бластных клеток; б) 25% и более бластных клеток; в) тотальном бластозе; г) менее 50% бластных клеток Для лечения острого лейкоза используют: а) циклофосфан, б) 6-меркаптопурин, в) интерферон, г) винкристин, д) миелосан Диагноз острого лейкоза становится несомненным: а) при появлении бластных клеток в гемограмме, б) при гепатоспленомегалии, в) при анемическом и геморрагическом синдроме, г) при наличии 25% и более бластных клеток в миелограмме, д) при угнетении всех ростков кроветворения в костном мозге В России для лечения ОЛ чаще всего применяют следующую программу лечения: а) SIOP, б) BFM, в) PECO Непрерывность лечебной программы при ОЛ соблюдается применением следующих этапов лечения: а) индукция ремиссии; б) трансформация ремиссии; в) консолидация ремиссии; г) интенсификация ремиссии; В общем анализе крови при остром лейкозе может регистрироваться: а) анемия, б) тромбоцитопения, в) лейкоцитоз, г) бластемия, д) все перечисленное Эталоны ответов в, г г а, б, г, д б а, б, г г б а, в, г д 10 По данным гемограммы регистрируется вариант ОЛ: а) лейкемический; б) гипо- а, в пластический; в) алейкемический Ситуационные задачи № п/п 1 Содержание задач Мальчик, 5 лет, поступил в ЦРБ с жалобами на необильные геморрагические высыпания на коже, повышение температуры, плохой аппетит. Со слов родителей мальчик заболел три недели назад, когда стал менее активным, побледнел, однако продолжал посещать детский сад. За 3 дня до поступления в стационар у него повысилась температура до 37,8С и появились геморрагии на коже. В гемограмме: эритроциты – 3,431012/л, гемоглобин – 110 г/л, тромбоциты - 20109/л, лейкоциты – 1,2109/л, метамиелоциты – 1%, палочкоядерные – 4%, сегментоядерные – 3%, лимфоциты – 90%, моноциты – 2%, СОЭ – 34 мм/ч. Учитывая клинико-гематологическое состояние, ребенок был направлен на госпитализацию для дальнейшего обследования и лечения в отделение гематологии. При поступлении состояние ребенка тяжелое, выражены бледность, вялость, недомогание, на коже ног и в области ягодиц петехиально-экхиматозная сыпь. Подкожножировой слой развит умеренно. Лимфатические узлы размерами 11,5 см, безболезненные, эластичные, подвижные. В легких дыхание везикулярное, тоны сердца ясные, на верхушке – систолический шум. Живот слегка вздут, болезнен при пальпации в области печени. Печень пальпируется на 4 см ниже реберной дуги, селезенка – на уровне пупка, плотная. Зев чистый, бледный. Стул и мочеиспускание не нарушены. Анализ крови при поступлении: эритроциты – 2,11012/л, гемоглобин – 67 г/л, тромбоциты – 20109/л, лейкоциты – 11,2109/л, бласты – 49%, сегментоядерные – 5%, лимфоциты – 46%, СОЭ – 62 мм/ч. Миелограмма при поступлении: бласты – 84%, нейтрофильные миелоциты – 0,5%, миелоциты – 1.5%, метамиелоциты – 1,5%, палочкоядерные нейтрофилы – 4%, лимфоциты – 1%, моноциты – 0, плазматические клетки – 1%, ретикулярные клетки – 3%, нормоциты базофильные – 1%, нормоциты полихроматофильные – 2%, нормоциты оксифильные – 0,5%. Мегакариоциты не обнаружены. Цитохимические реакции показали, что бластные клетки дают отрицательную реакцию на миелопероксидазу и липиды, и положительную на гликоген. Вопросы: 1.Поставить диагноз, дать ему Эталоны ответов 1. Острый лимфобластный лейкоз, период развернутых клинических проявлений, лейкемический вариант. Диагноз поставлен на основании: анамнеза заболевания; характерных клинических проявлений (выраженный интоксикационный синдром; геморрагический синдром в виде петехиально-экхиматозной сыпи на коже ног и ягодиц; пролиферативный синдром, проявляющийся увеличением печени до 4см, селезенки до уровня пупка); данных гемограммы: снижение гемоглобина, эритроцитов, тромбоцитопения, ускорение СОЭ; лейкемический вариант – на основании лейкоцитоза и бластемии; результата миелограммы: количество бластных клеток в костном мозге больше 30%; цитохимических реакций - отрицательная реакция бластных клеток на миелопероксидазу и липиды свидетельствует о лимфобластном характере лейкоза. 2. В плане обследования необходимо провести дополнительно комплекс лабораторноинструментальных методов обследования для определения состояния внутренних органов и систем организма перед началом терапии: биохимические показатели крови, анализы мочевого осадка, функциональные пробы почек, печени, ЭКГ, ЭХО-КГ, УЗИ органов брюшной полости и почек, рентгенографию грудной клетки. Ребенку показана терапия по протоколу ALL-BFM-90, принятая в России. Она включает в себя интенсивную химиотерапию в течение ½ года, которая состоит из следующих протоколов: индукция ремиссии, консолидация ремиссии, интенсификация ремиссии. При этом применяются следующие препараты: глюкокортикоиды (преднизолон, дексаметазон), алкалоиды (винбластин, винкристин), антиметаболиты (метотрексат, 6меркаптопурин, цитозар), алкилирующие соединения (циклофосфан), ферментные препараты (L-аспарагиназа), антрациклиновые антибиотики (рубомицин, доксорубицин). Согласно программе интенсивная химиотерапия проводится одновременно с сопроводительным лечением (обще-гигиенические мероприятия, инфузионная терапия, профилактика инфекционных осложнений, вторичных токсических поражений внутренних органов, мукозитов, дерматитов, противорвотная терапия). Спустя две недели после окончания интенсивной терапии и сохранении ремиссии переходят на поддерживающую терапию еще в течение 1,5 лет. 2 обоснование. 2.Составить план дальнейшего обследования и лечения. Ирина Л., 14 лет. Находилась в клинике повторно, была выписана в стадии полной ремиссии острого миелобластного лейкоза на поддерживающей терапии преднизолоном и 6-меркаптопурином. Стал развиваться побочный синдром Иценко-Кушинга, в связи с чем девочка через три месяца после начала поддерживающей терапии прекратила принимать препараты. Через месяц после отмены химиопрепаратов в тяжелом состоянии была доставлена в отделение гематологии. При поступлении отмечена слабость, резкая бледность, головокружение, над верхушкой сердца выраженный систолический шум, тахикардия, геморрагии на коже, маточное кровотечение; печень пальпировалась у края реберной дуги, селезенка на 6 см ниже; заметный синдром Кушинга; некротическая ангина. Анализ крови: гемоглобин – 50 г/л; эритроциты – 1,71012 ; цветовой показатель – 0,99; ретикулоциты – 8% ; тромбоциты – 20 тыс; лейкоциты - 88109 /л; миелобласты – 84%; миелоциты – 1%; метамиелоциты – 1%; палочкоядерные – 11%; сегментоядерные – 3%; лимфоциты – 0; СОЭ – 50 мм/ч. Миелограмма: миелобласты – 98%; ретикулярные клетки. Ликвор – без патологии. Вопросы: 1.Поставьте диагноз, дайте ему обоснование. 2.Какова дальнейшая тактика 1. Рецидив I (ранний) миелобластного лейкоза. Диагноз установлен на основании: А) данных анамнеза – самостоятельно отменена поддерживающая терапия; Б) клинических проявлений – интоксикационного синдрома (слабость, головокружение); геморрагического синдрома (геморрагии на коже, маточное кровотечение); пролиферативного синдрома (увеличение селезенки на 6 см) ; некротической ангины. В) Анализа крови: снижения гемоглобина, эритроцитов, тромбоцитов, выраженного лейкоцитоза - 88109 /л; бластемии, повышения СОЭ до 50 мм/ч. Г) Данных миелограммы: миелобласты – 98%; Д) Ранним рецидив называется в том случае, если он возникает в течение 6 месяцев после окончания химиотерапии. 2. С момента установления диагноза необходимо начало сверхинтенсивного химиотерапевтического лечения (Rez I), предусматривающего проведение терапии блоками. Рекомендуемая литература: Основная: 1. Шабалов Н.П. Детские болезни. Изд-е 5-е. В двух томах. Т. 2., Ст.-Пб: Питер, 2006.-731 с. . Дополнительная: 1. Детская онкология. //Под редакцией М.Б. Белогуровой. Санкт-Петербург, "СпецЛит", 2002г. 2. Руководство по детской онкологии. //Под редакцией академика Л.А.Дурова. Москва, «Милош», 2003г. Занятие № 3. РЕВМАТИЗМ, ПРИОБРЕТЕННЫЕ ПОРОКИ СЕРДЦА Цель занятия: изучить современные взгляды на этиопатогенез и диагностику ревматизма, рассмотреть особенности клиники заболевания в детском возрасте, усвоить алгоритм лечения и профилактики ревматизма; обучить студентов основным принципам диагностики приобретенных пороков сердца у детей. Вопросы для самоподготовки: 1. Современные представления об этиологии и патогенезе ревматизма. 2. Классификация ревматизма. Диагностические критерии Киселя-Джонса. 3. Особенности течения ревмокардита и внесердечных изменений при ревматизме в детском возрасте. 4. Современные подходы к лечению ревматизма. Первичная и вторичная профилактика. 5. Дифференциальный диагноз ревматизма с другими заболеваниями. 6. Клинико-инструментальная характеристика недостаточности и стеноза митрального клапана у детей. 7. Аортальные пороки сердца: особенности клинической картины и диагностики. Ревматизм или острая ревматическая лихорадка - системное воспалительное заболевание соединительной ткани с преимущественной локализацией процесса в сердечно-сосудистой системе, развивающееся в связи с острой стрептококковой инфекцией у предрасположенных к нему лиц, главным образом в возрасте 7-15 лет. Ревматизм не является массовым заболеванием, но представляет серьезную проблему в связи с нередким формированием пороков сердца. В последние годы в силу ряда негативных социально-экономических процессов и снижения чувствительности стрептококков к пенициллинам, отмечена тенденция к нарастанию заболеваемости ревматизмом у детей. Этиопатогенез. Развитие ревматизма тесно связано с предшествующей инфекцией βгемолитическим стрептококком группы А. В патогенезе болезни имеет значение повреждающее действие компонентов стрептококка (особенно М-протеина, входящего в состав клеточной стенки вирулентных штаммов стрептококка) и его токсинов на организм, а также воздействие противострептококковых антител - антистрептолизина 0 (АСЛ-0), антистрептогиалуронидазы (АСГ), антидезоксирибонуклеазы, перекрестно реагирующих с тканями сердца с развитием иммунного воспаления. Роль генетических факторов в развитии болезни подтверждается ассоциацией ревматизма с определенными группами крови и некоторыми антигенами системы гистосовместимости HLA (Dr5-Dr7, Cw2-Cw3, D8/17), а также более частой заболеваемостью детей из семей, в которых кто-то из родителей или сибсов страдает ревматизмом. Морфологические изменения представлены специфическими некротическипролиферативными реакциями (гранулемы Ашоффа-Талалаева) и неспецифическими экссудативными проявлениями, которые более отчетливы в детском возрасте, что определяет большую остроту и активность процесса. Клиника. В последние годы ревматизм у детей характеризуется преобладанием стертых и латентных форм. Как правило, он возникает в школьном возрасте и практически не встречается у детей младше 3 лет. В типичных случаях первые признаки болезни выявляются через 2-3 недели после перенесенной ангины или скарлатины в виде лихорадки, симптомов интоксикации, суставного синдрома, кардита и др. Возможно малосимптомное начало заболевания с появлением утомляемости и субфебрилитета. Одним из наиболее ранних признаков ревматизма является суставной синдром (артрит или артралгии), который имеет место у 80% детей, характеризуется острым началом, вовлечением крупных или средних суставов (коленных, голеностопных, локтевых) чаще в виде моно- или олигоартрита, доброкачественностью поражения (не оставляет деформаций) и быстрым обратным развитием процесса (при адекватной терапии – в течение нескольких дней или часов). Суставной синдром обычно сочетается с поражением сердечно-сосудистой и нервной систем. Поражение сердца (кардит) определяется у большинства детей уже в дебюте заболевания, а при повторных атаках его частота увеличивается. При этом дети чаще предъявляют жалобы астенического характера (на недомогание, повышенную утомляемость, слабость, раздражительность) и лишь при выраженных сердечных нарушениях могут жаловаться на боли в области сердца, сердцебиение, одышку. Объективными признаками ревмокардита являются изменение частоты сердечных сокращений (тахи- или брадикардия), увеличение размеров сердца, преимущественно влево, приглушение сердечных тонов (особенно I), появление систолического шума с максимумом на верхушке и в точке Боткина. Причем, при изолированном поражении миокарда шум, как правило, слабый или умеренный, редко проводится за пределы сердца, а при эндокардите, с характерным для ревматизма поражением митрального клапана, шум дующий, продолжительный, связанный с ослабленным I тоном, усиливается на левом боку и проводится в левую подмышечную область. Именно вальвулиту митрального клапана отводится основная роль в формировании пороков сердца, развитие которых может быть установлено не ранее, чем через 6 месяцев от начала болезни. Гораздо реже наблюдается развитие вальвулита аортального клапана, проявляющегося связанным со II тоном протодиастолическим шумом по левому краю грудины. Ревмокардит, особенно при вовлечении в процесс перикарда, может осложняться развитием застойной сердечной недостаточности. На ЭКГ при ревмокардите выявляются синусовая тахи- или брадиаритмия, миграция водителя ритма, замедление атриовентрикулярной проводимости (до блокады I степени), нарушения реполяризации, удли- нение электрической систолы, реже определяются гетеротопные аритмии (экстрасистолия). При вальвулите митрального клапана на ЭКГ могут определяться признаки острой перегрузки левого предсердия, а при вальвулите аортального клапана – диастолической перегрузки левого желудочка. Основным методом инструментальной диагностики ревмокардита является эхокардиография (ЭхоКГ), которая выявляет утолщение, «лохматость», «рыхлость» створок пораженных клапанов, ограничение их подвижности, нарушение сократительной функции миокарда, дилатацию полостей сердца (чаще левых). Возможно наличие перикардиального выпота. Рентгенологически также могут определяться признаки увеличения сердца, при вальвулите митрального клапана нередко определяется митральная, а при поражении аортального клапана - аортальная конфигурация сердца. Прогноз. В настоящее время при своевременно начатом лечении первичный ревмокардит у большинства детей заканчивается выздоровлением. Формирование клапанных пороков сердца при первой атаке происходит в 15-20% случаев преимущественно при тяжелом и затяжном течении заболевания. При повторных атаках частота формирования пороков сердца достигает 80-100%. Для детского ревматизма характерна малая хорея, встречающаяся преимущественно у девочек пубертатного возраста и проявляющаяся гиперкинезами, гипер- или гипорефлексией, мышечная гипотонией, нарушением координации движений, изменением психики ребенка и разнообразными вегетативными расстройствами. Начинается хорея постепенно. Появляется эмоциональная лабильность, раздражительность, плаксивость, рассеянность, снижение памяти, ухудшение успеваемости. Объективно выявляются непроизвольные подергивания мышц лица и конечностей с гримасничаньем, порывистыми, неловкими движениями, невнятная, нечеткая речь, изменение почерка, походки. Гиперкинезы чаще носят двусторонний характер, усиливаются при волнении, ослабевают или исчезают во время сна. Хорея нередко предшествует развитию кардита или протекает без сердечных нарушений. К редким симптомам ревматизма, определяющимся при высокой активности процесса, относятся аннулярная сыпь (нестойкая бледно-розовая кольцевидная эритема, появляющаяся в дебюте болезни, не возвышающаяся над поверхностью кожи и исчезающая при надавливании) и ревматические узелки (округлые, плотные, малоподвижные, безболезненные образования, локализующиеся в области суставов, остистых отростков позвонков, сухожилий и возникающие, как правило, при затяжном течении ревматизма). Поражение легких, почек и других органов при современном течении ревматизма практически не встречается.Диагностика. В активную фазу определяются лейкоцитоз со сдвигом влево, ускорение СОЭ, нередко анемия, диспротеинемия с гипергаммаглобулинемией, повышение уровня серомукоида, ДФА, С-реактивный белок (СРБ), антистрептококковые антитела. Однако специфических тестов для диагностики ревматизма нет. По рекомендациям ВОЗ (1992) на практике до настоящего времени используют, критерии А.А. Киселя (1940) и Джонса (1944), пересмотренные Американской Кардиологической Ассоциацией в 1992 году. Диагностические критерии острой ревматической лихорадки БОЛЬШИЕ ПОЛИАРТРИТ КАРДИТ ХОРЕЯ КОЛЬЦЕВИДНАЯ ЭРИТЕМА РЕВМАТИЧЕСКИЕ УЗЕЛКИ МАЛЫЕ КЛИНИЧЕСКИЕ Артралгии, лихорадка ЛАБОРАТОРНЫЕ Повышенные острофазовые реактанты: СОЭ, СРБ УДЛИНЕНИЕ ИНТЕРВАЛА PR на ЭКГ Данные, подтверждающие предшествовавшую стрептококковую инфекцию: Позитивная А-стрептококковая культура, выделенная из зева, или положительный тест быстрого определения стрептококкового антигена Повышенные (повышающиеся) титры противострептококковых антител Обнаружение 2 больших или 1 большого и 2 малых критериев в сочетании с данными, подтверждающими предшествующую стрептококковую инфекцию, свидетельствует о высокой вероятности ревматизма. Однако окончательный диагноз часто устанавливают лишь в ходе динамического наблюдения за больным. Классификация ревматизма, разработанная А.И. Нестеровым, по настоящее время используется для формулировки диагноза (таблица 6). Таблица 6 Классификация и номенклатура ревматизма Фаза болезни Активная активность I, II, III степени Неактивная Клинико-анатомическая характеристика поражения Характер течения сердца других органов и систем Ревмокардит Полиартрит, полиартралгии, серопервичный зиты (плеврит, перитонит, абдобез порока сердца минальный синдром Ревматизм возвратный с Хорея, энцефалит, менингопороком сердца энцефалит, церебральный васкулит Ревматизм без явных Васкулиты, нефрит, гепатит, сердечных изменений пневмонии, поражение кожи (анулярная сыпь, ревматоидные узелки), иридоциклит, тиреоидит Миокардиосклероз рев- Последствия и остаточные явления матический перенесенных внесердечных изменений Порок сердца (какой) Острое, подострое затяжновялое непрерывнорецидивирующее латентное Состояние кровообращения НК0 HК I НК IIА НК IIБ НК III Острое течение отражает быстрое развитие ревматизма, полисиндромность, яркие клинико-лабораторные проявления (продолжительность заболевания - 2-3 мес.). Подострое течение характеризуется более медленным развитием клинических симптомов, менее выраженными лабораторными проявлениями (длительность - 3-6 мес.). Затяжное течение отличается умеренными признаками активности, торпидностью к проводимой терапии (продолжительность - более 6 мес.). При рецидивирующем течении отмечаются полисиндромность, тяжесть клинических проявлений, рецидивы. Для латентного течения характерно обнаружение порока сердца при отсутствии признаков активности процесса и ревматического анамнеза. За последние 20-30 лет клиническая картина острой ревматической лихорадки претерпела существенные изменения, что обусловило необходимость создания новой классификации, в основу которой положены синдромы, характеризующие диагностические критерии ревматизма (таблица 7). Таблица 7 Классификация ревматической лихорадки (АРР, 2003) Клинические варианты Клинические проявления Основные Дополнительные Острая ревма- Кардит Лихорадка тическая лихо- Артрит Артралгии радка Хорея АбдоминальПовторная рев- Кольцевидный синдром матическая ная эритема Серозиты лихорадка Ревматические узелки Исход Стадия НК по Стражеско- По NYHA Василенко Выздоровление 0 0 Хроническая рев- I I матическая болезнь IIА II сердца IIБ III без порока сердца III IV порок сердца Дифференциальный диагноз ревматизма проводится с большой группой состояний и болезней, протекающих с суставным синдромом (реактивные артриты, ювенильный ревматоидный артрит, болезнь Лайма, лейкоз, неопластические процессы); с целым рядом воспалительных кардиологических заболеваний (неревматический кардит, инфекционный эндокардит); врожденных и приобретенных нарушений структуры сердца (пролапс митрального клапана, врожденная недостаточность митрального клапана или аномалия его развития); синдромом вегетативной дистонии. Диагноз малой хореи требует прежде всего исключения функциональных тиков и системной красной волчанки. Лечение ревматизма у детей осуществляют по принципу этапности: 1-й этап - стационар, 2-й этап - долечивание в местном кардио - ревматологическом санатории, 3-й этап – диспансерное наблюдение в поликлинике. В стационаре больному назначают постельный режим, длительность которого определяется, прежде всего, тяжестью кардита. Режим постепенно расширяют (по результатам пробы Шалкова). В диете ограничивают облигатные аллергены, соль и жидкость (при наличии признаков СН). Этиотропную терапию проводят пенициллином (50-100 тыс. ЕД/кг/сут в/м в 4-6 введений) в течение 14 дней. При наличии хронического тонзиллита или других очагов хронической инфекции, а также в случае непереносимости пенициллинов используют цефалоспорины (цефуроксим, цефотаксим), макролиды (спирамицин, азитромицин, кларитромицин) или линкозамины (линкомицин). Из нестероидных противовоспалительных препаратов (НПВП) предпочтение отдают ацетилсалициловой кислоте (0,2 г на г.ж./сут) и диклофенаку (2-3 мг/кг/сут), которые применяют не менее 1,5 месяцев. При умеренной и высокой активности процесса, остром или подостром кардите, полиартрите, хорее назначают глюкокортикостероиды (ГКС) - преднизолон в дозе 0,6-0,8 мг/кг/сут до получения клинического эффекта, затем дозу снижают на 5-2,5 мг каждые 5-7 дней. При затяжном и рецидивирующем течении ревматизма используют хинолиновые препараты, которые применяют длительно. В комплексной терапии используют препараты калия, витамины С и группы В, антигистаминные, антиаритмические средства, препараты для лечения сердечной недостаточности (гликозиды, диуретики, ингибиторы АПФ). В санатории продолжают начатую терапию, санируют очаги хронической инфекции, осуществляют соответствующий лечебно-оздоровительный режим с дифференцированной двигательной активностью, лечебной физкультурой. Третий этап комплексной терапии ревматизма предусматривает профилактику его рецидивов и прогрессирования на поликлиническом этапе. Профилактика ревматизма подразделяется на первичную и вторичную. Первичная профилактика направлена на предупреждение ревматизма и включает: повышение иммунитета и оздоровление детей (закаливание, чередование нагрузки и отдыха, полноценное питание и т.д.), выявление и лечение острой и хронической стрептококковой инфекции, профилактические мероприятия у предрасположенных к развитию ревматизма детей (из семей, в которых имеются случаи ревматизма или других ревматических заболеваний; часто болеющих носоглоточной инфекцией; имеющих хронический тонзиллит или перенесших острую стрептококковую инфекцию). Вторичная профилактика направлена на предупреждение рецидивов и прогрессирования ревматизма. С этой целью используют бензатин бензилпенициллин (экстенциллин или ретарпен), который назначают 1 раз в 3 недели круглогодично в дозе 2,4 млн. ЕД - детям старше 12 лет; 1,2 млн. ЕД – детям с массой тела более 27 кг, 600000 ЕД – детям с массой тела менее 27 кг. Пациентам, перенесшим ревматическую лихорадку без кардита, вторичную профилактику проводят 5 лет после последней атаки или до 18-летнего возраста (по принципу «что дольше»), после ревмокардита без порока сердца – 10 лет после последней атаки или до 25-летнего возраста (по принципу «что дольше»), с формированием порока сердца – пожизненно. В весенне-осенний период наряду с введением бензатин бензилпенициллина показано проведение профилактики НПВП в течение месяца. Приобретенные пороки сердца Недостаточность митрального клапана - наиболее частый ревматический порок сердца. Характеризуется уменьшением звучности первого тона на верхушке и наличием дующего продолжительного (занимает 2/3 систолы) жесткого систолического шума, который выслушивается в любом положении, усиливается при физической нагрузке и проводится за пределы сердца. Отмечается акцент II тона на легочной артерии. На ЭКГ выявляются признаки гипертрофии левого желудочка и в меньшей степени левого предсердия. На ФКГ записывается высокоамплитудный, высокочастотный систолический шум на верхушке, убывающий или лентовидный, тесно связанный с I тоном. При проведении ЭхоКГ выявляется увеличение размеров левого желудочка (ЛЖ) и левого предсердия (ЛП), увеличение амплитуды пульсации межжелудочковой перегородки, разнона- правленное диастолическое движение створок МК. Рентгенологически определяются признаки венозного застоя, увеличение ЛП и ЛЖ, выбухание дуги легочной артерии, сглаженность сердечной талии - “митральная конфигурация”. Митральный стеноз, как изолированное поражение сердца, встречается у детей редко (при вялом или латентном течении Р). Появляются жалобы на одышку и сердцебиение, цианотичный румянец. При аускультации выслушивается хлопающий I тон, рокочущий пресистолический шум, митральный щелчок, акцент и расщепление II тона на легочной артерии, пальпаторно нередко определяется “кошачье мурлыканье”. На ЭКГ определяется гипертрофия ЛП, позднее - правых отделов сердца. На ФКГ фиксируется увеличение амплитуды I тона, увеличение интервала Q-I тон выше 0,06 мс и тон открытия МК. При ЭхоКГ определяется уменьшение амплитуды движения передней створки МК, повышенная эхогенность и однонаправленное диастолическое движение створок, вследствие их сращения по комиссурам, увеличение размеров ЛП и правого желудочка, Рентгенологически также выявляется увеличение левого предсердия и правого желудочка, признаки застоя в малом круге. Значительно чаще стенозирование МК происходит на фоне уже сформированной его недостаточности. В этом случае симптоматика складывается из признаков того и другого порока. Недостаточность аортального клапана определяется по наличию льющегося диастолического шума, выслушиваемому по левому краю грудины. Характерны бледность, снижение диастолического и повышение пульсового давления. Периферические симптомы (“пляска каротид”, капиллярный пульс, Синдром Мюссе, Ландольфи, двойной тон Траубе и шум Дюрозье) у детей появляются редко. На ЭКГ порок проявляется признаками гипертрофии и перегрузки ЛЖ с отклонением электрической оси сердца влево, на ФКГ - лентовидным диастолическим шумом, следующим сразу за II тоном. ЭхоКГ выявляет расхождение аортальных створок в диастоле, увеличение размеров ЛЖ и ЛП. Рентгенологически определяется аортальная конфигурация сердца с явными признаками гипертрофии ЛЖ. Стеноз устья аорты как приобретенный порок чаще всего присоединяется к аортальной недостаточности. Во 2 межреберье справа появляется грубый систолический шум, который хорошо проводится на сосуды шеи. ЭКГ выявляет гипертрофию ЛЖ, ЭхоКГ – уменьшение систолического расхождения створок аортального клапана. Рентгенологически сердце приобретает форму “сапожка”. Вопросы для тестового контроля № п/п 1 2 3 4 5 6 7 Содержание вопросов К основным диагностическим критериям ревматизма не относится: а) кардит, б) полиартралгия, в) кольцевидная эритема, г) увеличение лимфатических узлов, д) ревматические узелки Типичные аускультативные признаки первичного ревмокардита все вышеперечисленные, кроме: а) приглушенность тонов, б) тахикардия в) брадикардия, г) экстрасистолия, д) систолический шум относительной недостаточности митрального клапана При первичной атаке ревматизма порок сердца формируется в: а)100%, б) 7080%, в) 50-60 % г) 15-20% д) 5% Длительность постельного режима у ребенка с ревматизмом определяется: а) возрастом ребенка, б) выраженностью недостаточности кровообращения, в) тяжестью кардита, г) наличием порока сердца, д) характером лечения (получает ли ГКС) При малой хорее показаны: а) делагил, б) ибупрофен, в) препараты брома, транквилизаторы, г) нейролептики, д) преднизолон Не характерным для малой хореи является: а) развитие у девочек пубертатного периода, б) развитие у мальчиков пубертатного периода, в) гиперкинезы, г) мышечная гипотония, д) нарушение поведения Вторичная профилактика ревматизма проводится: а) НПВС в течение месяца весной и осенью, б) экстенциллином круглогодично, в) бициллином-5 весной и Эталоны ответов б г г б, в в, д б а, б 8 9 10 осенью, г) бициллином-5 круглогодично, д) глюкокортикоидами весной и осенью Малые диагностические критерии ревматизма: а) артралгии, б) лихорадка, в) а, б, в, д острофазовые воспалительные лабораторные сдвиги, г) изменение сегмента SТ на ЭКГ, д) удлинение интервала РQ на ЭКГ Для ревмокардита типичны: а) жалобы астенического характера, б) изменение а, б, в, д частоты сердечных сокращений (тахи- или брадикардия), в) расширение границ сердечной тупости, преимущественно влево, г) гетеротопные аритмии, д) систолический шум с максимумом на верхушке и в точке Боткина Для митрального стеноза типичны: а) грубый диастолический шум на верхуш- а, в, д ке, б) грубый систолический шум на верхушке, в) пресистолическое дрожание (“кошачье мурлыканье”) г) ослабление 1 тона на верхушке, д) акцент 1 тона на верхушке (“хлопающий” 1 тон) Ситуационные задачи № 1. Содержание задач Девочка 11 лет поступила в стационар с жалобами на повышение температуры тела до 38,7С в течение пяти дней, боли в коленных суставах, кольцевидную сыпь на груди и животе. Со слов родителей суставы опухали и были горячими на ощупь. Три недели тому назад перенесла фолликулярную ангину (семь дней получала ампициллин). Ежегодно болела (2-3 раза) ОРВИ, отмечены явления аденоидита. У бабушки по материнской линии - митральный порок сердца. Объективно: кожа бледная, на груди и животе - нестойкая, розового цвета сыпь в форме колец и полуколец, которая усиливается под воздействием тепла и не сопровождается зудом. Коленные суставы симметрично припухшие, болезненные в покое и при движении. Движения в них сохранены в полном объеме. В легких везикулярное дыхание, ЧД-18/мин. Границы сердца: верхняя - III ребро, правая - на 1 см кнаружи от правой стернальной линии, левая на 1 см кнаружи от левой срединноключичной линии. Тоны сердца приглушены, особенно I тон на верхушке, здесь же выслушивается мягкий, непродолжительный систолический шум, не проводящийся за пределы сердца шум. ЧСС - 90 уд/мин, АД- 90/50 мм рт.ст. Живот мягкий, безболезненный. Печень и селезенка не пальпируются. Анализ крови: эритр.- 4,45 млн, гемоглобин125 г/л, лейк.-20 000 (п-6%, с-60%, лф-20%, м12%, базофилы-2%), СОЭ-46 мм/час, СРБ++++, сиаловые кислоты-300 ед, АСО-750ед., -глобулины-27%. ЭКГ: нарушение процессов реполяризации в миокарде, удлинение интервала РQ, незначительное замедление электрической систолы. Вопросы: 1.Ваш диагноз. 2.Оцените активность процесса. 3.Какова схема лечения? Таня И., 9 лет, обратилась к врачу с жалобами на утомляемость, раздражительность, плаксивость. Мать отмечает, что в последние 2 недели девочка стала неряшливо писать, гримасничать, излишне двигаться на уроках, снизилась успеваемость в школе. За месяц до появления указанных симптомов перенесла скарлатину, антибиотиками не лечилась. При объективном обследовании: де- Эталоны ответов 1.Ревматизм I, активная фаза, III ст. активности. Ревмокардит. Полиартрит. Анулярная сыпь. Острое течение. 2.Диагноз ревматизма поставлен с учетом отягощенного анамнеза, наличия кардита (расширение границ сердца, приглушение I тона, систолический шум на верхушке, ЭКГ), полиартрита (симметричное поражение крупных суставов, мигрирующий характер болей и признаки воспаления), характерной анулярной сыпи. Подтверждает диагноз связь заболевания со стрептококковой инфекцией. В пользу III ст. активности свидетельствуют преобладание экссудативного компонента воспаления (расширение границ сердца, анулярная сыпь, полисерозит); лейкоцитоз (20 0000), СОЭ более 40 мм/час; уровень глобулинов более 25%, увеличение титра АСО в 3 раза 3.Лечение. Режим постельный. Ограничение поваренной соли до 4-5 г/сут, жидкости (не более 1 л/сут.). Диета должна включать липотропные вещества, кальций и калий (творог, овес, молоко, курага, чернослив, картофель, капуста). Пенициллин назначают в дозе 50 000 ЕД/кг/сут 10 дней, затем экстенциллин в дозе 1200000 ЕД 1 раз в 3 недели. С учетом III ст. активности должен быть назначен преднизолон в дозе 0,7 мг/кг/сут в течение 3-4 недель. Диклофенак натрия – 2-3 мг/кг/сут. Для улучшения метаболизма миокарда – препараты калия, кокарбоксилаза, витамины группы В, фолиевая кислота, пантотенат кальция. 1. Ревматизм I, активная фаза, III степени активности, без явных сердечных изменений: малая хорея, острое течение. НК0-1. Хронический тонзиллит. Диагноз выставлен на основании характерных симптомов поражения нервной системы (гиперкинезы, нарушение координации движений, эмоциональная лабильность), возникших в связи со стрептококковой инфекцией. Наличие хореи 2. вочка бледная, «тени под глазами». Гипертрофия миндалин II степени. Подчелюстные лимфатические узлы увеличены до 1,5 см, подвижны. Гиперкинезы конечностей. Речь невнятна, скандирована, «проглатывает» слоги. Изменены координационные пробы. В легких дыхание везикулярное, ЧД - 20 в минуту. Границы относительной сердечной тупости возрастные. Тоны ясные, ритмичные ЧСС - 92 уд/мин, ритмичный; АД – 100/60 мм. рт. ст. Печень не пальпируется. Стул, диурез в норме. Общий анализ крови: эр.- 3,9х1012/л, Нb - 110 г/л, лейк.- 11,3х109/л, э - 2%, п - 3%, с- 67%, л - 22%, м - 6%. СОЭ - 3 мм/ч. Общий белок - 81,4 г/л, альб. - 46,4%, глобулины 53.6%: α1 - 7,9%, α2 -12,6%, β-13,2%, γ-19,9%. СРБ-++, фибриноген - 3,5 г/л, серомукоид - 0,44 ед. ЭКГ – синусовый ритм, нормальное положение ЭОС. Вопросы: 1. Поставить и обосновать диагноз. 2. Наметить принципы лечения больного 3. Дать план профилактических мероприятий. подразумевает III степень активности болезни, независимо от выраженности лабораторных признаков. 2. В стационаре постельный режим, стол 10. Антибиотики (бензилпенициллин 1014 дней, затем макролиды), преднизолон (0,5-0,7 мг/кг/сут 14 дней с постепенным снижением дозы, десенсибилизирующая терапия (препараты кальция, антигистаминные). Витамины С, В1 и В6, транквилизаторы (седуксен, мепротан), седативные (препараты брома, валериана). 3. Круглогодичная вторичная профилактика экстенциллином в дозе 1200000 ЕД 1 раз в 3 недели в течение 5 лет, сезонное применение салицилатов, санация очагов инфекции. Рекомендуемая литература: Основная: 1. Кардиология и ревматология детского возраста. Под ред. Самсыгиной Г.А., Щербаковой М.Ю. В книге «Практическое руководство по детским болезням» Под общей редакцией Коколиной В.Ф. и Румянцева А.Г. Т.III. М.: ИД Медпрактика-М, 2004, 744 С. 2.Н.А. Белоконь, М.Б. Кубергер Болезни сердца и сосудов у детей. В двух томах М.: Медицина, 1987.- Т.1.- С.353-391. Дополнительная: 1. Детская ревматология. Руководство для врачей. //Под редакцией А.А.Баранова и Л.К.Баженовой. М.: Медицина, 2002.-336 с. 2. Насонова В.А., Астапенко М.Г. Клиническая ревматология: руководство для врачей / АМН СССР.-М.: Медицина, 1989.-592 с. Занятие № 4. ЮВЕНИЛЬНЫЙ РЕВМАТОИДНЫЙ АРТРИТ Цель занятия: изучить современные представления об особенностях этиопатогенеза, клиники, диагностики и лечения ювенильного ревматоидного артрита (ЮРА) у детей. Вопросы для самоподготовки: 1. Современная терминология ЮРА, теории этиопатогенеза, принципы классификации. 2. Характеристика суставного синдрома при ревматоидном артрите у детей. 3. Суставно-висцеральные формы ЮРА (вариант с ограниченными висцеритами, аллергосептический вариант, субсепсис Висслера-Фанкони). 4. Лабораторные рентгенологические признаки ревматоидного артрита в детском возрасте. Критерии диагностики ЮРА. 5. Дифференциальный диагноз ЮРА. 6. Современные подходы к лечению ЮРА. Место базисных препаратов, стероидных и нестероидных противовоспалительных средств в медикаментозной терапии ЮРА. В основе современных взглядов на диагностику ювенильного ревматоидного артрита лежит принцип исключения всех остальных заболеваний ревматологического профиля. Между тем, в первые месяцы болезни это весьма затруднительно, в связи с чем, зарубежные специалисты предлагают использовать для обозначения любого артрита, начавшегося до 16 летнего возраста и продолжающегося более 6 недель термин «ювенильный хронический» (ЮХА) или «ювенильный идиопатический артрит» (ЮИА). Отечественные педиатры используют как термин ЮРА, так и ЮХА, подразумевая, что диагноз ЮХА является динамическим и объединяет достаточно разнородные артриты, которые, тем не менее, имеют и ряд общих черт (энтезопатии, серонегативность, связь дебюта болезни с кишечными или урогенитальными инфекциями и др.). Части из этих артритов свойственно доброкачественное течение и лишь часть может впоследствии трансформироваться в ЮРА или другие ДБСТ, например, в болезнь Бехтерева. Диагноз «ювенильный ревматоидный артрит» (ЮРА) в ходе динамического наблюдения выставляется при условии: 1) прогрессирования заболевания с генерализацией суставного синдрома или вовлечением в процесс внутренних органов; 2) наличия и прогрессирования костно-суставной деструкции; 3) стойкого и прогрессирующего нарушения функции суставов. ЮРА – начавшийся в детском возрасте хронический прогрессирующий системный полисиновиит, приводящий к постепенной деструкции суставов, сочетающийся с продукцией антител к IgG и характерными внесуставными изменениями. ЮРА страдает лишь 0,030,8% детей, но заболевание представляет серьезную социальную проблему, вследствие ранней инвалидизации пациентов. Этиопатогенез. ЮРА болеют чаще девочки, причем более половины детей заболевают в возрасте до 5 лет. Отмечается возможная связь заболевания с перенесенной стрептококковой, стафилококковой, листериозной, микоплазменной, хламидийной, вирусной инфекцией. Однако нет достаточных оснований считать какой-либо из этих микроорганизмов специфическим возбудителем ЮРА. Имеется тесная связь заболевания с носительством определенных генов гистосовместимости HLA (DR 1;2;4;5; B 12;27;35), что подтверждает генетическую предрасположенность к возникновению ЮРА. Пусковым механизмом возникновения ЮРА может быть травма сустава, профилактические прививки, стрессы, температурные воздействия. Неизвестный антиген воспринимается и обрабатывается детритнымии клетками и макрофагами, которые презентируют его Тh0-лимфоцитам. В результате их взаимодействия активируются Т-хелперы 1 типа (Th1), которые стимулируют выработку интерлейкина 2, вызывающего активацию клеточного звена иммунитета с клональной экспансией Тлимфоцитов и ростом В-лимфоцитов, что приводит к активации макрофагов и естественных киллеров, а также гиперпродукции иммуноглобулинов (Ig) класса G. Последние приобретают свойства аутоантигенов и плазматические клетки начинают продуцировать к их фрагментам аутоантитела, которые представлены, в основном, Ig класса М и носят название ревмато- идных факторов (РФ). Взаимодействие иммуноглобулинов G, РФ и комплемента приводит к образованию ЦИК и активации медиаторов воспаления. Активация Th2 приводит к выработке интерлейкина 4, активирующего иммунный ответ по гуморальному типу. Активированные Т-лимфоциты, макрофаги, фибробласты, синовиоциты вырабатывают большое количество провоспалительных цитокинов (интерлейкинов 1, 6, 8, фактора некроза опухоли α и др.), которые определяют как развитие экстраартикулярных проявлений, так и выраженность ревматоидного синовиита. Последний носит хронический деструктивный характер, что связывают с образованием «паннуса» («плаща»), выстилающего поверхность суставного хряща, нарушающего обменные процессы внутри сустава и усиливающего костно-суставную деструкцию. Классификация. В нашей стране широко используется следующая классификация ювенильного ревматоидного артрита (таблица 8). Таблица 8 Классификация ЮРА Форма Преимущественно суставная (с поражением или без поражения глаз) Моноартрит (1 сустав) Олигоартрит (2-4 сустава) Полиартрит (>4 суставов) Суставно-висцеральная С ограниченными висцеритами Синдром Стилла Субсепсис Висслера-Фанкони и аллергосептический вариант ЮРА Сочетанная (с другими ДБСТ) Течение Ак- Иссле- Рентгенологическая тив- дование стадия ность РФ БыстроI Серопо I ст.– околосуставной прогресII зитив- остеопороз сирующее III ст. ный II ст. - тоже + развоМедленвариант локнение хряща и нопросужение суставной грессиСероне- щели рующее гатив- III ст.– деструкция Малопроный хряща, костные и грессивариант костно-суставные рующее эрозии, вывихи и (доброкаподвывихи в сустачественвах ное) IV ст.- тоже + фиброзный или костный анкилоз Нарушение функции I II III степени Выделяют следующие варианты течения ЮРА – мало прогрессирующее (признаки прогрессирования: вовлечение в процесс новых суставов, переход в следующую рентгенологическую стадию и ухудшение функции сустава не определяются в течение 3 лет и более), медленно прогрессирующее (признаки прогрессирования определяются в течение 1,5-3 лет) и быстропрогрессирующее (определяются в течение 1 года болезни). Международная классификация ЮРА (ЮХА), предложенная J.Cassidy и R. Petty (1990) в модификации В.А. Насоновой (1997) выглядит следующим образом: системный вариант с олигоартритом (соответствует аллергосептическому варианту ЮРА) с полиартритом (соответствует синдрому Стилла); полиартикулярный вариант: субтип с наличием РФ; субтип с отсутствием РФ; олигоартикулярный вариант: субтип А, встречающийся, в основном, у девочек раннего возраста, с наличием АНФ, с отсутствием РФ, HLA-B27 и высоким риском развития в катамнезе поражения глаз; субтип Б, наблюдающийся чаще у мальчиков, с началом заболевания в среднем и старшем возрасте, с преимущественным поражением суставов нижних конечностей, наличием HLA-B27 и отсутствием РФ и АНФ; субтип В, встречающийся среди всех возрастных групп, с отсутствием РФ, АНФ и HLAB27. Клиника. Суставная форма ЮРА встречается у 70% больных ЮРА. Типично подострое начало на фоне субфебрилитета с появления болей и припухлости суставов, с ограничением его функции. Типична утренняя скованность и уменьшение болевого синдрома во вторую половину дня. При высокой степени активности процесса возможно местное повышение температуры. Постепенно развивается атрофия мышц. В половине случаев суставная форма ЮРА у детей начинается с моноартрита коленного сустава. Но в дальнейшем в процесс вовлекаются другие суставы: проксимальные межфаланговые суставы кистей рук, лучезапястные и голеностопные и др. Исключить диагноз ЮРА позволяют следующие признаки: 1) поражение в дебюте заболевания грудино-ключичных, грудино-реберных, плечевых, дистальных межфаланговых, тазобедренных, крестцово-подвздошных, плюсне-фаланговых и мелких суставов стоп; 2) «SEA»-синдром, характеризующийся серонегативностью, артритами и энтезопатиями (воспалением в местах прикрепления связок и сухожилий к костям), которые проявляются локальной гиперемией, припухлостью и болезненностью, особенно, при движении и пальпации; 3) наличие в дебюте заболевания синовиальных «кист Бейкера» (чаще в подколенной области). Из общих симптомов для этой формы ЮРА типичны признаки полигиповитаминоза (сухость кожи, ломкость волос, ногтей), лимфоаденопатия. Ревматоидный увеит встречается у каждого пятого ребенка с ЮРА, и проявляется триадой симптомов: катаракта, иридоциклит, лентовидная дистрофия роговицы, которую выявляет лишь осмотр на щелевой лампе. При развитии увеита у девочек младшего возраста в катамнезе высок риск развития тяжелых нарушений зрения, вплоть до полной слепоты. Суставно-висцеральная форма ЮРА встречается у 30% детей. Самый тяжелый вариант ее течения – синдром Стилла, который встречается преимущественно у маленьких детей. Начинается остро с повышения температуры до фебрильных цифр, появления выраженных симптомов общей интоксикации, болей и припухлости пораженных суставов. Лихорадка неправильного типа. Типичны похудание, бледность кожи, трофические расстройства, возможны полиморфные сыпи. Сравнительно редко походу сосудов или над суставами могут пальпироваться ревматоидные узелки, которые чаще наблюдаются при длительном течении ЮРА. В период максимальной активности характерно поражение суставов кистей рук, коленных, тазобедренных, височно-нижнечелюстных и суставов позвоночника, особенно шейного отдела. Боли в суставах настолько интенсивные, что ребенок практически полностью обездвижен и реагирует даже на прикосновение простыни (симптом «простыни»). Патогномонична реакция лимфоидных органов: увеличение лимфатических узлов (в большей степени локтевых и подмышечных), селезенки и печени с нарушением функции последней. Из висцеральных проявлений при этом варианте ЮРА наиболее часто отмечается поражение сердечно-сосудистой системы и почек, реже - легких. У большинства больных диагностируется миокардит или миоперикардит, иногда в сочетании с аортитом. Поражение легких проявляется интерстициальной пневмонией и плевритом. На современном этапе ввиду скудности клинической симптоматики диагностика кардита и плевропневмонита затруднена, и основное значение имеют инструментальные методы исследования. Поражение почек при ЮРА проходит несколько стадий. Для начальных стадий характерно лишь изменение мочевого осадка и незначительная протеинурия. При неблагоприятном течении процесс переходит в нефротическую стадию, для которой типичны значительная протеинурия, диспротеинемия и гиперлипидемия. Однако, несмотря на то, что имеется нарушение функции почек, АД долгое время остается нормальным. В дальнейшем прогрессирует почечная недостаточность и процесс переходит в терминальную азотемическую стадию, морфологическим признаком которой является амилоидоз почек. Последний может быть диагностирован лишь при биопсии. Суставно-висцеральная форма с ограниченными висцеритами занимает промежуточное место между полиартикулярным вариантом суставной формы ЮРА и синдромом Стилла. Аллерго-септический вариант ЮРА и аллергосепсис Висслера-Фанкони начинается внезапно с подъема температуры до фебрильных или гектических цифр, особенно в утренние часы, в сочетании с ознобом. Снижение температуры сопровождается проливным потом. Выражены симптомы общей интоксикации. Лихорадка рефрактерна к антибиотикам в течение 2-3 недель. Кардинальный признак аллергосепсиса – полиморфная сыпь, чаще по типу коре- или скарлатиноподобной, но патогномоничной заболеванию считают линейную сыпь, расположенную на боковых поверхностях туловища и разгибательных поверхностях конечностей. Из висцеральных поражений типичны полисерозиты (перикардит, плеврит, серозный перитонит). Суставной синдром может присоединиться спустя недели и даже месяцы от начала болезни. Диагностика. В анализах крови у детей с ЮРА - гипохромная анемия, нормальное или сниженное (при синдроме Стилла) количество лейкоцитов, небольшой нейтрофилез (при субсепсисе - выраженный), ускорение СОЭ (значительное и длительное). Определение мукоидных соединений и белковых сдвигов имеет вспомогательное значение. Высокая лабораторная активность характерна для системных вариантов. В иммунограмме – гипериммуноглобулинемия, неблагоприятно обнаружение Ig G и ЦИК. Вспомогательные методы диагностики - тепловизионное исследование и УЗИ, позволяющее в большинстве случаев судить о наличии выпота и характере воспалительного процесса (экссудативный, пролиферативный). При наличии жидкости показана пункция сустава. Исследование синовиальной жидкости при ЮРА выявляет ее обилие, низкую вязкость и высокое содержание белка. Наблюдается нейтрофильный цитоз. Обнаружение РФ в синовиальной жидкости и/или плазме крови (реже) возможно лишь у 15-20% детей. Важную роль в диагностике имеет рентгенологическое исследование. Для начальных стадий ЮРА характерны увеличение размеров эпифизов, более раннее появление ядер окостенения, деформация и нарушение роста костей. Диагностические критерии ЮРА Клинические признаки: 1. Артрит, продолжительностью 2-3 мес. и более 2. Артрит второго сустава, возникающий через 2-3 мес. и позже 3. Симметричное поражение мелких суставов 4. Ревматоидное поражение глаз 5. Ревматоидные узелки 6. Утренняя скованность 7. Тендосиновиит, бурсит 8. Выпот в полость сустава 9. Контрактура сустава или ревматоидный васкулит Рентгенологические признаки 10. Поражение шейного отдела позвоночника 11. Остеопороз, мелкокистозная перестройка структуры эпифизов 12. Сужение суставной щели, костные эрозии 13. Анкилоз суставов 14. Нарушение роста костей. Лабораторные признаки 15. Положительный РФ в плазме крови и/или синовиальной жидкости 16. Положительные данные биопсии синовиальной оболочки. Диагноз ЮРА считается вероятным при наличии 3, определенным – при наличии 4 и классическим при наличии 8 признаков, обязательным из которых является артрит. Дифференциальный диагноз ЮРА проводят с ДБСТ, ревматизмом, инфекционными заболеваниями (иерсиниоз, болезнь Лайма, тиф, паратифы), острым лейкозом, туберкулезом. Лечение. В период обострения ребенок госпитализируется в стационар. Назначают полноценное питание с достаточным количеством белка, витаминов. Двигательная активность определяется тяжестью процесса. Основной метод лечения – фармакотерапия. Для лечения используют ГКС, НПВС и медленнодействующие средства, схема применения которых представлены в таблице 6. НПВС назначаются при суставной форме ЮРА длительно (в течение нескольких месяцев или лет), курсами на 2-3 недели с последующей сменой препарата. Предпочтение отдают диклофенаку-натрия (вольтарен, ортофен), индометацину (метиндол) и напроксену (напросин). Таблица 9 Терапия ювенильного ревматоидного (хронического) артрита Суставная форма ЮРА Аллергосептический вариант, аллерВариант ОлигоарПолиартрит госепсис Вислера-Фанкони Стилла трит НПВС Не целесообразно Вольтарен (2-3 мг/кг/сут), другие НПВС Иммуно- Метотрексат (МТ) 7,5-10-12 мг/м2/нед. Циклоспорин Метотрексат, депресЦиклоспорин А (сандиммун-Нео) 3,5-4,5 мг/кг/сут. Если А и/или ме- Циклоспорин, санты эффект недостаточный – комбинации: тотрексат Делагил или МТ 8,2–8,4 мг/м2/нед. + ЦсА 4–4,5 мг/кг/сут или Сульфасала- комбинации МТ 10 мг/м2/нед. + сульфасалазин 30–40 мг/кг/сут зин (40-50 МТ с другими мг/кг/сут) средствами ВВИГ Имбио, пентаглобин, интраглобин, октагам, сандоглобу- Эффективность не доказана лин в/в капельно 0,3-1 г/кг/курс (при синдроме Стилла Возможно применение при только в сочетании с иммунодепрессантами) сопутствующей инфекции Симпто- Дезинтоксикационные препараты, средства нормали- Хондропротекторы, прематичес- зующие функцию сердечно-сосудистой и дыхательной параты кальция, ГКС местно кая тера- систем и др. при увеите Системная форма ЮРА пия Антибио- Аминогликозиды 3-4 поколений (амикацин, нетроми- Только при наличии признатики цин), пенициллины (пиперациллин), цефалоспорины ков инфекции Плазмаферез ГКС (клафоран, цефобид, роцефин, фортум, цефепим), метронидазол, фторхинолоны (абактал, ципролет) в/в или в/м 10-14 дней в монотерапии или в сочетаниях. При неэффективности - дополнительный курс тиенама или меронема Плазмаферез в сочетании с пульс-терапией метилпред- Не показан низолоном (МП) и МТ Пульс-терапия МП в/в 10–15 мг/кг Не показана Локальная (внутрисуставная) терапия ГКС: При неэффективности всех перечисленных мероприятий - преднизолон внутрь в дозе 0,3-1 мг/кг/сут, но не более 60 мг/сут у детей любого возраста Общими побочными эффектами НПВС является способность вызывать гастропатию, угнетать кроветворение и тормозить агрегацию тромбоцитов. Поэтому, необходим периодический эндоскопический и гематологический контроль, применение цитопротекторов - синтетических простагландинов, антацидных или антисекреторных препаратов. При невысокой активности возможно использование ингибиторов циклоксигеназы-2 - миелоксикама (мовалиса) и нимесулида (найза, нимулида). Основным свойством медленнодействующих противоревматических препаратов является способность замедлять суставную деструкцию и прогрессирование болезни, однако их эффект развивается лишь при длительном применении. В настоящее время иммунодепрессанты считают необходимым компонентом терапии всех вариантов ЮРА, кроме доброкачественного течения суставной формы и аллергосепсиса Висслера-Фанкони. «Золотым стандартом» противоревматической терапии считается метотрексат (МТ), лечение которым начинают с 7,5-10 мг/м2 внутрь 1 раз в неделю с возможным увеличением дозы и периодическим контролем аминотрансфераз. Сульфасалазин показан при субтипе Б олигоартрита (у мальчиков с поражением суставов нижних конечностей). Начинают лечение с ¼ дозы и постепенно (в течение 4-х недель) увеличивают ее. При этом, как и при использовании других иммунодепрессантов, необходим тщательный контроль периферической крови. Циклоспорин А высокоэффективен при серонегативных суставных вариантах ЮРА и при синдроме Стилла. Но даже современные базисные средства не всегда в состоянии остановить прогрессирование ЮРА. Поэтому при необходимости их меняют или комбинируют. При суставно-висцеральной форме и реже при тяжелых гормонозависимых полиартикулярных вариантах ЮРА применяют пульс-терапию метилпреднизолоном (МП) – 3-5 в/в капельных инъекций в дозе 10-15 мг/кг (250-500 мг) с последующим постепенным снижением дозы (раз в 2-3 дня), переходом на в/м способ введения и отменой. В случае высокой местной активности процесса при любой форме ЮРА используют внутрисуставное введение ГКС: депо-медрола или реже дипроспана. Антибактериальная терапия показана при аллергосепсисе и любых других вариантах ЮРА, осложненных присоединением инфекции. Наиболее часто у больных с ЮРА/ЮХА обнаруживают лабораторные признаки хламидийной инфекции, что является показанием к использованию макролидов в монотерапии или в сочетании с иммуномодуляторами (ликопид). Кроме того, этим больным рекомендовано введение ВИГ, оказывающего не только противоинфекционное (за счет наличия антител к большинству бактерий и вирусов), но и мягкое иммуносупрессивное действие. Местно также назначают аппликации с 10-15% раствором димексида, мази и гели с НПВС (фастум-гель, долгит-крем, гель диклофенака и др.), гепариновую мазь, хондроксид. Также используют электрофорез с НПВС, массаж, лазеро-, магнитотерапию, при стихании активности – ЛФК. Для профилактики остеопороза применяют активные метаболиты витамина Д и препараты кальция (кальций-Д3-Никомед), бифосфонаты и кальцитонин (миокальцик). Для лечения остеопороза показаны остеогенон (2 капсулы по 800 мг в сутки) и структум (хондроитина сульфат) курсами до 8 месяцев. Диспансеризация. Цель ее – закрепить эффект терапии, поддержать ремиссию и наметить пути реабилитации. Наблюдение осуществляется до передачи во взрослую сеть. На 1 году болезни ревматолог осматривает ребенка – 1 раз в квартал, затем - раз в полгода. Вопросы для тестового контроля № п/п 1 2 3 4 5 6 7 Содержание вопросов Лабораторные критерии диагностики ЮРА: а) положительные данные биопсии синовиальной оболочки, б) LE-клетки, антинуклеарный фактор, в) положительный РФ в крови и/или синовиальной жидкости, г) ускорение СОЭ более 40 мм/час, д) диспротеинемия Сужение суставной щели и единичные костные узуры характерны для а) I рентгенологической стадии ЮРА, б) II рентгенологической стадии ЮРА, в) III рентгенологической стадии ЮРА, г) IV рентгенологической стадии ЮРА Системное назначение глюкокортикоидных гормонов не показано: а) при суставной форме ЮРА, б) при суставно-висцеральной форме с ограниченными висцеритами, в) аллергосептическом варианте, г) варианте Стилла, д) при аллерго-сепсисе Висслера-Фанкони В план обследования при ЮРА обязательно входят: а) общ. ан. крови, б) общ. ан. мочи, в) проба Зимницкого, г) Эхо-КГ, д) осмотр окулиста Амилоидоз при ЮРА чаще всего возникает в: а) почках, б) сердце, в) суставах, г) стенке сосудов, д) печени Основные патоморфологические изменения в суставах при ЮРА не включают: а) пролиферативные и фибропластические процессы, б) склероз капсулы сустава, в) образование паннуса, г) экссудативный компонент, д) кровоизлияние в сустав При стойкости болевого синдрома у больного с артритом несмотря на проводимую противовоспалительную терапию, следует думать о: а) лейкозе, б) Эталоны ответов а, в б а а, б, д а д а, в 8 9 10 остеомиелите, в) туберкулезе, г) ревматизме, д) бореллиозе Для ЮРА наиболее характерно поражение в дебюте болезни: а) коленных, а голеностопных суставов, б) мелких суставов кистей, в) мелких суставов стоп, г) локтевых суставов, д) всех групп суставов Возбудитель ЮРА: а) вирусы, б) бактерии, в) микоплазмы, г) хламидии, д) не д известен ЮРА болеют преимущественно: а) дети грудного возраста, б) школьники, в) в дошкольники, г) подростки, д) независимо от возраста Ситуационные задачи № п/п 1 2 Содержание задач Эталоны ответов Игорь Б., 7 лет, направлен в клинику для установления диагноза с подозрением на сепсис. Среди полного здоровья повысилась температура до 40°С появились уртикарные высыпания. Обследовался в инфекционной больнице. Выявлена гиперплазия лимфатических узлов, печени, селезенки. Периодически отмечены боли в суставах и животе. Неоднократный посев крови, реакция Видаля, туберкулиновые пробы дали отрицательный результат. Проведено лечение ампициллином – без эффекта. В течение 4 недель у больного сохранялась лихорадка неправильного типа, временами - гектическая. Снижение температуры сопровождалось проливным потом, ознобом. Лишь спустя 6 месяцев от начала заболевания, появились признаки артрита коленных, а затем голеностопных и других суставов, что позволило заподозрить ревматоидное заболевание. Вопросы: 1.Сформулируйте диагноз. 2.Укажите ошибки в тактике ведения больного. 3. Каков план дальнейшего обследования и лечения? 1: Ювенильный ревматоидный артрит, суставнно-висцеральная форма, аллерго-септический вариант, активность 2—3 ст. 2. Основная ошибка состоит в том, что при длительно сохраняющемся лихорадочном состоянии с поражением кожи, ретикуло-эндотелиальной системы, серозитах и отсутствии суставных явлений должен был быть заподозрен субсепсис Висслера-Фанкони. Помимо исключения инфекций и исследования острофазовых воспалительных показателей (протеинограмма, серомукоид, СРБ, ДФА, реакция Жокинена, ГОФ), необходимо было провести исследование крови на ревматоидный фактор и клинико-инструментальное обследование почек (проба Зимницкого, Реберга, УЗИ, ан. крови на мочевину, креатинин) и сердечно-сосудистой системы (ЭКГ, Эхо- КГ, рентгенография органов грудной клетки). Обязательно надо было провести клинический анализ крови, исследование крови на маркеры гепатита и консультацию гематолога. 3. Показан осмотр окулиста, ЛОР–врача, стоматолога, иммунограмма, ан. на хламидии, исследование синовиальной жидкости, рентгенография суставов. Принципы лечения: пульс-терапия метилпреднизолоном с последующим переходом на в/с инъекции в сочетании с ВВЧИГ и массивной антибактериальной терапией, базисная терапия метотрексатом и/или сульфасалазином. А также санация очагов инфекции, лазеротерапия, массаж, - ЛФК, хондропротекторы. Диагноз: Ювенильный ревматоидный артрит, преимущественно суставная форма, олигоартритический вариант, активность 1-2 ст, быстропрогрессирующее течение, НФС 0-1. В плане обследования: клинические анализы крови и мочи, протеинограмма, ан. крови на серомукоид, СРБ, ДФА, реакцию Жокинена, ГОФ, ревматоидный фактор; рентгенография суставов, ЭКГ, иммунограмма, окулист, ЛОР–врач, стоматолог. По показаниям: ЭХО КГ, тепловидение, рентгенография органов грудной клетки, ан. крови на реакцию Видаля и HBsAg, ан. крови или соскоб на хламидии, пункция сустава с последующим исследованием синовиальной жидкости. Принципы лечения: НПВС (вольтарен – на 2-3 недели с последующим переходом на нимесулид), внутрисуставное введение глюкокортикоидов (депо-медрол), базисная терапия метотрексатом с фолиевой кислотой. Показано также лечение хронических очагов инфекции, магнитотерапия, лазеротерапия, местное использование Люся М., 11 лет, больна в течение 6 лет. После ушиба появились боли и опухание правого голеностопного сустава, Осмотрена хирургом, диагностировано растяжение связок. Через 3 месяца девочка консультирована по поводу виража туберкулиновой пробы (реакция Манту – папула 17 мм) фтизиопедиатром, которым выявлена деформация правого коленного сустава. Заподозрен туберкулез суставов, который при дальнейшем рентгенологическом обследовании не подтвердился, но ребенку было проведено специфическое противотуберкулезное лечение. Суставной синдром купирован, но через 5 месяцев вновь появились признаки артрита обоих коленных суставов: боль, припухлость, небольшое ограничение движений. Девочка направлена в клинику для выяснения диагноза. Вопросы:1.Ваш диагноз? 2.Тактика об- гелей и мазей с НПВС и компрессов с димексиследования и лечения? дом и гепарином. Рекомендуемая литература: Основная: 1. Шабалов Н.П. Детские болезни. Изд - е 5-е. В двух томах. Т. 2., Ст.- Пб: Питер, 2006.-731с. 2. Детская ревматология. Руководство для врачей. //Под редакцией А.А.Баранова и Л.К.Баженовой. М.Медицина, 2002.-336с. Дополнительная: 1. Беляева Л.М., Хрусталева Е.К. Сердечно-сосудистые заболевания у детей и подростков. – Минск: Высшая школа, 1999.- 301с. 2. Доэрти М., Доэрти Дж. Клиническая диагностика болезней суставов: Пер. с англ.Минск: Тивал, 1993.-144 с. 3. Практическое руководство по детским болезням. Под общей редакцией проф. В.Ф. Коколиной и проф. А.Г.Румянцева. Том III. Кардиология и ревматология детского возраста. Под ред. Г.А. Самсыгиной и М.Ю. Щербаковой. Медпрактика - М, Москва, 2004, 125223с. Занятие № 5. НЕРЕВМАТИЧЕСКИЕ КАРДИТЫ У ДЕТЕЙ Цель занятия: изучить этиологию, классификацию, особенности клиники врожденных и приобретенных кардитов, принципы лечения, вопросы диспансеризации и реабилитации. Вопросы для самоподготовки: 1. Этиология и патогенез неревматических кардитов 2. Классификация 3. Клиника врожденных кардитов 4. Клиника приобретенных кардитов 5. Инструментальная характеристика кардитов 6. Дифференциальная диагностика кардитов 7. Лечение, диспансеризация. Неревматический кардит (НК) – это заболевание миокарда воспалительного генеза, возникающее под действием различных инфекционных агентов, характеризуется воспалительной инфильтрацией миокарда с фиброзом, некрозом и/или дегенерацией миоцитов, не связанное с β-гемолитическим стрептококком группы А. В воспалительный процесс могут вовлекаться кардиомиоциты, интерстициальная ткань, сосуды, проводящая система сердца, а также перикард. Этиология. Выделяют 3 формы заболевания: инфекционные миокардиты, аллергические миокардиты, токсико-аллергические миокардиты (лекарственные, сывороточные, поствакцинальные, при ДБСТ, в результате повреждения миокарда физическими и химическими агентами). Заболевание чаще встречается у детей, чем у взрослых, болеют преимущественно мальчики. Тяжелые формы чаще диагностируются у детей раннего возраста. Наиболее распространенной причиной считают вирусы, особенно энтеровирусы (Коксаки А и В, ЕСНО), герпеса, краснухи, цитомегаловирусы, обладающие кардиотропностью. Причиной кардитов также могут быть бактерии (стрептококки группы В, стафилококки, протей и др.), токсоплазмы, хламидии, токсические (при дифтерии), паразитарные, идиопатические НК. Предрасполагающие факторы: наследственность, несовершенство иммунной системы, хронические очаги инфекции, состояние реактивности макроорганизма, аномалии конституции. Н.А.Белоконь предложена рабочая классификация НК у детей (таблица 10). Таблица 10 Период возникновения заболевания Этиологический фактор Форма (по преимущественной локализации процесса) Течение Тяжесть кардита Форма и степень СН Исходы и осложнения Врожденный – ранний и поздний Приобретенный Вирусный, вирусно-бактериальный, бактериальный, паразитарный, грибковый, иерсиниозный, аллергический (лекарственный, сывороточный), идиопатический Диффузный Поражение проводящей системы сердца Острое – до 3 мес., подострое – до 18 мес., хроническое – более 18 мес. (рецидивирующее, первично хроническое): застойный, гипертрофический, рестриктивный варианты Легкий, среднетяжелый, тяжелый Левожелудочковая I, IIA, Б, III степени Правожелудочковая I, II А, Б, III степени Кардиосклероз, гипертрофия миокарда, нарушение ритма и проводимости, легочная гипертензия, поражение клапанного аппарата, констриктивный миоперикардит, тромбоэмболический синдром Распространенность. Статистические данные о частоте и распространенности миокардитов скудны и разноречивы. По данным Ю.М.Белозерова миокардит в популяции составляет не более 10 на 100 000 населения. По данным других авторов он диагностируется в 1-15% случаев всех заболеваний, вызванных вирусной инфекцией и в 3-10% всех вскрытий. Патогенез. Выделяют три основных патогенетических механизма развития поражения миокарда в виде воспалительной реакции под действием инфекционных агентов: 1.Проникновение инфекционного агента в миокард, 2.Продукция миокардиальных токсинов, 3. Иммунное поражение миокарда. В настоящее время патогенез миокардитов рассматривается как иммунопатологический процесс - миокардит возникает лишь при сочетании внедрения вируса в клетку и нарушенной иммунологической реактивности. Патогенез острых и хронических НК различен. При острых имеет значение воздействие инфекционного агента, выделение медиаторов воспаления, возникновение реакции гиперчувствительности немедленного типа. При хроническом течении возбудитель не играет решающей роли и в основе заболевания лежат аутоиммунные нарушения. Выделяют три фазы воспаления: 1.Острая: вирусемия приводит к проникновению вируса в кардиомиоцит с последующей репликацией, 2. Подострая фаза: аутоиммунная фаза, опосредованная Т-клетками (4-14 день) с образованием аутоантигена, увеличением синтеза оксида азота, 3. Хроническая фаза: с 15-го дня до 90-го: наличие диффузного фиброза и сердечной недостаточности. Врожденные кардиты (ВК) – редкий диагноз, который ставится на основании тяжелого состояния новорожденного, наличия у него выраженных клинических симптомов внутриутробного генерализованного инфекционного процесса с поражением многих органов и систем, данных лабораторно-инструментальных методов. По анатомическому субстрату ВК делят на ранние и поздние. Определить, в какой период внутриутробного развития плода возник кардит , можно лишь по морфологическому субстрату раннего кардита – обилию эластической и фиброзной ткани в эндомиокарде. Ранние ВК возникают в результате воздействия повреждающего этиологического фактора в ранний фетальный период (4-7 месяц внутриутробного развития), когда ткани плода отвечают на альтерацию пролиферацией с развитием эластоза и фиброза, поэтому обязательным морфологическим признаком ранних кардитов является фиброэластоз (преобладание эластической ткани) или эластофиброз (преобладание фиброзной ткани) эндо-и миокарда, причем эластофиброз в отличии от фиброэластоза сочетается с признаками воспаления и является переходным признаком между ранним и поздним кардитом ВК, имеет более благоприятный прогноз. При поражении сердца после 7-го месяца внутриутробного развития наблюдается обычная воспалительная реакция и не развивается фиброэластоз (поздний ВК); ребенок может родиться как с исходом кардита, так и с текущим воспалительным процессом, что зависит от сроков появления заболевания. По последним данным фиброэластоз эндокарда является морфологическим понятием, подразу- мевающим неспецифическую реакцию эндокарда в ответ на миокардиальный стресс любой этиологии – воспаление, гипоксия. Первые признаки заболевания при обоих вариантах появляются в первые 6 месяцев жизни. В клинике различают экстракардиальные и кардиальные симптомы. Первыми клиническими проявлениями могут быть симптомы застойной сердечной недостаточности. Экстракардиальные проявления ранних ВК: низкая масса тела при рождении, затем плохая прибавка в массе, беспричинные приступы беспокойства, афония, вялость, бледность, сниженный аппетит, утомляемость при кормлении, потливость, мраморность кожных покровов. Кардиальные: одышка, сердечный горб, увеличение границ сердечной тупости, ослабление верхушечного толчка, приглушенность или глухость тонов, тахикардия, возможен трехчленный ритм галопа на верхушке, может быть систолический шум недостаточности митрального клапана, левожелудочковая недостаточность, рефрактерная к терапии. При сочетании кардита с ВПС могут быть аритмии. Инструментальная и лабораторные методы: ЭКГ – высокий вольтаж QRS, ригидный частый ритм, отклонение ЭОС влево, нарушение внутрижелудочковой проводимости, гипертрофия левого желудочка, субэндокардиальная ишемия миокарда, глубокий зубец Q в отведениях II, III AVF, V5,6. Рис. 1 ЭКГ при раннем врожденном кардите Рентгенологически легочный рисунок нормальный или незначительно усилен по венозному руслу, кардиомегалия (рис .2), форма сердца шаровидная или овоидная Эхокардиография: дилатация полостей сердца, гипертрофия миокарда, признаки фиброэластоза эндомиокарда, нарушение сократительной функции. Лабораторные методы исследования. Результаты общего анализа крови зависят от этиологии кардита. Для вирусного характерны лейкопения, лимфоцитоз, замедление СОЭ, бактериального – лейкоцитоз, нейтрофильный сдвиг, повышение СОЭ, при аллергических – эозинофилия, лейкоцитоз, нейтрофилез, ускорение СОЭ. Биохимические сдвиги обычно не изменены или не начительны кратковременны: положительный Рис. 2. Кардиомегалия при ВК СРБ, небольшое увеличение А2 глобулинов. В последние годы достигнуты определенные успехи в использовании новых высокочувствительных биохимических тестов, значительно пополняется информация о состоянии клеточных мембран кардиомиоцитов, нарушении внутриклеточного метаболизма, изменении активности ферментов митохондрий. Наиболее значимыми из лабораторных тестов являются повышение активности ЛДГ и ее «кардиальных» изоэнзимов – ЛДГ1 и ЛДГ2 , миокардиальной фракции КФК – изоферменту МВ (причем в последнее время предпочитают определять концентрацию этого белка иммунохимиче- ским методом), АСТ и АЛТ. При поражении кардиомиоцитов раньше всего в крови повышается содержание миоглобина (гемсодержащий пигментный белок, находящийся в мышечных клетках скелетных мышц и в кардиомиоцитах, основной функцией которого является удержание кислорода и создание его запасов в сердечной мышце), гликогенфосфорилазы-ВВ (ГФ-ВВ) и тропонина (TnI и TnT), кардиоспецифичность их обусловлена высокой концентрацией в миокарде и отсутствием в других тканях и в крови здоровых людей. Далее повышается КФК, КФК-МВ, АСТ, и существенно позже повышается активность ЛДГ и кардиоспецифического фермента ЛДГ1. Активность ЛДГ1 является маркером гибели миоцитов после 12-ти часов поражения и остается повышенным 10-12 дней. Содержание TnT при миокардитах может быть увеличено в течение нескольких недель после начала заболевания, что важно для поздней диагностике заболевания. Важным и перспективным направлением является изучение роли провоспалительных и противовоспалительных цитокинов. В ранней диагностике воспаления сердца применяются методы, отражающие изменения цитохимической активности лимфоцитов Установлено, что лимфоцитам крови свойственен тип метаболизма, близкий к таковому сердечной ткани, т.е. лимфоциты выступают в роли своеобразного ферментативного зеркала миокарда. Среди ферментов лимфоцитов важное значение имеют: КФ (кислая фосфатаза) локализуется в лизосомах, участвует в процессах разрушения и удаления токсических продуктов, расщепления отработанных структур клетки; СДГ (сукцинатоксидоредуктаза) – классический митохондриальный маркер, регулирует течение дыхательных процессов в митохондриях; α- ГФДГ (α - глицерофосфатдегидрогеназа) обеспечивает процессы координации гликолиза и окисления в лимфоцитах, снижение, а тем более «выпадение» его активности свидетельствует о переходе на менее экономный путь обменных процессов. В активном периоде миокардита отмечается повышение активности СДГ при снижении активности α- ГФДГ. В иммунограмме характерно повышение содержание иммуноглобулинов: в первые 2 недели заболевания-IgМ и позже IgG; возможны: уменьшение активных Т- лимфоцитов, нарушение соотношения Т-хелперов и Т - супрессоров, повышение уровня ЦИК и В-лимфоцитов. Значимыми в диагностике являются вирусологические и серологические реакции (нейтрализации, связывания комплемента, гемагглютинации). Титр вирусных антител увеличивается в 4 и более раз в парных сыворотках крови в течение 2-4 недель и постепенно снижается в период реконвалесценции. Критерием постановки диагноза является эндомиокардиальная биопсия. Сцинтиграфия является перспективным неинвазивным методом диагностики. Используют радионуклид галлий-67, обладающий тропизмом к зонам воспаления, и моноклональные антитела к миозину, меченные индием-111 – высокочувствительный метод выявления некроза кардиомиоцитов. Поздние ВК. Экстракардиальные симптомы.: плохая прибавка в массе при нормальной массе тела при рождении, беспокойство, судороги, повторные пневмонии, остальные признаки – как при ранних ВК. Кардиальные: умеренное расширение границ сердца, приподнимающийся верхушечный толчок, более звучные тоны и менее выраженные признаки сердечной недостаточности, чем при ранних ВК, шума в сердце чаще не бывает, характерны различные нарушения ритма. Инструментальные и лабораторные методы: ЭКГ – нарушения ритма – тахи- или брадикардия, экстрасистолия, пароксизмальная и непароксизмальная тахикардия, мерцательная аритмия, различные блокады, синдром слабости синусового узла, перегрузка левых отделов сердца, признаки гипертрофии левого желудочка. На рентгенограмме тень сердца увеличена. Эхокардиография – дилатация полостей сердца (преимущественно левых), снижение фракции выброса (менее 55%), возможна гипертрофия миокарда. Лабораторные показатели как и при ранних ВК. Прогноз при ВК: при ранних – неблагоприятный, продолжительность жизни не более 1,5 лет, при поздних - относительно благоприятный, но вероятен переход в хронический. Приобретенные кардиты. Острые. Тяжелые формы встречаются чаще у детей первых 3-х лет жизни. Как правило первые признаки заболевания выявляются на фоне ОРВИ или спустя 1-3 недели. Первыми признаками острого кардита чаще являются Экстракардиальные симптомы: вялость, слабость, утомляемость при кормлении, снижение аппетита, боли в животе, тошнота, рвота, потли- вость, раздражительность, беспокойство, стоны, приступы возбуждения, цианоза, потери сознания, навязчивый кашель. Далее нарастают кардиальные. Исход острого НК может быть различным: у половины детей заболевание принимает подострое, а затем хроническое течение, летальность до 2,2%. Подострые НК. По течению подразделяются на 2 подгруппы:1. С торпидным течением болезни, постепенным нарастанием сердечной недостаточности через 4-6 месяцев после перенесенной инфекции (первично подострые); 2. С очерченной острой фазой, переходящей на фоне лечения в длительный процесс. Встречаются реже, чем острые, чаще болеют дети от 2 до 5 лет. Признаки заболевания носят неспецифический характер – вялость, повышенная утомляемость, сонливость, снижение аппетита, температурная реакция чаще отсутствует. Экстракардиальные и кардиальные симптомы имеют менее яркие проявления, чем при острых НК. Могут быть различные нарушения ритма, систолический шум недостаточности митрального клапана. Лабораторные данные обычно спокойные. Подострые НК отличаются стойкостью симптомов, резистентностью к терапии, неблагоприятным течением из-за перехода в хронический. Летальность достигает 16% (Н.А.Белоконь, 1987). Хронические кардиты (ХК). Обычно развиваются у детей старше 7 лет. Выделяют 2 варианта ХК: ХК1 – застойный (дилатационный) вариант для которого характерно: дилатация левого желудочка и других камер сердца, выраженные склеротические и дистрофические процессы в миокарде, нарушение систолической функции. ХК2 – гипертрофический вариант, характеризуется преобладанием гипертрофических процессов и нарушением диастолической функции, нормальной или уменьшенной полостью левого желудочка. Этот вариант встречается реже. ХК чаще имеет первично хроническое течение. Экстракардиальные симптомы: отставание в физическом развитии, слабость, утомляемость, навязчивый сухой кашель, рецидивирующие пневмонии, гепатомегалия, реже рвота, приступы потери сознания. Среди первых кардиальных симптомов – одышка, систолический шум, внезапно развившаяся острая сердечная недостаточность, нарушения ритма. Особо следует выделить НК с преимущественным поражением проводящей системы сердца. Они встречаются чаще у детей старшего возраста, характеризуются стертой и маломанифестной клиникой и лабораторными показателями, но выраженными ЭКГ признаками нарушений в проводящей системе сердца - эктопические ритмы, политопная и полиморфная частая экстрасистолия, блокады. Признаки 2-х вариантов ХК представлены в таблице № 8 Прогноз при ХК серьезный, летальность 26,3%, а с течением времени 100%, имеется опасность наступления внезапной смерти. Схема клинической диагностики миокардитов, предложенная NYNA (1964, 1973) Критерии диагностики Связь с перенесенной инфекцией, доказанная клинически лабораторными данными: выделение возбудителя, результаты реакции нейтрализации, реакция связывания комплемента, реакция гемагглютинации, ускорение СОЭ, появление С-реактивного белка Признаки поражения миокарда Большие признаки: - патологические изменения на ЭКГ (нарушения реполяризации, нарушения ритма и проводимости); - повышение концентрации в крови кардиоселективных ферментов и белков (КФК, КФКМВ, ЛДГ, тропонин Т); - увеличение размеров сердца по данным рентгенографии или ЭхоКГ -застойная недостаточность кровообращения -кардиогенный шок Малые признаки: - тахикардия (иногда брадикардия); - ослабление первого тона; - ритм галопа Диагноз миокардита правомочен при сочетании предшествующей инфекции с одним большим и двумя малыми признаками Диагностические критерии миокардита (О.А. Мутафьян, 2006): 1. Миокардитический синдром (тахикардия, ослабленный и разлитой верхушечный толчок, расширение границ сердца преимущественно влево, ослабление или глухость 1 тона на верхушке, незначительное усиление II тона на легочной артерии, появление трехчленного ритма и систолического шума на верхушке, снижение САД, боли в сердце, характерные больше для миоперикардита. 2. Синдром сердечной недостаточности 3. Электрокардиографический синдром (снижен вольтаж зубцов первые 2-3 недели, перегрузка предсердий, желудочков, синусовая тахикардия, могут быть различные нарушения ритма и проводимости, нарушение процессов реполяризации миокарда желудочков). 4. Инструментально-рентгенологическое и лабораторное подтверждение (рентгенологически - усиление кровенаполнения венозного русла, корни расширены, конфигурация тени сердца варьирует. Эхокардиография – дилатация преимущественно левого желудочка и предсердия, гипокинезия МЖП и задней стенки ЛЖ, снижение функциональной способности миокарда; Лабораторные методы описаны выше). Диагностические критерии миокардитов для детей первого года жизни (Н.П.Котлукова,2002) Синусовая тахи- или брадикардия Увеличение размеров сердца Ослабление, расщепление 1 тона Ритм галопа Мягкий систолический шум Любые нарушения ритма и проводимости Снижение сократительной способности миокарда и увеличение полостей сердца по ЭХОКГ Таблица 11 Дифференциально-диагностические признаки хронических кардитов Симптомы Физическое развитие Малиновый цианоз Верхушечный толчок Сердечный горб Границы сердца Тоны сердца Шумы Частота сердечных сокращений Одышка Увеличение печени Хр. кардит с увеличенной полостью левого желудочка (ХК 1) Клинические Дефицит массы тела Редко Разлитой, ослабленный Хронический кардит с нормальной или уменьшенной полостью левого желудочка (ХК II) Тахикардия Дефицит массы тела и роста Часто Приподнимающийся, локализованный Может быть и менее выражен Умеренно или резко расширены в обе стороны Громкие, 1 тон хлопающий Шума нет или реже систолический шум во втором межреберье слева, а также в пятом межреберье слева Наклонность к брадикардии По типу тахипноэ 3-5 см Тахи- и диспноэ 5-10 см, асцит Часто, значительный Резко расширены преимущественно влево Чаще приглушены Систолический шум недостаточности митрального клапана Электрокардиографические Вольтаж Нарушение ритма Атриовентрикулярная проводимость Высокий или низкий Редко Часто Нормальная, реже ускорена или замедлена Внутрижелудочковая проНормальная, несколько замедлеводимость на Блокады ветвей п.Гиса Возможны в 25% случаев <α QRS Отклонена влево Перегрузка предсердий Умеренная Увеличение желудочков Преимущественно левого Зубец ТV5,6 Отрицательный или положительный Сегмент S ТV5,6 Изоэлектричный, реже смещен ниже изолинии Легочный рисунок Форма сердца Рентгенологические Умеренно усилен по венозному руслу Митральная, аортальная Высокий трапециевидная, Замедлена Значительно замедлена Часто (более 50% случаев) Отклонена влево или вправо Значительная, особенно левого Обоих или больше правого Чаще положительный Часто и значительно смещен ниже изолинии Резко усилен по венозному и артериальному руслу Как при митральном или аортальном стенозе Увеличение отделов сердЛевое и правое предсердия, праЛевый желудочек и левое предца вый желудочек, левый – небольсердие, меньше правые отделы шой Амплитуда пульсации леПовышена, нормальная, реже Снижена вого желудочка снижена План обследования при подозрении на НК: общий анализ крови, анализ крови на протеинограмму, СРБ, серомукоид, КФК, КФК-МВ, ЛДГ, ЛДГ1, тропонин, иммунограмма, электролиты, вирусологическое и серологическое исследования, ЭКГ, ЭХОКГ, рентгенография сердца. В последние годы используют сцинтиграфию миокарда и пункционную биопсию с последующей оценкой персистенции вируса. Кардиомиопатии Согласно определению комитета экспертов ВОЗ (1963), «Кардиомиопатии - заболевания миокарда неизвестной этиологии, проявляющиеся кардиомегалией и сердечной недостаточностью, если при этом исключено поражение клапанов сердца, коронарных, легочных сосудов, артериальная гипертензия». По классификации 1995г. Различают КМП: дилатационная, гипертрофическая, рестриктивная, специфическая - метаболическая, воспалительная, ишемическая), аритмогенная кардиомиопатия (дисплазия) ПЖ, неклассифицируемая (фиброэластоз и др.). ГКМП характеризуется гипертрофией стенок левого желудочка (изредка и правого) без расширения его полости с нарушением диастолической функции. Подразделяют симметричную (одинаково выраженная гипертрофия миокарда всех стенок левого желудочка) и асимметричную с градиентом давления левого желудочка и аорты и без градиента. Заболевание чаще наблюдается у лиц мужского пола. К этиологическим факторам относятся генетические (в 60% случаев), тератогенные. инфекционные, стрессорные, митохондриальные. У детей первыми симптомами являются систолический шум, выявляемый или случайно или в связи с жалобами на боль в области сердца одышка при нагрузке, приступы потери сознания, головокружение, быстрая утомляемость. Помощь в диагностике оказывают инструментальные методы исследования: ЭКГ, ЭХОКГ, рентгенография. Рис.3. ЭХОКГ при ГКМП. Выраженная гипертрофиия МЖП (указано стрелкой) На ЭКГ регистрируют признаки гипертрофии ЛЖ, ишемии миокарда, возможно признаки инфаркта миокарда, возможны различные нарушения ритма и проводимости. На рис.4. представлена ЭКГ ребенка 6 мес. с гипертрофической кардиомиопатией, «инфарктоподобными» изменениями. (QS во II, III и AVF отведениях), ишемией миокарда. В терапии применяют: β адреноблокаторы – чаще атенолол или небилет при асимметричной гипертрофии с градиентом давления или надичии других факторов риска (синкопе, экстрасистолия), антиоксиданты (цитохром, элькар), мембранопротекторы. Возможно использование антагонистов Са и ингибиторов АПФ. Сердечные гликозиды не показаны при ГКПМ, кардиотрофики, мочегонные, ингибиторы АПФ Рис. 4 назначают с осторожностью. Радикальным методом является хирургический. ДКПМ характеризуется диффузным поражением миокарда с дилатацией полостей сердца и резким снижением его сократительной функции. Это полиэтиологическое заболевание, выделяют следующие ведущие этиопатогенетические концепции: вирусно-иммунологическую, миокардиальную, метаболическую (селендефицитную, тауриндефицитную, карнитиндефицитную). В 30% ДКПМ имеет наследственную природу. Клиника определяется главным образом тяжестью сердечной недостаточности вследствие значительного снижения сократимости миокарда. Начало заболевания мало - или бессимптомное. Первым признаком могут быть нарушения ритма и тромбэмболии. На поздних сроках больные жалуются на быструю утомляемость, одышку, боли в области сердца, сердцебиение, отеки, синкопальные состояния, боли в животе. При аускультации наиболее часто наблюдаются: ослабление 1 тона, ритм галопа и систолический шум относительной недостаточности митрального и/или трикуспидального клапанов. Основными методами диагностики являются инструментальные, прежде всего, ЭХОКГ. Терапия направлена на улучшение инотропной функции сердца и уменьшение его гемодинамической перегрузки: сердечные гликозиды, диуретики, периферические вазодилататоры, используют нестероидные противовоспалительные препараты, метаболические средства, антиоксиданты, препараты калия, магния, селена, карнитина хлорид, кудесан (коэнзим Q10). РКМП встречается преимущественно Рис.5. ЭХОКГ при ДКМП. Резкая дилатация в странах с тропическим климатом. полости (указано стрелками) В основе лежит ригидный, плохо растяжимый миокард, препятствующий наполнению левого желудочка. Сердце увеличено за счет левого предсердия и правых отделов, шум отсутствует или связан с недостаточностью атриовентрикулярных клапанов, часто имеются нарушения ритма. Характерный симптом - правожелудочковая недостаточность. Лечение включает противовоспалительную терапию, сердечные гликозиды, вазодилататоры. Дифференциальный диагноз НК проводят с: ВПС (неполная атриовентрикулярная коммуникация, врожденная недостаточность митрального клапана, аномалия Эбштейна), пороками развития коронарных сосудов (аномальное отхождение левой коронарной артерии от легочной артерии - синдром Бланда-Уайта-Гарленда), ревматизмом, аритмиями (обусловленными экстракардиальными причинами), миокардиодистрофией, пролапсом митрального клапана, опухолями сердца и средостения, постгипоксическим синдромом дезадаптации сердечнососудистой системы у новорожденных и детей раннего возраста. Лечение НК. Залогом успешного лечения является ранняя диагностика заболевания до наступления необратимых нарушений в сердечной мышце. Цели лечения: воздействие на возбудитель, устранение воспалительного процесса, повышение иммунологической реактивности больного, ликвидация или компенсация НК, устранение метаболических изменений в миокарде. Различают два этапа терапии: стационарный и поликлинический (или санаторный). Стационарный: ограничение двигательного режима, ограничение поваренной соли, жидкости (определяется суточным диурезом, степенью сердечной недостаточности ). Питание с достаточным содержанием белка, витаминов, солей калия. Этиотропная терапия: в настоящее время для лечения острого вирусного миокардита целесообразно применение внутривенного иммуноглобулина 2 г/кг/сут. – стандартные, содержащие преимущественно антитела класса IqG (интраглобин, октагам, иммуноглобулин нормальный человеческий и др.), обогащенные Iq М (пентаглобин), гипериммунные (цитотект – нейтрализует цитомегаловирусы, а также содержит нейтрализующие антитела к вирусам герпеса). -При герпетической этиологии кардитов доказана эффективность интерферона. В острую фазу может применяться рибавирин. -Антибактериальная терапия проводится с учетом чувствительности возбудителя, а также для профилактики осложнений у детей раннего возраста (особенно при назначении гормонов). -Специфическая терапия показана при установленной этиологии заболевания, так при токсоплазмозных НК лечение хлоридином и сульфаниламидами, при микоплазменных - эритромицином. Широким спектром действия обладает сумамед. -Терапия, направленная на коррекцию системы интерферона (особенно в период новорожденности, в т.ч. и у недоношенных) – виферон. Патогенетическая терапия: -нестероидные противовоспалительные средства (НПВС): препарат выбора - диклофенак 1-3 мг/кг в сутки, возможно применение индометацина, нимесулида, ибупрофена. -глюкокортикостероиды 1-1,5 мг/кг 3-4 недели с постепенным снижением дозы. Показания к их назначению:1) диффузный процесс с СН, 2) подострое начало заболевания как предвестник хронизации процесса, 3) кардит с преимущественным поражением проводящей системы сердца. При сердечной недостаточности: сердечные гликозиды (дигоксин), мочегонные (фуросемид, верошпирон), при хронической СН используют ингибиторы АПФ (капотен, эналаприл). Расчет дигоксина при миокардитах Возраст Доза насыщения мг/кг Поддерживающая доза 1 день-1 месяц 0,03 1/4-1/5 дозы насыщения в сутки 1-36 месяцев 0,04-0,05 1/4-1/6 дозы насыщения в сутки старше 3 лет 0,02-0,04 1/5-1/7 дозы насыщения в сутки Есть сведения о положительном эффекте парентеральных метаболических препаратов в комплексной терапии сердечной недостаточности при инфекционных повреждениях миокарда: неотона (фосфокреатина), реамберина (1,5% полиионный раствор с янтарной кислотой с выраженным антигипоксическим, антиоксидантным, антитоксическим и умеренным диуретическим действием), цитофлавина (янтарная кислота, рибоксин, никотинамид, рибофлавина мононуклеотид), калия и магния аспарагинат инфузионный раствор. -антигистаминные препараты -препараты метаболического, кардиотрофического действия – поляризующая смесь, кокарбоксилаза, пиридоксин, карнитин (элькар), цитохром С, препараты калия, магния, пангамат кальция (витамин В15), пантотенат кальция (В5), рибофлавин, актовегин, солкосерил -антиоксиданты – витамин С, Е, А, триовит, рибоксин, антигипоксанты - мексидол., они способствуют улучшению энергообмена, активизации цепи дыхательных ферментов в митохондриях, назначаются чередуя. -при нарушении ритма – антиаритмические препараты При хронизации процесса применяются препараты аминохинолинового ряда (делагил, плаквенил). -При ХК – антикининовые препараты – продектин, пармидин, контрикал. -При затяжном гипореактивном течении инфекционно-воспалительного заболевания целесообразно применять стимуляторы моноцитарно-макрофагальной системы - ликопид. Назначают детям не ранее 14 дня жизни в составе комплексной этиотропной и посиндромной патогенетической терапии в дозе новорожденным 0,5 мг 2 раза в день 7-10 дней. Возможно сочетанное применение ликопида с вифероном и иммуноглобулином. Диспансеризация. Наблюдение кардиоревматолога и педиатра. Перенесшие острый и подострый НК находятся на учете 5 лет, ХК – до передачи во взрослую сеть. Прививки при остром НК можно проводить через 5 лет наблюдения при полном отсутствии клиникоинструментальных признаков заболевания. При ХК прививки противопоказаны, также вакцинация абсолютно противопоказана при аллергической, лекарственной, сывороточной этиологии НК. Таблица 12 Схема диспансерного наблюдения 1-й год наблюдения Последующие годы наблюдения Осмотр педиатра 1раз в 2 мес. первые 6 мес., затем 1 раз в 3 мес. 2 раза в год Кардиоревматолог 1 раз в мес. первые 3 мес., затем 1 раз в 3 мес. 3 раза в год и по показаниям ЛОР, стоматолог 2 раза в год Ан. крови, мочи, общ. 2 раза в год и по показаниям 2 раза в год 2 раза в год Биохим. анализ крови 2 раза в год и после перенесенной инфекции По показаниям ЭКГ ЭХОКГ Рентгенография 1 раз в 3 1 раз в 4 По помес. и по мес. и по казанипоказапоказаям ниям ниям 2 раза в год 1 раз в год и по показаниям По показаниям Профилактика. Первичная: - оздоровление женщин до и в период беременности - оздоровление, закаливание, полноценное питание детей - санация хронических очагов инфекции Вторичная: реабилитационные мероприятия – курсы кардиотрофиков, адаптогенов, витамины, ЛФК, весной и осенью курсы НПВС 3-4 недели. Реабилитационная терапия проводится на первом году наблюдения 4 раза, в последующие – 2-3 раза в год. Вопросы для тестового контроля № п/п 1 2 3 4 5 6 7 8 9 10 Содержание вопросов Для острых приобретенных кардитов характерно: а)сердечный горб, б)ослабление верхушечного толчка, в)одышка, г)кардиосклероз, д)все перечисленное Для ранних врожденных кардитов на ЭКГ характерно перечисленное кроме: а)глубокий Q в II, III aVF, б)высокий вольтаж QRS, в)низкий вольтаж QRS , г)ригидный частый ритм, д)ишемические ST-T Для лечения ДКМП используют препараты: а) дигоксин, б) кардиотрофики, в)ингибиторы АПФ, г) антиоксиданты, д) все перечисленное Для аускультативной картины острых приобретенных кардитов характерно: а)приглушенность I тона, б)грубый систолический шум, в)тахикардия, г)экстрасистолия, д)полная АВ блокада Рабочая классификация неревматических кардитов у детей включает перечисленное, кроме: а)этиологический фактор, б)период возникновения, в)тяжесть, г)течение, д)активность процесса Для поздних врожденных кардитов характерно перечисленное, кроме: а)потливость, б)одышка, в)фиброэластоз эндокарда, г)расширение границ сердца, д)громкие тоны Острое течение кардита: а)1 месяц, б)12 месяцев, в)2-3 месяца, г)18 месяцев, д) 2 недели Критические месяцы внутриутробного развития для возникновения ранних врожденных кардитов: а)первые 3 недели, б)4-7 месяцев, в)8-9 месяцев, г)первые 10-14 дней, д)первые 1-2 месяца При хроническом кардите решающую роль в исходе заболевания играют: а)возбудитель, б)аутоиммунные нарушения, в)переохлаждение, г)реинфекция, д) все перечисленное В лечении ГКМП не используют: а) цитохром, б) дигоксин, в) атенолол, г) элькар, д) антибиотики Эталоны ответов б, в в д а, в д в, д в б б б, д Ситуационные задачи № п/п 1 2 Содержание задач К Жене К., 1 года 6 месяцев был вызван участковый врач, диагностировавший у больного ОРВИ. На 5-й день амбулаторного лечения ночью состояние больного резко ухудшилось: стал беспокойным, появилась одышка, влажный кашель, цианоз губ, что явилось причиной госпитализации больного. При осмотре ребенок возбужден, плечи несколько приподняты, кожные покровы бледные, периорбитальные отеки, периоральный цианоз и цианоз губ. Одышка смешанного характера, частота дыхания 56 в минуту, в легких выслушиваются сухие свистящие и единичные влажные хрипы. Верхушечный толчок ослаблен, смещен влево, границы относительной сердечной тупости смещены влево на 2 см. Аускультативно тоны сердца: 1 на верхушке глухой, акцент 2 тона во 2-м межреберье слева. Тахикардия стойкая до 180 в минуту. Живот мягкий, печень +2,0 из-под края реберной дуги. Диурез не нарушен. На рентгенограмме – обогащение легочного рисунка, увеличение тени сердца за счет левого желудочка. ЭКГ: синусовая тахикардия, диффузные изменения миокарда. Снижение вольтажа QRS на ЭКГ, Нb – 130 г/л, лейкоциты – 9х109/л, СОЭ – 10 мм/ч Вопросы:1.Поставить диагноз. Обосновать диагноз. 3.Тактика участкового врача: что делать? 4. Назначить лечение. У мальчика 3 мес. с массой 4200 г после проведения профилактической прививки появились приступы упорного влажного кашля, пенистая мокрота. Насморка нет, зев бледный. Ребенок вялый, капризный, отказывается от еды. При осмотре состояние тяжелое, выражена одышка с участием вспомогательной мускулатуры; периферический цианоз при беспокойстве. Над легкими ясный легочный звук. ЧД 68 в мин., обильные влажные хрипы на фоне ослабленного дыхания. Перкуторно границы сердца: правая:на 0,5 см кнаружи от правой парастернальной линии, левая: по передней подмышечной линии. Тоны сердца приглушены, акцент 2 тона над легочной артерией, ЧСС 164 в мин., печень +1,5 см. На ЭКГ – тахиаритмия синусовая, увеличение R в V5, 6. Из анамнеза: на 34 неделе беременности мать перенесла грипп. Масса ребенка при рождении 3200 г, длина 50 см. У ребенка отмечали утомляемость и одышку при кормлении, потливость,бледность. Вопросы.1.Предполагаемый диагноз. Укажите осложнения основного заболевания. 2.Ваша тактика. Лечение. 3.Проведите дифференциальный диагноз с другими заболеваниями Эталоны ответов 1.Диагноз: приобретенный острый кардит вирусной этиологии, осложненный острой сердечной левожелудочковой недостаточностью 2А степени. Диагноз кардита поставлен на основании анамнеза /развитие заболевания в ходе острой вирусной инфекции/. Данных объективного исследования – расширения границ сердца влево, приглушенности тонов, ослабления верхушечного толчка, одышки смешанного характера, хрипы в легких, данных инструментальнолабораторного исследования (синусовая тахикардия, диффузные изменения миокардита левого желудочка на ЭКГ, усиление легочного рисунка на рентгенограмме). 2. Строгий постельный режим, оксигенотерапия /увлажненный кислород/, доступ к вене: лазикс 2-4 мг/кг (т.е. 24-48 мг), строфантин 0,01-0,02 мг/кг/сут в 3-4 введения (0,05-0,1 мл раз. доза), лечение вирусной инфекции, глюкокортикоиды /преднизолон 1 мг/кг, антибиотики на период терапии, гормонами, для улучшения сократительной функции миокарда – допамин в/в капельно 3-6 мкг/кг в минуту под присмотром АД и ЧСС, и) мероприятия по коррекции метаболических нарушений миокарда: поляризующая смесь, кокарбоксилаза, рибоксин, вит С. 1.Поздний врожденный кардит. Острая левожелудочковая недостаточность – отек легких. 2.Срочная госпитализация в реанимационное отделение. Оксигенотерапия увлажненным О2, доступ к вене: лазикс 2-4 мг/кг, допамин 3-6 мкг/кг в минуту, нанипрусс 2-5 мкг/кг в минуту, глюкокортикоиды (преднизолон 1 мг/кг), антибиотики, коррекция метаболических нарушений (кокарбоксилаза, аскорбиновая кислота, рибоксин) 3.а) ранний врожденный кардит: характерно воздействие повреждающего фактора на 4-7 месяце беременности, низкая масса тела при рождении, выраженная кардиомегалия, сердечный горб, б) приобретенный кардит, наличие с рождения утомляемости, одышки при кормлении, потливости, бледности, в) врожденные пороки сердца, отсутствие значимого патологического воздействия в 1-2 триместрах беременности, органического шума в сердце. Рекомендуемая литература. Основная: 1. Шабалов Н.П. Детские болезни. Изд-е 5-е. В двух томах. Т. 2., Ст.-Пб: Питер, 2006.-731 с. 2. Детская ревматология. Руководство для врачей. // Под редакцией А.А.Баранова и Л.К.Баженовой. М.Медицина, 2002.-336 с. Дополнительная: 1. Котлукова Н.П. Дифференциальная диагностика поражений миокарда у детей первого года жизни. В кн. «Физиологи и патология сердечно-сосудистой системы у детей первого года жизни». Под ред. Школьниковой М.А., Кравцовой Л.А., Москва, 2002., С113-124. 2. Леонтьева И.В. Лекции по кардиологии детского возраста. Москва, 2005, С.275-326. 3. Мутафьян О.А. Кардиты у детей и подростков (клиника, диагностика и лечение), СанктПетербург, 2006, С.56-126. 4. Черкасов Н.С. Заболевания сердца у новорожденных и детей раннего возраста, Ростов - на Дону, 2006, 190 с. 5. Практическое руководство по детским болезням. Под общей редакцией проф. В.Ф. Коколиной и проф. А.Г.Румянцева. Том III. Кардиология и ревматология детского возраста. Под ред. Г.А. Самсыгиной и М.Ю. Щербаковой. Медпрактика - М, Москва, 2004, 125-223с. Занятие № 6. ПИЕЛОНЕФРИТ У ДЕТЕЙ Цель занятия: изучить этиологию, патогенез, клинические проявления и лечение пиелонефрита, его особенности в зависимости от формы заболевания и возраста ребенка, научиться дифференцировать пиелонефрит с другими болезнями органов мочевой системы. Вопросы для самоподготовки: 1.Этиология, эпидемиология и патогенез пиелонефрита. 2.Клинические проявления пиелонефрита и его особенности в зависимости от возбудителя и формы заболевания. 3.Особенности пиелонефрита у детей в зависимости от возраста. 4.Диагностика и дифференциальная диагностика пиелонефрита. 5.Лечение и диспансерное наблюдение за больными пиелонефритом. Пиелонефрит – неспецифическое инфекционно-воспалительное очаговое заболевание, протекающее с преимущественным поражением чашечно-лоханочной системы и тубулоинтерстициальной ткани почек. Практически во всем мире пиелонефрит оценивается как самое частое заболевание почек и как второе по частоте заболевание детского возраста (после ОРВИ). Распространенность пиелонефрита составляет от 33,3 до 186 на 100 000 детского населения. У детей отмечается наличие возрастных и половых различий в частоте встречаемости пиелонефрита. Считается, что в грудном возрасте заболевает столько же детей, сколько в последующие 14 лет жизни вместе взятые. Заболеваемость на 2-м году жизни понижается, а затем снова возрастает на 3-м году, уменьшаясь к 6-му году, а затем наблюдается некоторое повышение. На первом году жизни заболевание встречается с одинаковой частотой у мальчиков и девочек. В дальнейшем отмечается увеличение частоты пиелонефрита у девочек, что в значительной степени связано с особенностями строения мочевых путей и особенностями гормонального фона. Этиология. Возбудителем пиелонефрита в большинстве случаев является грамотрицательная флора с преобладанием вирулентных штаммов кишечной палочки. Достаточно часто из мочи высеваются: клебсиелла, протей, энтерококки, грибы рода Candida, стафилококки и стрептококки, причем последние два чаще определяются у детей раннего возраста. Роль вирусов до настоящего времени дискутируется. В последние годы возрастает роль непатогенной и условно-патогенной флоры, что связано с бесконтрольным применением антибиотиков. Большое значение в развитии пиелонефрита имеет так называемый феномен «бактериальной адгезии»: большинство грамотрицательных бактерий имеют «реснички» белковой природы (Р - фимбрии), рецепторами для которых являются структуры мембран клеток мочевых путей. Наличие фимбрий позволяет бактериям прикрепляться к клеткам мочевых пу- тей. Данный феномен облегчает проявление вирулентности бактерий, которая связана с наличием у них капсулярных (К-) и эндоплазматических (О-) антигенов. Для реализации микробного воспаления в почечной ткани необходимо наличие факторов «риска» и условий развития пиелонефрита. Наиболее значимыми факторами «риска» являются: наследственная предрасположенность, неблагоприятная экологическая ситуация, частые ОРВИ, патология беременности, отягощенный аллергологический анамнез. К условиям развития пиелонефрита следует отнести нарушение оттока мочи (органическое или функциональное), бактериологическое обсеменение почек, изменение реактивности почечной ткани, изменение общего состояния организма. Условиями хронизации пиелонефрита у детей являются: недостаточная фагоцитарная активность лейкоцитов, незавершенный фагоцитоз, сниженный уровень В-лимфоцитов в крови. Патогенез. Бактериальная инвазия при пиелонефрите происходит гематогенным (характерен для детей раннего возраста и мальчиков) и уриногенным - восходящим (более характерен для девочек и детей старшего возраста) путем. Роль лимфогенного пути проникновения инфекции в почку в настоящее время большинством авторов отвергается. Основой для развития пиелонефрита является расстройство уродинамики, так как какими бы факторами патогенности не обладали микроорганизмы, им нужно время (нарушение оттока мочи), чтобы проявить всю свою агрессивность. Нарушение уродинамики наиболее часто возникает на фоне: аномалий развития мочевыводящих путей (сужение мочеточников, перегиб мочеточников при нефроптозе, сдавление мочеточников добавочными сосудами, пузырно-мочеточниковый рефлюкс и др.); мочекаменной болезни; расстройства уродинамики функционального генеза на фоне дисфункции мочевого пузыря. Способствуют развитию ПН метаболические нарушения-кристаллы солей (метаболитов), выделяясь в большом количестве, могут вызвать микрообструкцию, что приводит к развитию интерстициального нефрита, а затем при наслоении инфекции - ПН. При восходящем пути распространения инфекции, вследствие турбулентного течения или ПМР, происходит транспорт микроорганизмов и их адгезия на уроэпителии верхних отделов мочевыводящих путей. Р - фимбрии, вызывая уретрит и блокаду проведения нервных импульсов, способствуют нарушению кинетики мочевыводящих путей, развитию функциональной обструкции. Вследствие нарушения уродинамики происходит повышение внутрилоханочного и внутримочеточникового давления, приводящее к обструктивным изменениям чашечно-лоханочной системы, почечных сосочков и возникновению пиело-тубулярного рефлюкса (схема 1). Схема 1. Патогенез пиелонефрита Микроорганизм Р-фимбрии О-Антиген К-Антиген Адгезия к уротелию Динамическая обструкция мочеточника Продвижение по стенке мочеточника Пиеловенозный рефлюкс Противодействие опсонизации и фагоцитозу Проникновение в почку Пиелонефрит Воспалительный ответ Клеточная инфильтрация Иммунный ответ Освобождение лизосомальных ферментов Фагоцитоз Организм Гидролитические ферменты, лизоцим и др. Неспецифические факторы зашиты Таблица 13 Классификация пиелонефрита у детей (1980). Форма пиелонефрита Первичный Вторичный (обструктивный) Течение Острое Хроническое Рецидивирующее Латентное Активность Активная стадия Частичная клиниколабораторная ремиссия Полная клиниколабораторная ремиссия Функции почек Без нарушения С нарушением функций -канальцевых -клубочковых -смешанного типа ХПН Первичный пиелонефрит – это микробно-воспалительный процесс в почечной паренхиме, когда при использовании современных методов обследования не удается выявить отчетливых причин, способствующих фиксации микроорганизма в тубулоинтерстициальной ткани почек. Вторичный (обструктивный) пиелонефрит – это микробно-воспалительный процесс в почечной ткани, который развивается на фоне уже имеющейся патологии в мочевыводящей системе. Обструктивный пиелонефрит развивается на фоне органической или функциональной обструкции. В клинической картине пиелонефрита выделяют следующие синдромы: а) интоксикационный, б) болевой, в) синдром дизурических расстройств, г) мочевой При остром пиелонефрите преобладает интоксикационный синдром и выраженность клиники зависит от возраста ребенка: а) дети первого года жизни - пиелонефрит чаще протекает под маской кишечной инфекции; в клинике преобладают токсикоз, дегидратация, понос, может появляться менингиальный синдром, желтушность кожи и склер; б) дети от одного до трех лет - пиелонефрит часто развивается после какого-либо другого инфекционного процесса - ОРВИ, пневмонии, кишечной инфекции и т.д.; в клинике преобладают интоксикационный синдром и диспептические расстройства; в) дети дошкольного и школьного возраста - клиника может быть менее яркой, на первом плане – интоксикационный синдром. Хронический ПН диагностируется при сохранении признаков заболевания более 6 месяцев от ее начала или наличия за этот период не менее двух рецидивов. Особенности хронического пиелонефрита: 1. Чаще протекает латентно и выявляется случайно или при профилактическом осмотре. 2. Клиника зависит от активности процесса, распространенности воспалительных очагов в почках и формы пиелонефрита: а) в клинике первичного пиелонефрита преобладает интоксикационный синдром; б) в клинике вторичного - болевой синдром и дизурические явления. Характеристика мочевого синдрома при пиелонефрите: характер мочевого синдрома зависит от формы пиелонефрита. Для первичного пиелонефрита характерны лейкоцитурия, бактериурия, может быть умеренная цилиндрурия, незначительная или умеренная протеинурия (не более 1г/сут) и незначительная гематурия. Для вторичного пиелонефрита характерны лейкоцит- и эритроцитурия, бактериурия, может быть небольшая протеинурия и умеренная цилиндрурия. Диагностика и план обследования. С целью диагностики пиелонефрита применяют обязательные и дополнительные методы исследования. Обязательные применяются ко всем больным, дополнительные - по специальным показаниям. Кратность диагностических исследований определяется индивидуально. Обязательные лабораторные исследования для выявления активности микробновоспалительного процесса Диагностические процедуры Кратность обследования Клинический анализ крови - период максимальной активности 1 раз в 6-10 дней - период стихания 1 раз в 2 недели - период ремиссии 1 раз в 6-12 месяцев - при интеркуррентных заболеваниях однократно Биохимический анализ крови (общий белок, белковые фракции, мочевина, фибриноген, СРБ) - период максимальной активности 1 раз в 2 недели - период стихания 1 раз в 2-4 недели - период ремиссии 1 раз в 6-12 месяцев Общий анализ мочи -период максимальной активности 1 раз в 3-5 дней - период стихания 1 раз в 7-14дней - период ремиссии 1 раз в 3 месяца Количественные анализы мочи (по Нечипоренко. Амбурже и др.) - период максимальной активности 1 раз в 2 недели - период стихания 1 раз в месяц -период ремиссии 1 раз в 6-12 месяцев -при интеркуррентных заболеваниях однократно Посев мочи на флору - до назначения этиотропного лечения однократно - через 4 недели лечения однократно Дополнительные методы исследования для подтверждения активности микробновоспалительного процесса: 1).Исследование крови на содержание R-белков, средних молекул. 2).При затяжном течении инфекции мочевой системы, отсутствии эффекта от традиционной терапии, отягощенном семейном анамнезе, подозрении на микст-инфекцию проводятся исследования мочи на: хламидии, микоплазмы, уреаплазмы, грибы, вирусы, микобактерии туберкулеза 3).У детей с гипоиммунными состояниями - исследование иммунного статуса (уровень секреторного IgА, состояние фагоцитоза). Обязательные лабораторные исследования для характеристики функционального состояния почек: уровень креатинина, мочевины в крови, проба Зимницкого, клиренс эндогенного креатинина, исследование рН, титруемой кислотности, контроль диуреза. Дополнительные лабораторные исследования для уточнения функционального состояния почек: осмоляльность мочи; ферменты мочи, проба с хлористым аммонием; проба Зимницкого с сухоедением. Обязательные инструментальные исследования: измерение артериального давления, ультразвуковое исследование органов мочевой системы, микционная цистография, экскреторная урография. Дифференциальная диагностика. Пиелонефрит следует дифференцировать с циститом (встречается часто у девочек, протекает без интоксикации, с нормальной температурой тела, часто отмечаются дизурические расстройства, дневное и ночное недержание мочи, боли в надлобковой области, промежности во время или в конце акта мочеиспускания); абактериальным интерстициальным нефритом (в генезе имеют значение токсико-аллергическое поражение почек, отравления, ожоги, воздействие лекарственных препаратов, характеризуется гипостенурией, умеренной протеинурией и гематурией, лейкоцитурией лимфомоноцитарного типа); туберкулезом почек (в клинике преобладают астенический синдром, повышение температуры тела субфебрильного характера, в ан. мочи лейкоцитурия при малой бактериальной обсемененности, может отмечаться гематурия, решающая роль в дифференциальной диагностике принадлежит посеву мочи на ВК и туберкулиновым пробам). Лечение пиелонефрита зависит от формы заболевания и клинических проявлений. Лечебные мероприятия направлены на ликвидацию или уменьшение микробновоспалительного процесса в почечной ткани, нормализацию обменных нарушений и функционального состояния почек, на стимуляцию регенераторных процессов, повышение иммунологической реактивности организма, предупреждение развития склероза в интерстициальной ткани почек. Режим - постельный, полупостельный (на период выраженной активности микробновоспалительного процесса). Диетотерапия при пиелонефрите в активной фазе: - ограничение поступления продуктов, содержащих белок и экстрактивные вещества; -исключение или ограничение продуктов, для метаболизма которых требуются большие энергетические затраты; - ограничение продуктов, содержащих избыток натрия. При остром пиелонефрите и обострении хронического на 7-10 дней применяется молочно-растительная диета с умеренным ограничением белка (1,5-2,0 г на кг массы), соли (до 2-3 г в сутки). Рекомендуется достаточное питье, на 50% больше возрастной нормы в виде "некрепкого" чая, компотов, соков. По мере уменьшения активности воспалительного процесса переводят на 5 стол, после лабораторной ремиссии в течение 6 месяцев, можно - на 15 стол с ограничением специй, копченостей, маринадов. При ПН на фоне дисметаболических нарушений проводится коррекция диеты в зависимости от экскреции вида солей. Рекомендуется прием слабощелочных минеральных вод (типа Славяновской, Смирновской) из расчета 2-3 мл/кг массы на прием в течение 20 дней, 2 курса в год. Антимикробная терапия проводится с учетом нефротоксичности препарата и чувствительности возбудителя, длительность ее не менее 6 недель. В острый период предпочтение отдается защищенным пенициллинам или цефалоспоринам не ниже второго поколения. В отношении грамотрицательных бактерий более эффективны аминогликозиды (гарамицин, гентамицин) и цефалоспорины (цепорин, цефамизин, цефалексин, цефиксим). При легком течении инфекции мочевой системы может быть использован оральный путь введения антибиотика в виде специальных детских форм антибиотиков (сиропа, суспензии), которые отличаются хорошей всасываемостью из желудочно-кишечного тракта, приятными вкусовыми качествами. Парентеральный путь введения антибиотика используется при тяжелом и среднетяжелом течении пиелонефрита с последующим переводом на пероральный путь. В настоящее время широко используется «ступенчатая» терапия пиелонефрита: в первые 3 дня заболевания используется препарат для парентерального введения, затем этот же препарат в течение 7 дней – через рот. По мере стихания процесса переходят на препараты нитрофуранового ряда, налидиксовой кислоты и другие антимикробные средства (фурагин, неграм, 5- НОК, нитроксолин, грамурин, бактрим, палин и др.). При первичном пиелонефрите непрерывный курс антимикробной терапии составляет 4-6 недель, затем проводится поддерживающая терапия в течение 3 месяцев. При вторичном пиелонефрите непрерывный курс антимикробной терапии составляет 6-8 недель, поддерживающее лечение проводятся 6-12 месяцев. Назначаются десенсибилизирующие средства коротким курсом - 7-10 дней (тавегил, супрастин, фенкарол). При ярко выраженных симптомах интоксикации с целью дезинтоксикации применяют внутривенное капельное введение 10% раствора глюкозы, физраствора. Для улучшения иммунологической реактивности используют: метилурацил на 3-4 недели, левамизол по 3 дня в неделю 2-4 курса. Для улучшения обменных процессов применяются: поливитамины, ККБ, эссенциале, ксидифон, димефосфон, препараты Q10, липоевая кислота по 3-4 недели 2 раза в год. В острый период заболевания показан курс УВЧ-терапии - 4-5 процедур, с последующим переходом на СВЧ-терапию - 5-8 процедур. В период стихания процесса применяется УЗ на область почек. Лечение обструктивного пиелонефрита проводится совместно с детским урологом. Выбирая антибактериальные препараты для детей с обструктивным пиелонефритом, необходимо учитывать состояние функции почек и нефротоксичность антибиотиков. У больных с незначительным снижением клубочковой фильтрации дозы "защищенных" пенициллинов, цефалоспоринов могут не подвергаться корректировке. При снижении клубочковой фильтрации более чем на 50% по пробе Реберга дозы этих препаратов должны быть уменьшены на 25-75%. При выраженной активности обструктивного пиелонефрита с проявлениями синдрома эндогенной интоксикации наряду с этиотропным лечением важное значение имеет инфузионно - корригирующая терапия и нормализация уродинамики. С этой целью на несколько дней (2-4) катетеризируется мочевой пузырь. Показано назначение препаратов, улучшающих почечную гемодинамику (эуфиллин). При отсутствии острой задержки мочи возможно проведение "почечного дренажа" (назначается в утренние часы водная нагрузка в соответствии с возрастом и через 1 час фуросемид из расчета 1 мг/кг массы тела в сочетании с препаратами калия). При выявлении артериальной гипертензии решается вопрос о назначении гипотензивных препаратов. Фитотерапия назначается в период ремиссии. Рекомендуются травы, обладающие противовоспалительным (брусничный лист, листья василька полевого, кора дуба, крапива двудомная), антисептическим (плоды и листья брусники, зверобой, календула),регенерирующим действием (брусничный лист, крапива двудомная, ячмень обыкновенный). Диспансеризация. Частота осмотров специалистами: детей с острым ПН педиатр 1-й год осматривает 1 раз в месяц(первое полугодие), затем-1 раз в 2 месяца; 2-й год-1 раз в 3 месяца, затем- 1 раз в 3-6 мес.; с хроническим ПН- 1-й год- 1 раз в 1 мес.; 2-й год- 1 раз в 2 мес., затем-1 раз в 3 мес. Нефролог при хроническом ПН 1-й год осматривает 1 раз в 3 мес., 2-й год-1 раз в 6 мес., затем 1 раз в год. На диспансерном учете дети с острым пиелонефритом находятся 3 года (снятие с учета после комплексного обследования в нефрологическом стационаре и при условии полной клинико-лабораторной ремиссии в течение 3-х лет), с хроническим ПН - до передачи во взрослую сеть. Вопросы для тестового контроля № п/п 1 2 3 4 5 6 7 8 9 10 Содержание вопросов Пиелонефрит по течению подразделяется на: а) острый, б) хронический, в) затяжной, г) латентный, д) волнообразный При подозрении на пиелонефрит в план обследования необходимо включить следующие исследования: а) анализ мочи на дифференцированные клетки, б) анализ мочи на сахар, в) анализ мочи на кетоновые тела, г) анализ мочи по Зимницкому, д) анализ мочи на бактериурию При пиелонефрите чаще высевается из мочи: а) клебсиелла, б) кишечная палочка, в) стрептококк, г) протей, д) сальмонелла Ведущие звенья патогенеза пиелонефрита: а) нарушение кровообращения, б) нарушение оттока мочи; в) снижение общей резистентности к инфекции, г) наличие почечного дизэмбриогенеза, д) образование аутоантител Хронический пиелонефрит диагностируется при сохранении признаков болезни в течении: а) 2 мес., б) 3 мес., в) 4 мес., г) 6 месяцев и более, д) 1 год Для пиелонефрита не характерно: а) бактериурия. б) лейкоцитурия, в) деформация ЧЛС, г) гипостенурия, д) олигурия Для детей раннего возраста при остром пиелонефрите характерно наличие следующих синдромов: а) болевого, б) геморрагического, в) астенического, г) диарейного, д) менингиального Для лечения пиелонефрита у детей раннего возраста не применяют: а) пенициллины, б) макролиды, в) нитрофурановые препараты, г) нитроксолин, д) стрептомицин Вторичным будет пиелонефрит, возникший: а) на фоне другого заболевания, б) после другого заболевания, в) на фоне дисметаболических нарушений, г) на фоне врожденной патологии, д) после кишечных инфекций При кислой реакции мочи усиливается действие: а) пенициллина, б) полусинтетических пенициллинов, в) эритромицина, г) невиграмона, д) линкомицина Эталоны ответов а, б, г а, г, д б б, в, г г д г, д д в, г а, б, г Ситуационные задачи № п/п 1 2 Содержание задач Оля Л., 3 лет, поступила в областную детскую больницу с жалобами на повышение температуры до 3839С, боли в животе, снижение аппетита, периодически учащенное мочеиспускание. Со слов мамы, больна с конца первого года жизни, когда после перенесенной кишечной инфекции были изменения в моче. Но ребенок нигде не обследовался и не лечился. В анамнезе частые ОРВИ. При поступлении состояние средней степени тяжести. Девочка пониженного питания, кожные покровы очень бледные, под глазами "тени". Увеличены подчелюстные лимфоузлы, зубы кариозные, неровные; миндалины рыхлые, гиперемии, налетов нет. Границы сердца не расширены. Тоны ритмичные, приглушены, систолический шум на верхушке, в V точке. В легких выслушивается везикулярное дыхание, хрипов нет. Живот мягкий, печень у края реберной дуги, мочеиспускание свободное. Суточный диурез 600мл. При обследовании в общем анализе крови: эритроцитов- 3,28х1012; Hb- 102 г/л, цветной показатель0,8, лейкоцитов- 8,1х109; э-2, п-10, с-52, л-26, м-10, СОЭ-18мм/ч. Общий анализ мочи: белка нет, плотность мочи1008, лейкоцитов-13-18 в поле зрения, эритроцитов нет. Почечный эпителий-3-5 в поле зрения. Другие исследования не проводились. Вопросы: 1. Какое заболевание можно заподозрить у ребенка? 2. Какие исследования необходимо назначить, чтобы поставить правильный диагноз? 3. Назначить лечение (с учетом режима, диеты, лекарственных препаратов). Мальчик 1 года поступил для обследования с жалобами на неоднократные "немотивированные" подъемы температуры тела до 38С с 2-х месячного возраста, периодическое беспокойство при мочеиспускании, неустойчивый стул. Ребенок от первой беременности, протекавшей на фоне токсикоза первой половины. Родился в срок с массой 3000г., длиной 50 см, закричал сразу. Период новорожденности без особенностей. К году весит 9 кг. Аппетит снижен. Объективно: пониженного питания, бледный. В анализе мочи, лейкоциты покрывают все поле зрения, белок 0,099 г/л, эритроциты 3-5 в поле зрения. По УЗИ- расширение лоханки левой почки. При проведении цистографии - заброс рентгеноконтрастного вещества в расширенный левый мочеточник и левую почку с умеренной дилятацией лоханки и верхней трети мочеточника. Вопросы: 1.Ваш диагноз.2.Тактика лечения. Эталоны ответов 1.Пиелонефрит, активная фаза 2.План обследования: кровь на белковые фракции, остаточный азот, мочевину, креатинин сыворотки, серомукоид, С - реактивный белок. Исследование мочи на Нечипоренко, на бактериурию, исследование функционального состояния почек (проба Зимницкого, Реберга), в/венная урография, цистография, консультация уролога. Измерение АД. 3. Стол №5, режим свободный, витамины внутрь, антигистаминные препараты, антибактериальные препараты (защищенные пенициллины, цефалоспорины), с последующим переходом на уросептики (фурагин, нитроксолин), 1.Вторичный хронический пиелонефрит на фоне ПМР- III степени слева, активная фаза. Лечение: непрерывная антибактериальная терапия не менее 3-х месяцев –1-2 курса антибиотиков (защищенные пенициллины, цефалоспорины 3-4 поколения), затем уросептики (фурагин, нитроксолин) в полной дозе до 3-х месяцев с последующим переходом на поддерживающую терапию (однократный прием фурагина на ночь не менее 6 мес.) Курсы физиопроцедур. Препараты метаболического действия (В15, В2, В6, кокарбоксилаза, АТФ, липоевая кислота) ежеквартально в течение месяца. Контрольная цистография через 6 месяцев. При отсутствии положительной динамики–консультация уролога (для решения вопроса о необходимости оперативного лечения). Рекомендуемая литература: Основная: 1. Шабалов Н.П. Детские болезни. Изд -е 5-е. В двух томах. Т. 2., Ст.- Пб: Питер, 2006.-731 с. 2. Папаян А.В., Савенкова Н.Д. Клиническая нефрология детского возраста. С.-Пб., «Левша», 2008. – 600 с. Дополнительная: 1. Практическое руководство по детским болезням. Под общей редакцией проф. В.Ф. Коколиной и проф. А.Г.Румянцева. Том VI. Нефрология детского возраста. Под ред.С.В. Бельмера, И.М. Османова. Медпрактика - М, Москва, 2005, 712 с. 2. Баранов А.А., Сергеева Т.В. Амбулаторная нефрология. Амбулаторная педиатрия.-М.: Союз педиатров России. Том 1, 2009.-156 с. Занятие №7. ГЛОМЕРУЛОНЕФРИТ У ДЕТЕЙ Среди приобретенных заболеваний почек у детей гломерулонефрит (ГН) является вторым по распространенности после инфекции мочевыводящих путей. Вместе с тем в ряде возрастных групп ГН служит ведущей причиной развития хронической почечной недостаточности и инвалидизации больных. Среди детского населения ГН в основном болеют дети в возрасте от 7 до 12 лет, несколько чаще мальчики. Цель занятия: Изучить этиологию, патогенез, клинику, диагностику, современные принципы терапии гломерулонефрита у детей. Вопросы для самоподготовки. 1. Этиопатогенез гломерулонефрита у детей 2. Классификация гломерулонефрита 3. Клинические проявления различных вариантов гломерулонефрита 4. Диагностика гломерулонефрита у детей 5. Принципы лечения ГН у детей и диспансерное наблюдение Гломерулонефрит – это иммуновоспалительное заболевание, преимущественно клубочкового аппарата почек, а также с вовлечением канальцев и интерстициальной ткани. Этиология. ГН у детей–полиэтиологическое заболевание, которое развивается в результате взаимодействия генетических и средовых (инфекционных и неинфекционных) факторов. К инфекционным факторам относятся бактериальные инфекции, в основном стрептококковая и вирусные. Нефротропными являются вирусы: гепатита В, кори, краснухи, цитомегалии. К неинфекционным факторам, способствующим развитию ГН, относятся пищевая и лекарственная аллергия, укусы насекомых. Достаточно часто клиника ГН разворачивается после вакцинации. Патогенез. В настоящее время выделяются два основных вида иммунологических реакций в результате которых повреждается почечная ткань: -иммунокомплексный, при котором в состав ИК, фиксирующихся на территории почечных клубочков входят внеклубочковые антигены и антитела к ним. При этом механизме ИК могут образовываться в циркулирующей крови, а также на территории клубочков в результате предшествующей фиксации антигенов в них и последующей реакции с циркулирующими антителами; -аутоиммунный, при котором в качестве антигена выступает сама гломерулярная базальная мембрана. Результатом обоих механизмов является иммунное воспаление, приводящее к повреждению почечной ткани и проявляющееся активацией гуморальных систем воспаления (комплемента, свертывающей, кининовой) и привлечением в очаг повреждения в клубочках воспалительных клеток (моноцитов, нейтрофилов, тромбоцитов). Активированные клетки выделяют повреждающие факторы (активные радикалы кислорода, протеазы, цитокины), которые стимулируют пролиферацию собственных клеток почечных клубочков (мезангиальных, эндотелиальных, эпителиальных). Активированные клетки почечных клубочков одновременно с пролиферацией усиливают синтез внеклеточного матрикса. Патогенетически фи- нальным этапом иммуно - воспалительных реакций является склероз (избыточное накопление внеклеточного матрикса), прогрессирование которого поддерживается гемодинамическими и метаболическими нарушениями, что в итоге может привести к потере почечных функций и развитию хронической почечной недостаточности (схема 2). Схема 2. Патогенез гломерулонефрита Антигены Иммунная реакция Иммунные комплексы в гломеруле. Комплемент Полинуклеарные лейкоциты Сенсибилизация Т-лимфоцитов Моноциты Макрофаги Мезангиальные клетки Энзимы, простогландины, радикалы О2Изменение гломерулярной базальной мембраны: протеинурия, гематурия Пролиферация клеток почечных клубочков, усиленный синтез внеклеточного матрикса Гломерулярный и интерстициальный склероз Различают первичный ГН (собственно первичное заболевание клубочков почек, как правило, после воздействия инфекции) и вторичный (при ряде системных заболеваний) ГН. Таблица 14 Классификация гломерулонефрита (Винница,1976) Формы ГН Острый: с нефритическим синдромом с изолированным мочевым синдромом с нефротическим синдромом с нефротическим синдромом, гематурией, гипертензией Хронический: нефротическая форма смешанная форма гематурическая форма Подострый (злокачественный) Активность ГН Период начальных проявлений Период обратного развития Переход в хронический Период обострения Период частичной ремиссии Период полной клиниколабораторной ремиссии Почечные функции Без нарушения функций почек С нарушением функций почек Острая почечная недостаточность Без нарушения функций почек С нарушением функций почек Хроническая почечная недостаточность С нарушением функций почек Хроническая почечная недостаточность В соответствии с классификацией ГН при формулировке диагноза учитывается форма, активность заболевания, состояние ренальных функций (табл. 11). Острый ГН у детей, в отличие от взрослых, в 80-90% случаев заканчивается выздоровлением, 5-20% случаев наблюдается исход в хронический ГН. При циклическом течении острого ГН, т.е. исходом в полную ремиссию, выделяются периоды начальных проявлений (3-4 недели), обратного развития симптомов (6-18 мес.) и полной клинико-лабораторной ремиссии, сохранение которой в течение 5 лет и более свидетельствует о выздоровлении от этой болезни. Симптомы острого ГН, которые условно делятся на ренальные (мочевой синдром и др.) и экстраренальные (гипертензия, отеки и др.), у детей обычно проявляются через 2-3 недели после инфекционного поражения, чаще стрептококковой этиологии (-гемолитический, группы А, типы 4, 12, 49), глотки, ушей, кожи. При циклическом течении острого ГН в начальном периоде у детей могут наблюдаться 4 клинических синдрома: 1.нефритический синдром, который характеризуется умеренными отеками, гипертензией, гематурией и небольшой или умеренной (не более 1,5 г/сут.) протеинурией; 2. изолированный или асимптоматический мочевой синдром, проявляющийся гематурией и небольшой или умеренной протеинурией; 3. нефротический синдром с характерными для него распространенными отеками, гипо- и диспротеинемией, гиперлипидемией, выраженной (50мг/кг/сут и более) протеинурией; 4. нефротический синдром с гематурией и гипертензией. Помимо перечисленных синдромов лишь у отдельных детей с острым ГН нарушения гемодинамики сопровождаются отеком легких и сердечной недостаточностью. У 1/3 больных отмечается транзиторная гиперазотемия, которая сопровождается умеренным ограничением клубочковой фильтрации и функции осмотического концентрирования. При исходе острого ГН в хронический, заканчивается эволюция отдельных признаков и определяется форма затяжного (через 6 мес.) и хронического (через 1 год) ГН. Нефротическая форма хронического ГН характеризуется отеками, протеинурией (как правило, селективной) более 2,0-2,5 г/сут, гипо- и диспротеинемией. Гипертензия отсутствует, функции почек, как правило, сохранены, осадок мочи нормальный. Смешанная форма хронического ГН характеризуется сочетанием нефротического синдрома с гематурией и гипертензией. У этих больных отмечается неселективная протеинурия, в течение 1-2 лет становятся ограниченными клубочковая фильтрация и канальцевые функции без признаков почечной недостаточности. Эта форма ГН отличается резистентностью к современным методам лечения и неблагоприятным прогнозом. При гематурической форме хронического ГН наблюдается гематурия разной степени выраженности (от минимальной до макрогематурии) без или в сочетании с небольшой (до 1г/сут) протеинурией. Отеки и гипертензия отсутствуют, функции почек длительное время (годы) сохранены у большинства больных. Отдельно в классификации вынесен быстропрогрессирующий (злокачественный) ГН, характеризующийся сверхвысокой активностью ГН, прогрессирующей почечной недостаточностью. При данном варианте в иммуновоспалительный процесс захватывается вся стенка капилляров с возникновением деструкции, разрыва стенки, происходит экстравазация фибрина в просвет капсулы Боумена - Шумлянского с вовлечением в процесс и ее листков. Поэтому данный вариант ГН еще называют экстракапиллярным, т.е. выходящим за пределы капилляров клубочка. В итоге происходит формирование полулуний в более чем 50% гломерул. Быстропрогрессирующий ГН, как вариант первичного ГН, регистрируется в 3-5% случаев, чаще у детей школьного возраста, в остальных случаях он бывает вторичным, ассоциированным с различными инфекционными, системными заболеваниями, опухолями. Клинически быстропрогрессирующий ГН чаще всего характеризуется нефротическим синдромом, гематурией, анемией, стойкой артериальной гипертензией, прогрессирующей почечной недостаточностью, с исходом в хроническую почечную недостаточность. Диагностика. Ежедневно проводить учет выпитой и выделенной жидкости, измерение артериального давления и массы тела. Таблица 15 План обследования при гломерулонефрите Исследование Мазок из зева на гемолитический стрептококк Антистрептолизин - О и антистрептокиназа Выявляются Высев редко Как правилоповышены при нефритическом синдроме HbsAq при нефротическом синдроме Выявляются у 1/3 Клинический анализ крови Лейкоцитоз, нейтрофилез, повышена СОЭ Биохимический анализ крови: протеинограмма, Неспецифические признаки воспаления, при СРБ, сиаловые кислоты, холестерин, - нефротическом синдроме – гипопротеинемия, липопротеиды, мочевина, К, Na гипер 2-глобулинемия, повышение уровня холестерина, -липопротеидов, мочевина может быть Иммунограмма Jg G, C, ЦИК Протромбиновый индекс, фибриноген Анализ мочи клинический Суточная экскреция белка Уроцитограмма мочи (при лейкоцитурии) Посев мочи Клиренс эндогенного креатинина Проба Зимницкого Осмотр отоларинголога, стоматолога Осмотр окулиста (глазное дно) ЭКГ Ультразвуковая диагностика почек Протромбиновый индекс, фибриноген Протеинурия, зритроцитурия Как правило, не выше 1,0-1,5 г/сут -при нефритическом синдроме, массивная (выше 50 мг/кг/сут)-при нефротическом синдроме Мононуклеарный характер лейкоцитурии Как правило, стерильный, если не присоединилась инфекция Креатинин, клубочковая фильтрация Соотношение ДД : НД, Разница d max и d min Выявление очагов инфекции Увеличение размеров почек, более отчетливая визуализация пирамид При подозрении на аномалию развития почек экскреторная урография (при стихании активности ГН) Дифференциальный диагноз необходимо проводить с токсическим поражением почек, в том числе при острых инфекционных заболеваниях (грипп, пневмония, сепсис и др.), острым интерстициальным нефритом, мочекаменной болезнью, острым пиелонефритом, дисметаболической нефропатией, травмой почек, туберкулезом почек, опухолями органов мочевой системы, поражением почек при системных заболеваниях. Таблица 16 Дифференциально-диагностические признаки острого гломерулонефрита и острого пиелонефрита (Г.А. Маковецкая) Показатель Время появления Возраст пациента Стойкость синдрома Артериальная гипертензия Отеки Лихорадка Дизурия Болезненность при поколачивании по поясничной области Реакция мочи Протеинурия Гематурия Лейкоцитурия Бактериурия Повышение содержания мочевины Клубочковая фильтрация Проба Зимницкого Острый гломерулонефрит Через 2-3 недели после инфекции, чаще стрептококковой Чаще 5-12 лет Более 2 недель У 60-80% У 60-80% Редко Очень редко Очень редко Острый пиелонефрит Через 7-12 дней после ОРВИ Любой Более 2 недель Отсутствует Отсутствуют Имеется Часто Часто Кислая До 1-1,5 г/сут. - при нефритическом синдроме; выше 50 мг/кг/сут)-при нефротическом синдроме До макрогематурии Может быть в дебюте, незначительная или умеренная, лимфоцитарного типа Отсутствует В дебюте может повышаться Часто щелочная Не более 1,0 г/сут Снижена В 30-40% случаев может отмечаться гипостенурия Не изменена У ½ нарушение ритма мочеотделения и снижение концентрационной способности Микрогематурия у 1/3 больных До лейкоцитурии во всех полях зрения, нейтрофильного типа Имеется Не отмечается Лечение гломерулонефрита. Режим – больные с выраженными экстраренальными проявлениями заболевания, прежде всего с артериальной гипертензией, должны находиться на строгом постельном режиме. Расширение режима осуществляется после нормализации АД и/или уменьшении гипертензии и ликвидации макрогематурии. Длительный постельный режим, особенно при нефротическом синдроме, увеличивает возможность развития остеопороза из-за уменьшения мышечной активности. Диета гипонатриевая, с ограничением белка (диета №7 по Певзнеру). Жидкость при ГН не ограничивается. При явлениях гипергидратации, при сердечно-сосудистой недостаточности, при острой почечной недостаточности необходимо строго учитывать количество вводимой жидкости внутрь и параллельно - в продуктах. Диуретики и гипотензивные препараты. При отсутствии положительного эффекта от диетотерапии в течение 2-3 дней или при резко выраженном повышении АД, выраженном отечном синдроме, назначают диуретики: фуросемид-1-2-5 мг/кг в день, гипотиазид – 2,5 мг/кг в день, альдактон (верошпирон) – 1-3 мг/кг/сут. (до 10мг/кг/сут.), но не более 200 –300 мг/сут. При наличии стойкой гипертонии показано назначение нифедипина – 0,15 –0,25 мг/кг – разовая доза, энап – в дозе 0,1-0,5 мг/кг в день (противопоказан при выраженном отечном синдроме, снижении клубочковой фильтрации). Лечение, направленное на уменьшение антигенной стимуляции Антибиотики назначаются в основном при постстрептококковом ГН длительностью от 2 до 4, а при необходимости - и более недель, а также при наслоении интеркуррентных заболеваний. Используются антибиотики с минимальной нефротоксичностью, предпочтение отдается препаратам пенициллинового ряда, цефалоспоринам 2 – 3 поколения. Патогенетические методы лечения 1. Глюкокортикоиды (преднизолон) – показаны при нефротическом синдроме, при сочетании нефротического синдрома с гематурией без гипертензии. Не показаны стероиды при постстрептококковом ГН. Преднизолон назначается в дозе 2,0-3,0 мг/кг (60 мг/м2) в сутки но не более 80 мг/сут. Курс лечения максимальной дозой преднизолона продолжается 46-8 недель, с переходом на альтернирующий режим приема препарата (суточная терапевтическая доза преднизолона назначается через день) не менее 2х месяцев. При лечении преднизолоном необходимо назначать препараты калия, ежедневно измерять АД, подсчитывать пульс, взвешивать больного, 1 раз в 3 дня исследовать кал на скрытую кровь, 1 раз в неделю исследовать мочу на сахар, 1 раз в неделю делать ЭКГ, следить за симптомами остеопороза (боли в позвоночнике и костях). 2. Цитотоксические препараты (антиметаболиты и алкилирующие) назначаются при наличии противопоказаний к лечению преднизолоном, гормонорезистентном варианте нефротического синдрома, часторецидивирующем и гормонозависимом нефротическом синдроме. Лейкеран (хлорбутин) назначается в дозе 0,2 – 0,3 мг/кг массы в сутки, циклофосфан 2мг/кг в сутки. Лечение этими препаратами в терапевтической дозе проводится на фоне применения антибиотиков (в возрастной дозе) и преднизолона в дозе 0,5 мг/кг в сутки с целью профилактики осложнений (бактериальное воспаление, цитопения). 3. Гепарин – антикоагулянт прямого действия, первоначальная доза – 150-200ЕД/кг массы тела в сутки. Доза препарата определяется под контролем времени свертывания крови по Ли Уайту. Терапевтической считается та доза, от введения которой время свертывания крови по сравнению с исходной (перед первой инъекцией) удлиняется в 1,5 – 2 раза через 4 часа после в/в и через 6 – 8 часов после п/к инъекции. Курс лечения 4-6 недель. В последние годы синтезированы гепарины с низкой молекулярной массой (фрагмин, фраксипарин), в том числе и для перорального применения, что позволяет назначать их амбулаторно и длительно. 4. Курантил (дипиридамол) – антиагрегант, применяется в течение 6 – 12 месяцев. Назначается в сочетании с антикоагулянтами на фоне цитостатика и преднизолона (четырехкомпонентная терапия ). К другим методам лечения ГН относятся: 1) пульсовая терапия метилпреднизолоном внутривенно в дозе 30 мг/кг (до 1000 мг) через день в течение 1 – 3 недель. Проведение пульсовой терапии метилпреднизолоном ре- комендуется у детей с первичным ГН, проявляющимся нефротическим синдромом, резистентным к стандартному пероральному режиму преднизолона. 2) гемосорбция и плазмаферез способствуют не только механическому удалению циркулирующих иммунных комплексов, но и изменению их свойств, ведущему к улучшению их фагоцитоза. 3) иммуномодулирующие препараты (декарис) назначается в дозе 1мг/кг массы тела в день (по 3 дня в неделю, всего 8-12 циклов) в сочетании с постоянным (до 12 недель) применением 10 мг преднизолона, фенилина и курантила. В последние годы у больных с частыми рецидивами нефротического синдрома и осложнениями кортикостероидной терапии применяют иммунодепрессанты - циклоспорин А (сандиммун, сандиммун - неорал) и селлсепт (микофенолат - мофетил) в сочетании с небольшой дозой преднизолона. Диспансеризация. Детей с острым ГН педиатр осматривает 1-й год в первые 3 мес.- 2 раза в месяц, с 3 до 12 мес.- 1 раз в мес., затем-1 раз в 2-3 мес. Нефролог 1-й год- 1 раз в 3 мес., затем- 1-2 раза в год. При хроническом ГН педиатр 1-2 год- 1 раз в месяц, затем-1 раз в 2-3 мес., при снижении почечных функций - ежемесячно; нефролог-1 раз в 2-3 мес. На диспансерном учете дети с ОГН находятся 5 лет. С учета можно снимать при условии стойкой клинико-лабораторной ремиссии и после комплексного обследования в нефрологическом стационаре. При хроническом ГН больные наблюдаются до передачи во взрослую сеть. Вопросы для тестового контроля № п/п 1 2 3 4 5 6 7 8 9 10 Эталоны ответов При остром гломерулонефрите с нефротическим синдромом в анализе мо- б чи диагностируется: а) умеренная протеинурия, б) выраженная протеинурия, в) умеренная гематурия, г) лейкоцитурия, д) небольшая протеинурия При лечении острого гломерулонефрита с нефритическим синдромом не а применяются: а) кортикостероиды, б) антибиотики, в) антикоагулянты, г) антиагреганты, д) диуретики При какой длительности гломерулонефрита можно говорить о затяжном в течении заболевания: а) 3 мес., б)1 год, в) 6 мес., г) 2 мес., д)1 ,5 года Острый гломерулонефрит чаще всего развивается после: а) ангины, б) а, г пневмонии, в) гриппа, г) скарлатины, д) энтеробиоза При остром гломерулонефрите назначается стол №: а)1, б) 5, в) 7, г) 9, д)10 в При гломерулонефрите преимущественно поражается: а) клубочек, б) ка- а нальцы, в) почечные лоханки, г) интерстициальная ткань, д) мочеточники При хроническом гломерулонефрите у детей выделяют следующие клини- б, в, д ческие формы: а) гипертоническая, б) нефротическая, в) гематурическая, г) волнообразная, д) смешанная Острый гломерулонефрит после стрептококковой инфекции возникает че- б рез: а) 1 неделю, б) 1-3 недели, в) 4-6 недель, г) 7-10 недель, д) 3 месяца Препараты калия показаны при назначении: а) гипотиазида, б) ретаболила, а, г в) капотена, г) фуросемида, д) верошпирона Признаками нефротического синдрома являются: а) массивные отеки, б) а, д гипертензия, в) гипотензия, г) гематурия, д) выраженная протеинурия Содержание вопросов Ситуационные задачи № п/п 1 Содержание задач Эталоны ответов Коля С., 10 лет поступил в клинику с жалобами на выраженные отеки лица, нижних конечностей, редкие мочеиспускания. Заболел около 2-х недель назад, когда после купания в реке поднялась температура, беспокоила боль в горле, слабость, головная боль, к врачу не обращались. Лечился дома аспирином, полоскал горло. Температура нормализовалась, но держалась слабость. На 10-й день болезни появились отеки век, стал реже мочиться. Обратился к врачу и был направ- 1. Острый гломерулонефрит с нефритическим синдромом, период начальных проявлений. 2. Необходимо исследовать: кровь на общий анализ, белки сыворотки, белковые фракции, фибриноген, холестерин, остаточный азот, мочевину, креатинин сыворотки, титр анти-стрептолизин - О, се- лен на стационарное лечение. При поступлении состояние тяжелое, резкая бледность кожных покровов, отеки на лице, голенях. При исследовании в зеве рыхлые, гипертрофированные миндалины, гиперемия. Зубы кариозные. Границы сердца расширены влево на 1 см, тоны глухие, выслушивается систолический шум на верхушке, Y точке и акцент тона на легочной артерии. Пульс 108/минуту. Артериальное давление –130/80 мм рт. ст. Диурез за сутки 600 мл. Моча красного цвета. Стул оформлен. Вопросы: 1. Поставить предварительный диагноз. 2. Назначить исследования. 3. Составить план лечения. 2 Марина Л., 6 лет, поступила в детское отделение областной больницы с жалобами на распространенные отеки на лице, туловище, конечностях, головную боль, тошноту, снижение аппетита, уменьшение количества мочи. Из анамнеза известно, что больна в течение 1 года 5 месяцев. Лечилась по поводу данного заболевания по месту жительства в течение 10 месяцев, затем выписана с улучшением домой. Дома самочувствие было удовлетворительным, но по утрам отмечалась пастозность век, периодически болела голова. После острого респираторного заболевания усилились отеки, стала мало мочиться. При поступлении состояние тяжелое, отеки лица нижних конечностей, определяется свободная жидкость в животе. Расширены границы сердца, артериальное давление 140/95 мм. рт. ст. Печень выступает на 3 см из-под края реберной дуги. В анализе мочи обнаружена протеинурия - 1,65 %0, лейкоциты -3-4 в поле зрения, эритроциты выщелоченные и свежие 5-7 в поле зрения, цилиндры гиалиновые, зернистые до 5-6 в поле зрения. В общем анализе крови: эритроциты - 3,1х1012 , Hb- 110 г/л, цветной показатель- 0,87, лейкоциты - 10,8х109, СОЭ60 мм/ч. Вопросы: 1. Поставить предварительный диагноз. 2. Назначить необходимые исследования. ромукоид, СРБ. Общий анализ мочи. Проба Зимницкого, клиренс эндогенного креатинина. Консультация лор - врача, стоматолога, окулиста, ЭКГ. 3. Стационарное лечение: режим постельный, стол №7, Антибиотики (пенициллин), витамины, антиагреганты (курантил), антикоагулянты (гепарин - после получения данных коагулограммы) антигистаминные, диуретики (фуросемид). 1. Хронический гломерулонефрит, смешанная форма, период обострения. 2. План обследования: ан. крови на белок, белковые фракции, фибриноген, холестерин, остаточный азот, мочевину, креатинин сыворотки. Клиренс эндогенного креатинина, проба Зимницкого. Иммунограмма. Ан. мочи на суточную экскрецию белка, селективность протеинурии, пункционная биопсия почек. ЭКГ, ЭХО-КГ. Консультация лор врача, стоматолога, окулиста. Рекомендуемая литература: Основная: 1. Шабалов Н.П. Детские болезни. Изд - е 5-е. В двух томах. Т. 2., Ст.- Пб: Питер, 2006.-731 С. 2. Папаян А.В., Савенкова Н.Д. Клиническая нефрология детского возраста. С.-Пб., «Левша», 2008. – 600 с. Дополнительная: 1. Сергеева Т.В., Цыгин А.Н.и др. Лечение гломерулонефрита у детей. Методическое пособие для врачей. Москва 2001.-28с. 2. Практическое руководство по детским болезням. Под общей редакцией проф. В.Ф. Коколиной и проф. А.Г.Румянцева. Том VI. Нефрология детского возраста. Под ред.С.В. Бельмера, И.М. Османова. Медпрактика - М, Москва, 2005, 712 С. 3. Баранов А.А., Сергеева Т.В. Амбулаторная нефрология. Амбулаторная педиатрия.-М.: Союз педиатров России. Том 1, 2009.-156 с. Занятие № 8. ЯЗВЕННАЯ БОЛЕЗНЬ Цель занятия: Изучить клинические особенности язвенной болезни в детском возрасте, методы ранней диагностики, принципы лечения и профилактики на современном этапе. Вопросы для самоподготовки: 1. Эпидемиология язвенной болезни 2. Современные представления об этиопатогенезе язвенной болезни 3. Особенности течения язвенной болезни у детей 4. Дифференциальная диагностика язвенной болезни 5. Осложнения язвенной болезни 6. Современные принципы и методы терапии язвенной болезни 7.Профилактика язвенной болезни у детей Язвенная болезнь (ЯБ) – хроническое рецидивирующее заболевание, характеризующееся формированием язвенного дефекта в желудке или 12-перстной кишке, обусловленное нарушением равновесия между факторами агрессии и защиты гастродуоденальной зоны. Эпидемиология язвенной болезни. На современном этапе ЯБ перестала считаться редким заболеванием у детей в связи с довольно частым ее распространением (1 случай на 600 детей). В последние десятилетия наблюдается омоложение ЯБ (регистрация заболевания в дошкольном возрасте), увеличение тяжелых форм, трудно поддающихся терапии, высокий процент инвалидизации детей с ЯБ. Этиопатогенез. Язвенная болезнь относится к полиэтиологичным (мультифакториальным) заболеваниям. Ведущую роль в формировании и хронизации заболевания играют нервнопсихические, эндокринные и наследственно-конституциональные факторы, микроорганизмы, лекарственные воздействия и пищевая аллергия, нарушение характера и режима питания (употребление грубой и острой пищи, поспешная еда, еда в сухомятку, большие перерывы между приемами пищи, плохое пережевывание и т.д.). В последние годы установлена важная роль микроорганизмов Helicobacter pylori (НР) в развитии повреждений слизистой оболочки желудка и 12-перстной кишки. Проникая в межклеточные пространства, НР благодаря наличию у них уреазной активности и способности вырабатывать цитотоксины способствуют развитию повреждений эпителиальных клеток и воспалительных реакций. В настоящее время полагают, что уничтожение НР слизистой оболочки желудка значительно снижает риск последующих рецидивов заболевания. Язвенная болезнь возникает при нарушении равновесия между факторами кислотно - пептической агрессии желудочного содержимого и элементами защиты слизистой оболочки желудка и 12перстной кишки. Схематично это равновесие может быть представлено в виде так называемых весов Шея (схема 3.). Агрессивное звено язвообразования включает в себя: повышение выработки соляной кислоты, которое может происходить при увеличении массы обкладочных клеток, гиперфункции гастрина, нарушении нервной и гуморальной регуляции желудочного кислотовыделения; повышенное образование пепсиногена и пепсина; нарушение моторной функции желудка и 12-перстной кишки (задержка или, наоборот, ускорение эвакуации кислого содержимого из желудка, дуоденогастральный рефлюкс) и, в последнюю очередь, прямое травматизирующее действие пищи. Ослабление защитных факторов слизистой оболочки желудка и 12-перстной кишки может возникнуть в результате снижения выработки и нарушения качественного состава желудочной слизи, уменьшения концентрации бикарбонатов (в составе желудочной и панкреатической секреции), ухудшения процессов регенерации в слизистой оболочке желудка и 12перстной кишки, ухудшения кровоснабжения и уменьшения содержания простагландинов в слизистой оболочке желудка. Схема 3. Патогенез язвообразования нет язвы язва факторы кислотнопептической агрессии - Увеличение выработки соляной кислоты - повышение образования пепсиногена и пепсина - нарушение гастродуоденальной моторики - прямая травматизация слизистой оболочки желудка и 12-перстной кишки факторы защиты слизистой оболочки желудка - нарушение желудочного слизеобразования - уменьшение выделения бикарбонатов - нарушение регенераторных процессов в слизистой оболочке желудка - ухудшение кровоснабжения слизистой оболочки желудка - уменьшение содержания простагландинов в стенке желудка Соотношение тех или иных патогенетических факторов агрессии и защиты может быть различным в каждом конкретном случае заболевания. Все же принято считать, что значение кислотно-пептического фактора наиболее выражено при язвах 12-перстной кишки, тогда как снижение резистентности слизистой оболочки чаще выступает в качестве патогенетического фактора язв желудка. Кроме того, в патогенезе язвенной болезни важное значение имеют гормональные факторы (половые гормоны, гормоны коры надпочечников, гастроинтерстициальные пептиды), биогенные амины (катехоламины, гистамины, серотонин), иммунные механизмы, нарушения процессов перекисного окисления липидов. Классификация язвенной болезни строится по клинико-анатомическому и патоморфологическому принципу (таблица 17). Таблица 17 Классификация язвенной болезни у детей Клиническая фаза Тяжесть и эндоскопическая стадия течения В желудке: ОБОСТРЕНИЕ Легкое I стадия (свежая язва) Средней - медиагастральная II стадия (начало эпителизации) тяжести - пилороантральная Тяжелое СТИХАНИЕ ОБОСТРЕНИЯ В 12-перстной кишке: III стадия (заживление язвы) - луковичная - без образования рубца - постлуковичная - с формированием рубца, рубцово-язвенная деформация В желудке и РЕМИССИЯ 12-перстной кишке Локализация язвы Осложнения Кровотечение перфорация пенетрация стеноз перивисцерит При формулировке диагноза указывается локализация язвы (желудок, 12-перстная кишка или сочетанное поражение), клиническая фаза заболевания (обострение, стихание обострения, ремиссия), эндоскопическая характеристика дефектов (количество – одиночный, множественные) и стадия эволюции язвенного процесса. Клиника. Клинико-эндоскопическая картина I стадии (свежая язва). Ведущим симптомом являются тощаковые и поздние боли в эпигастрии, которые появляются через 2-3 часа после приема пищи. У половины детей отмечаются ночные боли. Имеется четкий «мойнигановский» ритм болей: голод – боль – прием пищи – облегчение и т.д. Прием пищи улучшает самочувствие ребенка, но полного исчезновения болей не наблюдается. По характеру боли приступообразные, нередко иррадиируют в спину, поясницу. Пальпация живота из-за болевого синдрома и активного напряжения мышц брюшной стенки затруднительна. Отмечается положительный симптом Менделя (поколачивание указательным пальцем в проекции пилоробульбарной зоны вызывает болевые ощущения), имеются зоны кожной гиперестезии Захарьина-Геда. Из диспепсических расстройств выражены признаки ацидизма (изжога, отрыжка кислым), тошнота, реже рвота. При эндоскопическом исследовании на фоне выраженных воспалительных изменений слизистой оболочки гастродуоденальной зоны выявляется дефект (дефекты) округлой или овальной формы, окруженный воспалительным валом, создающим картину глубокого изъязвления. Края дефекта отечные. Дно язвы с четкими краями, равномерно покрыто наложениями фибрина серо-желтого или зеленого цвета. Клинико-эндоскопическая картина II стадии (начало эпителизации). Поздние боли сохраняются, но возникают, как правило, днем. У большинства детей после приема пищи боли полностью исчезают, хотя и сохраняется «мойнигановский» ритм. По характеру боли становятся ноющими, тянущими, иррадиация менее выражена и отмечается лишь у 20% больных. Болезненность при поверхностной пальпации и зоны кожной гиперестезии отсутствуют, сопровождается мышечной защитой. Уменьшается степень выраженности диспепсических проявлений. Визуально при эндоскопическом исследовании уменьшается гиперемия слизистой оболочки, сглаживается отек вокруг язвенного дефекта и исчезает воспалительный вал. Края дефекта уплощаются, становятся неровными, надвигаются к центру язвы, уменьшая ее размеры и глубину. Дно дефекта начинает очищаться от фибрина, намечается конвергенция складок к язве, что отражает процесс заживления язвенного дефекта. Клинико-эндоскопическая картина III стадии (заживление язвы). У больных периодически отмечаются поздние боли и натощак, без четкой локализации и «мойнигановской» периодичности, чувство голода, как эквивалент ночных болей. При глубокой пальпации живота, сохраняется болезненность в пилородуоденальной зоне. Диспепсические расстройства слабо выражены. Визуально при эндоскопии на месте дефекта определяются следы репарации в виде рубцов красного цвета различной формы (линейной, циркулярной, звездчатой) с деформацией стенки желудка (12-перстной кишки) или без таковой. Эпителизация поверхностных дефектов происходит без образования рубца с разрастанием грануляционной ткани округлой или неправильной формы вишневого цвета, выступающей над уровнем слизистой. Несмотря на заживление дефектов сохраняются признаки активности сопутствующего воспалительного процесса слизистой оболочки желудка и особенно 12-перстной кишки, моторно-эвакуаторные нарушения (гипертонус, дуодено - гастральный рефлюкс). Диагностика и план обследования. Диагноз язвенной болезни ставится на основании эндоскопического обнаружения язвенного дефекта в желудке или двенадцатиперстной кишке. Рентгенологическое исследование с барием не является обязательным для диагностики неосложненной язвенной болезни. Но если оно проводится, то типичным рентгенологическим симптомом язвы является обнаружение ниши - затек контраста вглубь стенки органа. Секреторная функция желудка, как правило, характеризуется повышением показателей как базальной, так и стимулирующей фракции, отмечается снижение нейтрализующей способности антрального отдела. Исследование желудочной секреции не является методом диагностики язвенной болезни, но оно позволяет выявить те функциональные нарушения, которые необходимо учитывать при проведении терапии. Исследование на НР также входит в обязательную схему обследования больного с язвенной болезнью. НР обнаруживается у абсолютного большинства пациентов. Алгоритм диагностических методов при подозрении на язвенное кровотечение следующий: сбор анамнеза и осмотр больного, определение группы крови и резуспринадлежности, эндоскопия и при необходимости – рентгеноскопия желудка и двенадцатиперстной кишки и УЗИ брюшной полости. Дифференциальная диагноз ЯБ проводится с многочисленной группой патологических состояний, сопровождающихся гастродуоденальными изъязвлениями («стрессовые» язвы, лекарственные язвы), а также с гастродуоденитом и вторичными симптоматическими язвами (гепатогенные, панкреатогенные и эндокринные язвы). Осложнения ЯБ в детском возрасте отмечаются у 8,5% больных, у мальчиков в 2 раза чаще, чем у девочек. В структуре осложнений доминируют кровотечения (80%), которые при язвенной болезни 12-перстной кишки встречаются в 6 раз чаще, чем при язвенной болезни желудка, на втором месте по частоте (11%) – стенозирующие процессы. Перфорация язвы в 2 раза чаще встречается при желудочной локализации язвы. Пенетрация чаще всего возникает на фоне длительного и тяжелого течения болезни, а также при неадекватной терапии. Лечение язвенной болезни комплексное (режим, лечебное питание, медикаментозная и немедикаментозная терапия) и этапное (стационар – поликлиника – санаторий). Тактика ведения больных должна быть дифференциальной и строго индивидуальной. В период обострения заболевания лечение проводится в условиях стационара. Назначается постельный режим до исчезновения самостоятельных болей в животе (в первой стадии – на 3-4 недели, во второй – на 2-3 недели, в третьей – на 1-2 недели). Основа лечения диетотерапия, которая строится на принципах антацидных свойств пищи, механического, химического и термического щажения слизистой оболочки верхних отделов пищеварительного тракта (диета 1а, 1б, 1 по Певзнеру). Кратность приемов пищи 4-5 раз в день. Медикаментозная терапия предусматривает воздействие на основные патогенетические звенья. Основная ее цель - снижение кислотно - пепсической активности желудочного сока, эрадикация (уничтожение, элиминация) Helicobacter pуlori, повышение защитных свойств слизистой оболочки желудка и 12-перстной кишки, коррекция моторноэвакуаторной функции гастродуоденальной системы, а также уменьшение или устранение боли, предупреждение рецидивов и осложнений. К препаратам, используемым в педиатрической практике для эрадикационной терапии российской группой экспертов по изучению хеликобактериоза в 1999г. были рекомендованы следующие: 1. Коллоидный субцитрат висмута (Де-нол) - 4мг/кг 2. Амоксицилин (Флемоксин - солютаб) - 25 мг/кг (мах - 1 г/сут.) Кларитромицин (Клацид) - 7,5 мг/кг (мах - 500мг/сут) Рокситромицин (Рулид) - 5-8 мг/кг (мах - 300мг/сут) Азитромицин (Сумамед) - 10мг/кг (мах - 1г/сут.) 3. Макмирор 15 мг/кг Фуразолидон - 20мг/кг Метронидазол - 40мг/кг 4. Омепрозол (Лосек) - 0,5 мг/кг Ранитидин (Зонтак) – 3 мг/кг С учетом рекомендованных препаратов предложены различные их сочетания (схемы) в виде двойной, тройной и квадротерапии (4 препарата). Основой лечения являются использование схем тройной эрадикационной терапии на основе блокаторов протонового насоса или H2 -гистаминовых рецепторов в сочетании с антибиотиками, метронидозолом и нитрофуранами, которые входят в национальные рекомендации по лечению хеликобактериоза. В схему квадротерапии к вышеперечисленным препаратам дополнительно назначается Де-нол. Продолжительность эрадикации 7 дней. В детской практике из антибиотиков для проведения эрадикационной терапии наиболее часто используется полусинтетический производный пенициллинового ряда амоксициллин. Он устойчив в кислой среде желудочного содержимого, практически не влияет на биоценоз кишечника, разрешен к применению, у детей различного возраста резистентность штаммов Helicobacter pуlоri к нему практически не различается. Другой группой антибиотиков, исследуемых для эрадикации хеликобактериоза являются макролиды, обладающие высокими кислотоустойчивыми свойствами (кларитромицин, азитромицин, рокситромицин). Однако, к ряду препаратов этой группы вырабатывается устойчивость. В ряде стран Восточной Европы отмечается также высокая первичная резистентность Н. pуlоri к метронидозолу (от 40% до 75%). В место метронидозола в схемах эрадикации используется кислотоустойчивый препарат нитрофуранового ряда фуразолидон. После завершения эрадикационной терапии назначается антациды: альмагель, ремагель, фосфалюциль, маалокс, гелносиллок, тальцид, тальцид рени, викалин и др. В качестве антисекреторных средств широко используются блокаторы H+/K+ АТФазы омепразол (омез), лансопразол, пантогразол, рабокразол и др.) Назначаются витамины группы В, витамин U (по 0,05-0,1 г 3 раза в день). Антацидная терапия является одним из основных патогенетических факторов лечения (неадсорбируемые препараты – альмагель, ремагель, фосфалюгель, маалокс, гастрофарм, а также препараты висмута – викалин, Де-Нол и другие). Для снятия болевого синдрома назначают спазмолитики миотропного ряда (папаверин, Но-шпа, галидор, реглан в возрастной дозировке) одновременно с периферическими Мхолиноблокаторами (гастроцепин, метацин, пробантин, платифиллин по ½ таблетки 3 раза в день до еды и перед сном), препараты белладоны по 0,005-0,01г 2-3 раза в день. Патогенетически обоснованным является назначение препаратов, блокирующих Н2-рецепторы гистамина, снижающих секрето- и кислотообразование (ранитидин в дозе 4-5 мг на 1 кг массы в течение 3-4 недель, а также препараты нового поколения – фамотидин, низотидин). В качестве антисекреторных средств широко используются ингибиторы Н+/К+ АТФазы (омепразол в возрастной дозировке). Учитывая важную роль пилорического хеликобактериоза в возникновении ЯБ, используются различные схемы антибактериальной терапии язвенной болезни (Де-Нол + оксициллин, Де-Нол + амоксициллин + метранидозол, Де-Нол + оксициллин + трихопол и др.). Важное место в комплексном лечении язвенной болезни занимает седативная терапия (настой корня валерианы, настойка пустырника, препараты брома, по показаниям – элениум, триоксазин, седуксен). С целью ускорения процессов регенерации назначают производные пиримидина (метилурацил по 0,3-0,5 г 3 раза в день, пентоксил 0,1-0,5г 3 раза в день в течение месяца). Из немедикаментозных способов лечения используется фитотерапия, иглорефлексотерапия, лазеротерапия, гипербарическая оксигенация, прием минеральных вод. Физиолечение при язвенной болезни имеет ограниченное применение, учитывая возможность осложнений. Наиболее часто назначаются: электросон, воротник по Щербаку с бромистым натрием, синусоидальные модулированные токи (СМТ). Санаторное лечение детей с ЯБ проводится в условиях специализированного гастроэнтерологического санатория (местно и на курортах Кавказских Минеральных Вод). Оптимальный срок для направления в санаторий – первые 3 месяца после наступления ремиссии ЯБ. Прогноз. Благоприятное или неблагоприятное и течение язвенной болезни у детей определяется частотой рецидивирования заболевания и сроками заживления язвенного дефекта. Диспансерное наблюдение. 1.Наблюдение специалистами. Первый год наблюдения: педиатр, гастроэнтеролог - 1 раз в 3 месяца. В последующие годы - 2 раза в год. Осмотр невропатолога, других специалистов, ЛОР, стоматолог - 1 раз в год. 2.Методы обследования: - исследование желудочной секреции вне обострения - 1 раз в год (или pH - метрия). - ЭГДС - 2 раза в год на первом году после обострения (через 6 мес. после обострения и в конце первого года наблюдения). В последующие годы - 1 раз в год. - диагностика хеликобактериоза экспресс - методом (при положительном тесте в анамнезе) 1 раз в год. анализ крови (эритроциты, гемоглобин) - 2 раза в год. Основные пути оздоровления: -Диета I -1 год, через 1-2 года после обострения - диета5. -Медикаментозная терапия (антациды, H2 - блокаторы рецепторов гистамина, ингибиторы "протоновой помпы", прокинетики, вегетотропные препараты, поливитаминотерапия) -Физиолечение (СМТ ног область эпигастрия, микроволновая терапия, электрофорез брома на воротниковую область, электрофорез на эпигастральную область новокаина, папаверина № 10-12 -ЛФК №10 - Санаторно-курортное лечение: в местных условиях, санатории Кавказских Минеральных Вод (Железноводск). Профилактика. Первичная профилактика - это выявление фактора риска, способствующих формированию заболевания и по возможности своевременное их устранение. Вторичная профилактика - это комплекс реабилитационных мероприятий, проводимых в процессе диспансерного наблюдения за детьми с язвенной болезнью. Диспансерное наблюдение ребенка с ЯБ осуществляет педиатр и гастроэнтеролог детской поликлиники, по достижении 15 лет больной с диспансерного учета не снимается и передается под наблюдение терапевта. Вопросы для тестового контроля № п/п 1 2 3 4 5 6 7 8 9 10 Содержание вопросов К основным проявлениям ЯБ у детей относятся: а) голодные боли, б) боли в суставах, в) ночные боли, г) субфебрилитет, д) поносы Основными методами диагностики ЯБ являются: а) ультразвуковое исследование органов брюшной полости, б) общий анализ крови, в) эзофагогастродуоденоскопия, г) копрограмма, д) рентгеноскопия желудка и 12-перстной кишки С антацидной целью при язвенной болезни наиболее часто назначаются: а) гидрокарбонат натрия. б) альмагель, в) фосфалюгель г) жженая магнезия, д) маалокс Осложнения язвенной болезни у детей: а) кровотечения, б) гастроэзофагальный рефлюкс. в) стенозирующие процессы, г) пенетрация, д) малигнизация язвы К факторам защиты слизистой оболочки желудка относятся: бикарбонаты, б) соляная кислота, в) простогландины, г) пепсин, д) слизь Наиболее частая область иррадиации болей при язвенной болезни у детей: а) левое плечо, б) спина, в) паховая область, в) поясница, д) правое подреберье Симптомы массивных кровотечений при язвенной болезни у детей: а) рвота в виде кофейной гущи, б) дегтеобразный стул, в) артериальная гипертензия, г) тахикардия, д) дыхание Куссмауля В схему лечения хеликобактериоза включают: а) галидор, б) Де-нол, в) трихопол, г) атропина сульфат, д) витамин U Симптомы, свидетельствующие о повышении кислотности желудочного сока: а) жидкий водянистый стул, б) изжога, в) отрыжка воздухом, г) тошнота, д) горечь во рту К блокаторам Н2 рецепторов гистамина относятся: а) ранитидин, б) фамотидин, в) низотидин, г) ранитек, д) фосфалюгель Эталоны ответов а, б в, д б, в, д а, в, г а, б, д б, г а, б, г б, в б, г а, б, в Ситуационные задачи № п/п Содержание задач Эталоны ответов 1 Мальчик 14 лет страдает хронический гастродуоденитом с 9 – летнего возраста. Наследственность отягощена: у дедушки по отцу и у отца язвенная болезнь. Дедушка умер от прободной язвы желудка. Ребенок наблюдается и лечится в поликлинике по месту жительства. За последний год наблюдается ухудшение состояния. Стал более раздражительным, сон беспокойный, появилась отчетливая сезонность обострений, мойнигановский ритм болей. Последние 2 недели беспокоят интенсивные приступообразные боли в эпигастрии и пилородуоденальной зоне, с иррадиацией в спину, ночные, натощак, поздние; иногда возникает рвота, без примесей крови. При пальпации живота мышечный дефанс. Положительный симптом Менделя. Фиброгастродуоденоскопия: выраженные воспалительные изменения слизистой оболочки желудка и 12 – перстной кишки. На слизистой оболочки луковицы овальной формы дефект размером 1,5 см в диаметре, окруженный воспалительным валом с четкими краями. Ваш диагноз? Укажите план терапии. 2 Больной 15 лет обследован в гастроэнтерологическом отделении по поводу болей в эпигастральной и пилородуоденальной областях. Внутрижелудочная рН – метрия выявила усиление кислотообразующей функции тела желудка: рН базальной секреции – 1,4, стимулированной – 1,1. Фиброгастроскопия: диффузная гиперемия и отек слизистой оболочки желудка, гиперплазированные лимфоидные фолликулы в антральном отделе, пятнистая гиперемия слизистой луковицы 12 – перстной кишки. Проведение уреазного теста и иммуноферментного анализа выявило НР (Helicobacter pуlori). Ваш диагноз? Назначьте лечение. Определите мероприятия и длительность диспансерного наблюдения. .Диагноз: Язвенная болезнь луковицы двенадцатиперстной кишки, обострение (свежая язва) средней степени тяжести, неосложненная. Подростковый возраст больного, отягощенная наследственность (язвенная болезнь у отца и дедушки), длительность заболевания 5 лет, усиление астено-вегетативного синдрома, отчетливая сезонность и мойнигановский ритм болей, интенсивность болей с иррадиацией в спину, рвота, мышечный дефанс при пальпации живота, положительный симптом Менделя являются основанием для диагноза. Данные фиброгастродуоденоскопии подтвердили диагноз язвенной болезни и уточнили локализацию язвы. Лечение. Режим и диета, как при хроническом гастродуодените. Антациды: альмагель, фосфалюгель, маалокс. Антисекреторные препараты: гастроцепин, ранитидин. Препараты висмута: викалин, викаир, де - нол. Для повышения защитных свойств слизистой оболочки – ликвиритон, пентоксил, метацил, облепиховое масло, винилин, витамин U, сукральфат. Физиотерапевтическое лечение: парафиновые аппликации, УВЧ, диатермия, электрофорез с новокаином, магния сульфатом, кальция хлоридом. Диагноз: Хронический гастродуоденит с усилением кислотообразующей функции желудка хеликобактериозной зтиологии. Лечение больного с хроническим гастродуоденитом в фазе обострения с высоким уровнем кислотной продукции должно проводиться в стационаре. На 3-5 дней назначают облегченный постельный режим, далее палатный и больничный. Диета должна быть механически, термически и химически щадящей. Сначала назначают стол 1 по Певзнеру, затем – стол 5. Для борьбы с инфекцией НР существует несколько схем лечения. Схема №1: денол, амоксициллин, метронидазол 7-10 дней. Схема №3: денол 4 нед, амоксициллин 7-10 дней. Де - нол может быть заменен на вентрисол, амоксициллин – на кларитромицин рокситромицин. Из-за высокого уровня кислотной продукции показаны антацидные препараты (альмагель, фосфалюгель, маалокс), антисекреторные средства (фамотидин, ранитидин). Необходимо повысить защитные свойства слизистой оболочки. В фазе неполной клинической ремиссии целесообразно продолжить лечение в условиях местного специализированного санатория. Общая продолжительность диспансерного наблюдения – 3-5 лет. Противорецидивное лечение (осень-весна) включает снижение учебной нагрузки, строгий режим питания, фитотерапию, витамины, минеральные воды. Проводят санацию хронических очагов инфекции. Рекомендуемая литература: Основная: 1. Шабалов Н.П. Детские болезни. Изд - е 5-е. В двух томах. Т. 1., Ст.- Пб: Питер, 2006.-829 с. Дополнительная: 1. Лекции по педиатрии. Том 3. Гастроэнтерология // Под редакцией В.Ф. Демина, С.О. Ключникова, Л.Н. Цветковой, Ю.Г. Мухиной. РГМУ, Москва, 2003г., 320 с. 2. Гастроэнтерология и гепатология: диагностика и лечение // Под редакцией А.В. Калинина и А.И. Хазанова. – Москва, 2007 – 602 с. Занятие № 9. ЗАБОЛЕВАНИЯ ЖЕЛЧЕВЫДЕЛИТЕЛЬНОЙ СИСТЕМЫ У ДЕТЕЙ Цель занятия: Изучить клинические особенности холецистопатий в детском возрасте, методы ранней диагностики, принципы лечения и профилактики на современном этапе. Вопросы для самоподготовки: 1. Современные представления об этиопатогенезе дискинезий желчевыводящих путей, воспалительных заболеваний, желчекаменной болезни. 2. Классификация заболеваний желчевыделительной системы. 3. Клинические особенности гипер- и гипомоторной дискинезии, воспалительных заболеваний желчевыделительной системы. 4. Диагностика холецистопатий. 5. Дифференциальный диагноз воспалительных заболеваний желчевыделительной системы. 6. Этапное лечение заболеваний желчевыделительной системы. Хронические заболевания желчевыделительной системы (холепатии) занимают одно из центральных мест в детской гастроэнтерологии, уступая по частоте лишь патологии гастродуоденальной зоны. Хроническое, преимущественно рецидивирующее течение этих заболеваний, требует ранней диагностики, своевременной и рациональной терапии, длительного диспансерного наблюдения. Классификация заболеваний желчевыделительной системы 1. Дискинезия желчного пузыря и желчевыводящих путей. а) гипермоторная – гипертония, гиперкинезия; б) гипомоторная – гипотония, гипокинезия; в) смешанная 2. Дискриния желчного пузыря 3. Воспалительные заболевания: а) холецистит; б) холангит; в) холецистохолангит. По течению - острое, хроническое (рецидивирующее). 4. Врожденные пороки (аномалии) желчного пузыря и желчных путей. 5. Желчнокаменная болезнь 6. Паразитарные заболевания: аскаридоз, лямблиоз, описторхоз, эхинококкоз, фасциолез. 7. Опухолевидные заболевания Самой ранней и распространенной формой билиарной патологии у детей является дискинезия желчевыводящих путей. Под дискинезией желчевыводящих путей понимают нарушения моторики желчного пузыря и сфинктерного аппарата, клинически проявляющиеся болями в правом подреберье. Этиопатогенез. Ведущее значение в возникновении дискинезий желчевыводящих путей (ДЖВП) принадлежит нарушениям нейрогуморальной регуляции, приводящим к изменени- ям сочетанного сокращения желчного пузыря и сфинктерного аппарата желчевыделительной системы. Среди множества других этиологических факторов большое значение придается нарушению характера и режима питания, гиподинамии, наследственной предрасположенности, аллергической перестройке организма, нервным перенапряжениям и стрессовым ситуациям. В возникновении воспалительных заболеваний ведущая роль принадлежит инфекционноаллергическому фактору, а также снижению местной иммунной защиты билиарного тракта. Возбудителем заболевания чаще всего является условно-патогенная микробная флора (кишечная палочка, стафилококк, стрептококк, протей), реже – вирусная инфекция. Микробы проникают в желчные пути гематогенным, лимфогенным и восходящим путем (из кишечника при наличии дисбиоза). Важным условием развития воспаления является наличие застоя желчи и нарушение физико-химических свойств желчи (дискриния). Клиника. Ведущими проявлениями холецистопатий являются боли в правом подреберье, диспептические расстройства и признаки хронической интоксикации. Симптоматика дискинезий желчевыводящих путей зависит от характера моторных нарушений. При гипермоторной ДЖВП боли в животе приступообразного характера (схваткообразные, колющие, режущие), кратковременные, чаще всего связаны с отрицательными эмоциями или физической нагрузкой. Боли могут иррадиировать в правое плечо, подложечную и околопупочную области. При ДВЖП по гипотоническому типу боли в животе тупого характера, постоянные, ноющего характера, возникают после нарушения питания, перенесенных интеркуррентных заболеваний. Из диспептических расстройств наиболее часто наблюдается снижение аппетита, тошнота, реже – рвота и отрыжка горечью. При воспалительных заболеваниях тяжесть клинических проявлений нарастает и обусловлена фазой патологического процесса. В период обострения хронического холецистита (холецистохолангита) явления интоксикации ярко выражены (слабость, вялость, утомляемость, головные боли), усиливаются диспептические расстройства (тошнота, рвота, отрыжка, неустойчивость стула). Больных беспокоят боли в правом подреберье приступообразного или тупого характера в зависимости от характера сопутствующей дискинезии. Боли усиливаются при беге, ходьбе, при приеме острой, жирной пищи. При холецистохолангите (холангите) может быть повышение температуры до субфебрильных, реже до фебрильных цифр. При пальпации живота – болезненность в правом подреберье, положительные пузырные симптомы (Кера, Ортнера, Мерфи, Георгиевского - Мюсси). Умеренное увеличение печени (+1,52см по срединно-ключичной линии) наблюдается лишь при холангите или холецистохолангите. В фазу стихания обострения в желчных путях самостоятельных болей в животе не наблюдается, диспептические расстройства выражены в умеренной степени, при пальпации живота – умеренная болезненность в правом подреберье. Острый холецистит у детей в отличие от взрослых встречается редко (4-5% в структуре всех заболеваний желчевыделительной системы). Заболевание начинается остро, отмечаются сильнейшие боли в правом подреберье, эпигастрии, характерна иррадиация болей в правое плечо, правую лопатку, правую часть поясницу, реже - в подвздошную область. Боли сопровождаются тошнотой, повторной рвотой с примесью желчи. Ребенок беспокоен, для уменьшения болей постоянно меняет положение. Температура повышается до фебрильных цифр (38-40С). При поверхностной пальпации живота выражен дефанс в правом подреберье, а затем наблюдается мышечное напряжение всей брюшной стенки. Глубокая пальпация живота практически невозможна. В анализе крови увеличение СОЭ (25-30 мм/час), лейкоцитоз (12-20х109/л), нейтрофилез со сдвигом влево. У детей чаще встречается катаральный холецистит. Наиболее тяжелой формой острого холецистита является гангренозный, характеризующийся перфорацией желчного пузыря, развитием перитонита. Желчекаменная болезнь (ЖКБ) - это обменное заболевание гепатобилиарной системы, характеризующиеся образованием камней в желчном пузыре и протоках. Распространенность ЖКБ среди детей России за последнее десятилетие увеличилась в 10 раз (с 0,1 до1%). Среди взрослых частота ЖКБ колеблется в пределах 3-12%. Женщины страдают ЖКБ в 3-4 раза чаще, чем мужчины. Факторами риска формирования ЖКБ в детском возрасте являются: ранний перевод на искусственное вскармливание (доказано, что естественное вскармливание оказывает превентивный эффект гиперлипидемии), ожирение; влияние ксенобиотиков, лекарственных средств (метронидазол, эритромицин, ванкомицин и др. снижают конверсию холестерина); изменение состава микробной флоры кишечника (индигенная флора хозяина способствует поддержанию стабильного уровня холестерина, появление избыточного количества патогенной флоры усиливает синтез холестерина). Желчекаменная болезнь чаще различаются на фоне аномалий желчевыделительной системы (перегибы, перетяжки, стриктуры), прослеживается отягощенная наследственность преимущественно по женской линии. У детей чаще выявляются билирубиновые камни, холестериновые камни чаще всего формируются у подростков. У трети детей имеется сочетание ЖКБ с дисметаболической нефропатией (гипероксалурия, уратурия). В клинической картине ЖКБ выделяют 3 варианта течения: 1) бессимптомное камненосительство; 2) клиническая манифестация (боли в животе, диспепсические расстройства); 3) желчекаменная (печеночная) колика. Бессимптомное камненосительство - это отсутствие клиники заболевания, камни в желчном пузыре (или протоках) являются диагностической находкой при ультразвуковом обследовании ребенка. При манифестной форме боли в животе могут быть острыми, приступообразными, тупого характера. Появлению болей, как правило, предшествует прием жирной пищи либо физическая нагрузка. При печеночной колике приступ болей продолжается от нескольких минут до нескольких часов, отмечается тошнота и многократная рвота, не приносящая облегчения. При осмотре: положительный "пузырные" симптомы, может быть иктеричность склер, обесцвеченный стул, потемнение мочи. Наиболее информативным методом диагностики является ультразвуковое исследование (УЗИ) желчного пузыря и протоков. Диагностика и план обследования. Основа диагностики заболеваний желчевыделительной системы – дуоденальное зондирование и ультразвуковое исследование печени и желчевыделительной системы. По показаниям проводится внутривенная рентгеноконтрастная холецистография. Дуоденальное зондирование с последующей микроскопией порций желчи является одним из доступных методов исследования билиарной системы. При воспалительных заболевания в порциях желчи «В» и «С» обнаруживают признаки воспаления (хлопья слизи, лейкоциты, клетки цилиндрического эпителия). При ДЖВП признаки воспаления отсутствуют, но отмечаются нарушения ритма желчеотделения (при гипертонической дискинезии – удлинение времени пузырного рефлекса, быстрое опорожнение желчного пузыря; при гипотонической дискинезии время пузырного рефлекса уменьшается, а общая продолжительность желчеотделения увеличивается за счет увеличения выделения порции «В»). Изменяется и объем порции «В» желчи: при гипертонической ДЖВП резко уменьшен (3-5 мл при норме 10-30мл), при гипотонической - наблюдается значительное его увеличение (60-80мл и более). Ультразвуковое исследование желчного пузыря и печени позволяет выявить их аномалии, определить двигательные нарушения (характер дискинезии) и признаки воспаления (утолщение и уплотнение стенок желчного пузыря), а также состояние паренхимы печени. При нормальной функции желчного пузыря начало его сокращения соответствует 30-45 мин. после приема желчегонного завтрака (ксилит их расчета 0,5гр на 1 кг массы больного). Сокращение желчного пузыря менее чем на 55% от первоначального его объема расценивается как гипомоторная ДЖВП, а сокращение более, чем на 75% - как гипермоторная ДЖВП. При воспалительных заболеваниях желчевыделительной системы в период обострения могут быть также признаки воспаления в клиническом анализе крови (незначительный лейкоцитоз, ускорение СОЭ до 15-20мм/час). Дифференциальный диагноз заболеваний желчевыделительной системы проводится с хроническим гастритом, гастродуоденитом, дуоденитом, хроническим панкреатитом, глистной инвазией, хроническим колитом и т.д. Дифференциальный диагноз печеночной колики проводят с острым аппендицитом, почечной коликой, дискинезией желчевыводящих путей, дивертикулами 12- перстной кишки, паразитарными заболеваниями желчевыводящих путей (аскаридоз, фасциолез, эхинококкоз). Лечение. Режим больного зависит от фазы заболевания. В период обострения назначается постельный режим до исчезновения самостоятельных болей в животе. Диета у детей с холецистопатиями в фазе обострения должна быть легкоусвояемой, физиологичной с исключением жирных, жареных блюд, мясных и рыбных бульонов, экстрактивных веществ (стол 5 по Певзнеру). Питание дробное до 4-5 раз в сутки. Медикаментозная терапия. С целью устранения болей в животе назначают препараты белладонны (1мг на год жизни на прием), 0,1% раствор атропина внутрь по 1/2 капли на год жизни на прием, миотропные спазмолитики (но-шпа, папаверин). Однако спазмолитики одновременно снижают сократительную активность желудочно-кишечного тракта, проявление системного эффекта, подавление секреции пищеварительных желез. В связи с этим в последние годы с успехом используются препараты с изолированным спазмолитическим действием на различные отделы желчевыводящих путей (гепабене, дюспаталин (мебеверин), одестон, бускопан). Антибиотикотерапия при воспалительных заболеваниях желчевыделительной системы имеет ограниченное применение (острый холецистит, выраженный болевой синдром с повышением температуры, лейкоцитозом, ускорением СОЭ и выраженными воспалительными изменениями в желчи). Чаще всего используются полусинтетические пенициллины, эритромицин, линкомицин и др. в возрастной дозировке курсом 7-10 дней. При хроническом воспалении желчных путей рекомендуется назначение никодина или циквалона в дозе 1/2-1 таб. 3 раза в день, обладающих помимо желчегонного эффекта противовоспалительным действием. Желчегонную терапию проводят длительно прерывистыми курсами (не менее 2-х курсов по 7-10 дней в стационаре) с последующим приемом в амбулаторных условиях по 10 дней ежемесячно в течение 6 месяцев. Назначение желчегонных средств при холецистопатиях проводится дифференцированно в зависимости от формы дискинезии. При гипотонической (гипокинетической) дискинезии назначаются холекинетики, усиливающие опорожнение желчного пузыря. Холеретики, усиливающие секрецию желчи, назначаются при гипертонической (гиперкинетической) дискинезии - таблица 18. Таблица 18 Лечение дискинезий желчевыводящих путей 1 2 3 4 5 Гиперкинетическая дискинезия Диета 5 Спазмолитические препараты: Мхолинолитики - атропина сульфат, бускопан, платифиллин гидротартрат, метацин и др. и миотропные спазмолитики: галидор, но-шпа, папаверин и др. - эпизодически для снятия болевого синдрома. Желчегонные класса холеретиков, обладающие холеспазмалитическим действием: гепабене, одестон, галстена, гепатофальк планта, олиметин, фламин, холагогум, холагол, холосас, холофлукс, холензим и др. Минеральные воды низкой минерализации (Славяновская, Смирновская, Арзни, Ессентуки №4, 20 и др.) Физиотерапия (электрофорез с сульфатом магния, новокаином, папаверином, индуктотермия, на область правого подреберья, ультразвук высокой интенсивности на место проекции желчного пузыря, электросон, гальванический воротник по Щербаку). Гипокинетическая дискинезия Диета 5 Препараты стимулирующие моторику желчных путей: мотилиум, мотилак. цизаприд и другие прокинетики. Желчегонные класса холекинетиков, вызывающие сокращение желчного пузыря и расслабление сфинктеров Люткенса и Одди: гепабене, одестон, галстена, хофитол, ксилит, сорбит, магния сульфат, холагогум, и др. Минеральные воды высокой минерализации (Ессентуки №17, Мокшанская, Баталинская и др.) Физиотерапия (ультразвук низкой интенсивности, синусоидальные модулированные токи (СМТ) на область желчного пузыря, электрофорез с хлористым кальцием или прозерином на область правого подреберья, электросон, гальванический воротник по Щербаку). С целью устранения застоя желчи назначают слепые зондирования (тюбажи по Демьянову): при гипотонической дискинезии с сульфатом магния (25-30% раствор), с минеральной водой (200-300мл), сорбитом (10% - 100-50мл); при гипертонической дискинезии – с щелочными минеральными водами, настоем трав. Комплексная терапия больных холецистопатиями предусматривает назначение витаминов: А, группы В (В1, В2, В6 и В15), аскорбиновой и глютаминовой кислот, гипосенсибилизирующей терапии, лекарственных средств, улучшающих обменные процессы в печени (липоевая кислота, липамид, рибоксин, кокарбоксилаза и др.). Из физиотерапевтических средств рекомендуется электрофорез с сульфатом магния на область печени с последующим назначением индуктотермии, диатермии или парафиновых аппликаций. В лечение желчекаменной болезни используются препараты, способствующие растворению камней желчного пузыря (хенофальк, урсофальк, урсосан др.). Контроль за эффективностью проводимой терапии осуществляется через 6 мес.: при эффективности лечения отмечается уменьшение размеров камней желчного пузыря по результатам УЗИ. В случаях отсутствия эффекта от консервативной терапии проводится хирургическое лечение, которое является альтернативой консервативной терапии. В последние годы с успехом используются эндоскопические методы: 1) эндоскопическое удаление камней желчного пузыря (холелитотомия); 2) эндоскопическое удаление желчного пузыря и камней (холецистэктомия). Показано раннее оперативное лечение в плановом порядке на неосложненном желчном пузыре. Терапия хронических заболеваний желчевыделительной системы должна проводиться с учетом сочетанной патологии (хронический гастродуоденит, хронический панкреатит, лямблиоз, дисбактериоз и др.), особое внимание обращается на санацию очагов хронической инфекции в носоглотке и полости рта (гайморит, тонзиллит, аденоидит, кариес зубов и т.д.). Диспансерное наблюдение. 1. Наблюдение специалистами: - Врач - педиатр- 1 раз в квартал в течение первого года после обострения; 1 раз в 6 месяцев - в течение последующих лет Гастроэнтеролог - 2 раза в год в течение первого года после обострения; 1 раз в год - в последующие годы, по показаниям – чаще - ЛОР, стоматолог - 1-2 раза в год 2. Обследование: общий анализ крови, мочи- 1-2 раза в год; биохимический анализ крови (функции печени) - по показаниям. УЗИ органов брюшной полости - 1 раз в год. 3. Основные пути оздоровления: диета 5, противорецидивные курсы желчегонными средствами по 10 дней ежемесячно в течение 6 мес. после обострения, фитотерапия (зверобой, бессмертник, кукурузные рыльца, пижма, шиповник и др.), тюбажи по Демьянову, курсы минеральной воды (Смирновская, Славяновская, Ессентуки-4, Ессентуки-17) по 1 месяцу 3-4 раза в год, ЛФК. 4. Вакцинация: не ранее чем через 6 месяцев после обострения. 5. Длительность диспансерного наблюдения: не менее 3 лет после последнего обострения. Профилактика. В предупреждении холецистопатий важное значение имеет рациональное питание детей в семье, дошкольных учреждениях и школах, своевременное выявление и лечение паразитарных заболеваний (аскаридоз, лямблиоз, описторхоз и др.), профилактика и лечение кишечных инфекций, санация хронических очагов инфекции. Вопросы для тестового контроля № п/п 1 2 3 4 Содержание вопросов Эталоны ответов При воспалительных заболеваниях желчевыделительной системы боли в живо- б те локализуются: а) в правой подвздошной области, б) в правом подреберье, в) в эпигастрии, г) по ходу кишечника, д) в левом подреберье Из диспепсических расстройств у больных с холепатиями наиболее часто на- б, в блюдаются: а) запоры, б) тошнота, в) снижение аппетита, г) жидкий стул В диагностике заболеваний желчевыделительной системы необходимо исполь- а, в зовать: а) дуоденальное зондирование, б) посев кала на кишечную группу, в) УЗИ органов брюшной полости, г) анализ кала на дисбактериоз, д) копрограмма При обострении хронического холецистохолангита положительны следующие б, в, г симптомы: а) Пастернацкого, б) Кера, в) Ортнера, г) Мерфи, д) Воскресенского 5 6 7 8 9 10 Показаниями для назначения антибактериальной терапии при воспалительных заболеваниях желчевыделительной системы являются: а) боли в правом подреберье, б) острый холецистит, в) субфебрилитет, г) ускорение СОЭ до 40 мм/час, д) астенический синдром Большое значение в возникновении дискинезий желчевыводящих путей принадлежит: а) нарушениям нейрогуморальной регуляции, б) нарушению характера и режима питания, в) гиподинамии, г) наследственной предрасположенности, д) вирусным инфекциям .При гипермоторной ДЖВП боли в животе: а) приступообразного характера, б) кратковременные, в) чаще всего связаны с отрицательными эмоциями, г) ноющего характера, д) возникают после нарушения питания При гипомоторной ДЖВП боли в животе: а) приступообразного характера, б) кратковременные, в) чаще всего связаны с отрицательными эмоциями, г) ноющего характера, д) возникают после нарушения питания Дифференциальный диагноз заболеваний желчевыделительной системы проводится с: а) хроническим гастритом, б) гастродуоденитом, в) хроническим панкреатитом, г) глистной инвазией, д) пиелонефритом При лечении заболеваний желчевыделительной системы назначается диета №: а)1, б)1б, в) 5, г) 7, д) 9 б, г а, б, в, г а, б, в г, д а, б, в, г в Ситуационные задачи № п/п 1 2 Содержание задач Девочка 9 лет поступила в клинику с жалобами на приступ резчайших болей в животе, сопровождающихся тошнотой и рвотой. В первый год болезни приступы возникали 2 – 3 раза в месяц и месяц и были настолько мучительными, что каждый раз думали о хирургическом заболевании. Через год острые приступы прекратились, но осталась постоянная ноющая боль. В последующие 6 лет сохранялись симптомы интоксикации: частая тошнота и головная боль, субфебрилитет, упорная анорексия, потливость, бледность кожных покровов, быстрая утомляемость, периодически отмечали проявления нейродермита в локтевых сгибах. При исследовании кала обнаружены цисты лямблий. Объективно: отставание в физическом развитии, которое соответствует возрасту 6 – 7 лет. При пальпации живота: печень увеличена на 2 см, резко выражены пузырные симптомы. Вопросы: Ваш предполагаемы диагноз и план обследования ? Ваши рекомендации по режиму, диете, лечению? Укажите мероприятия диспансерного наблюдения. Эталоны ответов Диагноз: Хронический холецистохолангит в фазе обострения. Лямблиоз кишечника. Холецистохолангит – это одновременное поражение желчного пузыря и желчных путей. Изолированное их поражение встречается редко и процесс, как правило, захватывает всю желчевыделительную систему, поэтому термин холецистохолангит является предпочтительным. Показана тимоловая проба, исследование белкового спектра плазмы. Необходимо определение экскреторных ферментов (щелочная фосфатаза и др.), являющихся биохимическими маркерами холестаза, при котором в крови может повышаться уровень билирубина, холестерина желчных кислот и липопротеидов. Для уточнения диагноза необходимо провести инструментальное исследование (УЗИ органов брюшной полости, тепловидение, рентгеноконтрастная холецистография). Показана госпитализация. Постельный режим определяется длительностью болевого синдрома, симптомов интоксикации, температурной реакцией. Диета 5 или 5 а. Прием пищи дробный, малыми порциями, 5-6 раз в сутки. Показано назначение антибиотиков широкого спектра действия (ампициллин) курсом в течение 7-10 дней. Сопутствующая лямблиозная инвазия служит показанием к назначению трихопола, тинидазола, макмирора, тиберала, настоя березового листа. Широко используют желчегонные препараты, выбор которых зависит от вида нарушения моторики желчных путей. В связи с явлениями нейродермита назначают антигистаминные препараты (кларитин, фенкарол ). Девочка 8 лет госпитализирована с Диагноз: Дискинезия желчевыводящих путей по жалобами на постоянные боли в гипотоническому типу. правом подреберье, тупые, ноющие, Главный принцип диетотерапии – дробное питадавящие, периодически усиливают- ние, 5 – 6 раз в день. Потребность в белке обеспеся. Возникают через 1 – 1,5 часа по- чивается на 2/3 за счет животного белка и на 1/3 – сле приема жареной пищи (жареная свинина, пирожные с кремом) или физических нагрузок. Боли длятся 1 – 2 часа. Девочка жалуется на слабость, быструю утомляемость, тошноту. При пальпации живота отмечена болезненность в области правого подреберья и увеличение печени. Положительные пузырные симптомы. Длительность заболевания – 1 год. Вопросы: Ваш предположительный диагноз? Укажите режим и диету, принципы медикаментозного лечения. за счет белка растительного происхождения. Большинство больных не нуждаются в ограничении жира, так как он оказывает выраженное холеретическое и холецистокинетическое действие, способствует всасыванию жирорастворимых витаминов. Предпочтительнее растительное масло, но не следует полностью исключать и сливочного Содержание углеводов в рационе должно соответствовать возрастным нормам с учетом массы тела. Рекомендуется стол 5а, с исключением продуктов, содержащих тугоплавкие жиры (свинина, гусь). Постельный режим назначают редко, только больным с выраженным болевым синдромом. Кроме диеты 5, необходимо эффективное сочетание истинных холеретиков (стимулируют образование желчи и синтез желчных кислот) и холекинетиков (сульфат магния, сорбит, ксилит, маннит). Весьма эффективно проведение тюбажа с раствором сульфата магния по Демьянову. После 1-2 курсов желчегонных препаратов переходят на желчегонные травы. Физиотерапия в остром периоде: аппликация парафина и озокерита, электрофорез сульфата магния. Минеральные воды назначают из расчета 3 мл/кг массы тела (Ессентуки №4, боржоми, Славянская, Арзни). Прогноз при своевременной диагностике и проведении этиопатогенетического лечения благоприятный. Рекомендуемая литература: Основная: 1. Шабалов Н.П. Детские болезни. Изд - е 5-е. В двух томах. Т. 1., Ст.-Пб: Питер, 2006.-829 с. Дополнительная: 1. Лекции по педиатрии. Том 3. Гастроэнтерология // Под редакцией В.Ф. Демина, С.О. Ключникова, Л.Н. Цветковой, Ю.Г. Мухиной. РГМУ, Москва, 2003г., 320 с. 2. Гастроэнтерология и гепатология: диагностика и лечение // Под редакцией А.В. Калинина и А.И. Хазанова. – Москва, 2007 – 602 с. 3. Потапов А.С. Дисфункции билиарного тракта у детей. -М.: «АдамантЪ». – 2007. – 28с. Занятие № 10. САХАРНЫЙ ДИАБЕТ У ДЕТЕЙ Цель занятия: уметь диагностировать сахарный диабет, определить его тип согласно классификации ВОЗ, степень тяжести, состояние компенсации. Знать основные современные принципы лечения сахарного диабета. Иметь понятие об острых и поздних осложнениях сахарного диабета у детей, методах их профилактики и лечения. Сахарный диабет – это состояние хронической гипергликемии, обусловленной воздействием на организм многих экзогенных и эндогенных (генетических) факторов, нередко дополняющих друг друга (ВОЗ, 1985). ЭТИОЛОГИЧЕСКАЯ КЛАССИФИКАЦИЯ САХАРНОГО ДИАБЕТА (ВОЗ 1999) 1. Сахарный диабет типа 1 (деструкция бета клеток, обычно приводящая к абсолютной инсулиновой недостаточности) А. Аутоиммунный В. Идиопатический 2. Сахарный диабет типа 2 (от преимущественной резистентности к инсулину с относительной инсулиновой недостаточностью до преимущественного секреторного дефекта с инсулиновой резистентностью или без нее). 3. Другие специфические типы диабета А. Генетические дефекты бета-клеточной функции Б. Генетические дефекты в действии инсулина В. Болезни экзокринной части поджелудочной. Г. Эндокринопатии Д. Диабет, индуцированный лекарствами или химикалиями Ж. Необычные формы иммунно - опосредованного диабета З. Другие генетические синдромы, иногда сочетающиеся с диабетом 4. Гестационный сахарный диабет Нарушения толерантности к глюкозе а) улиц с нормальной массой тела б) у лиц с ожирением Классы статистического риска а) лица с предшествовавшим нарушением толерантности к глюкозе б) лица с потенциальным нарушением толерантности к глюкозе В клинической практике используется следующая классификация (таблица 19): Таблица 19. Клиническая классификация сахарного диабета степень тяжести состояние компенсации острые осложнения сахарного диабета поздние осложнения диабета легкая, среднетяжелая, тяжелая компенсация, субкомпенсация, декомпенсация гипергликемическая кетоацидотическая кома; гипергликемическая гиперросмолярная кома, гиперлактацидемическая кома микроангиопатии (ретинопатия, нефропатия); макроангиопатии (синдром диабетической стопы, инсульт, инфаркт миокарда и т.д.); нейропатия (полинейропатия, автономная нейропатия, энцефалопатия) осложнения инсули- гипогликемические состояния и гипогликемическая кома; аллергические нотерапии реакции на инсулин поражения других энтеропатия, катаракта, остеоартропатия, дермопатия; синдром Мориака органов и систем СД 1 типа возникает в результате деструкции β-клеток поджелудочной железы. Манифестация его происходит только при гибели 80 –90% всех клеток. Данный тип заболевания характерен для лиц молодого возраста. В настоящее время не вызывает сомнения аутоиммунный генез сахарного диабета. В крови больных ИЗСД обнаруживаются антитела к островкам Лангерганса, β -клеткам поджелудочной железы, белковым фрагментам капсулы β -клеток и т.д., кроме того, отмечается лимфоцитарная инфильтрация островков Лангерганса, что свидетельствует об активации клеточного звена иммунитета. В последнее время многими учеными подтверждается наличие генетического дефекта иммунной системы. Наиболее часто у больных ИЗСД встречаются гаплотипы HLA B8, HLA B15, аллели DR 3\DR 4. К факторам способствующим развитию сахарного диабета относятся вирусные инфекции, которые, с одной стороны, способствуют нарушению иммунной системы, а с другой непосредственно повреждают β-клетки поджелудочной железы. К группе так называемых диабетогенных вирусов относятся: вирус Коксаки и ECHO , вирус эпидемического паротита, кори, краснухи, энтеровирусы. Провоцировать манифестацию сахарного диабета у детей могут стрессовые ситуации, нарушение питания (избыток углеводов и жиров, недостаток белка). Пусковым механизмом патологических процессов при сахарном диабете у детей является инсулинопения, которая развивается у детей при гибели 85 –95 % β -клеток поджелудочной железы. Недостаток инсулина приводит к нарушению поступления глюкозы в клетки инсулинзависимых тканей (мышечной, жировой, печеночной). Гипергликемия приводит к повышению осмолярности плазмы и, следовательно, переходу жидкости из клеток и внеклеточного пространства в кровяное русло. У больного клинически отмечаются симптомы эксикоза (сухость кожи и слизистых). Повышение осмолярности крови приводит к увеличению по- чечной фильтрации, кроме того, гипергликемия преодолевает почечный порог глюкозы (индивидуальный показатель колеблется от 10 до 13 ммоль\л) и появляется во вторичной моче. Что приводит к повышению ее удельного веса и полиурии. Так как клетки инсулинзависимых тканей испытывают резкий энергетический дефицит, активируется комплекс контринсулярных гормонов (катехоламины, глюкокортикоиды, соматотропный гормон, глюкагон, тиреоидные гормоны), которые активируют распад гликогена (гликогенолиз) и усугубляют гипергликемию. Параллельно с распадом гликогена в качестве энергетического субстрата активно используются жиры (как эндогенные, так и экзогенные), что в условиях дефицита печеночных ферментов приводит к повышению кетогенеза, а также накоплению свободных жирных кислот в гепатоцитах (у больных отмечается увеличение печени и уплотнение ее структуры по УЗИ). Кетокислоты (ацетон, β -оксимасляная кислота, ацетоуксусная кислота), а также лактат, накапливающийся в результате нарушения в цикле Кребса способствуют развитию кетоацидоза (слабость, снижение внимания и памяти, появление запаха ацетона в выдыхаемом воздухе, ацетонурия). При сохраняющемся дефиците инсулина увеличивается катаболизм белка под действием глюкокортикоидов (активация ресинтеза глюкозы из аминокислотных остатков –глюконеогенез), что приводит к отрицательному азотистому балансу и повышению уровня азотистых шлаков в крови. В условиях отсутствия инсулина отмечается снижение поступления калия в клетки, кроме того, при сахарном диабете отмечается нарушение функции K / Na- АТФ - азы в почечных канальцах, что приводит к повышенной потере калия. У больных с декомпенсацией сахарного диабета уровень калия в крови может быть нормальным за счет гемоконцентрации, однако при проведении ЭКГ отмечаются признаки гипокалиемии. Развившийся кетоацидоз стимулирует дыхательный центр, в результате чего у больных появляется дыхание Куссмауля. Нарастающая дегидратация, ацидоз, кетоз способствуют формированию гиповолемического шока. В условиях кетоацидоза повышается токсическое влияние β-оксимасляной кислоты на головной мозг, что приводит к развитию комы. Основные клинические симптомы сахарного диабета у детей Полиурия Жажда Потеря массы тела Слабость Выраженные симптомы интоксикации Снижение аппетита Симптом «крахмального пятна» на белье Снижение успеваемости в школе При прогрессировании кетоацидоза: Боли в животе Нарушение зрения («туман», «мушки» перед глазами) Боли в мышцах Зуд кожи и слизистых Нарушение сознания Шумное, глубокое дыхание (дыхание Куссмауля) При осмотре ребенка с сахарным диабетом в стадии декомпенсации отмечается выраженная сухость кожных покровов и слизистых оболочек. Губы ярко-красного цвета, сухие. Язык сухой, обложен белым или бело-серым густым налетом, иногда отмечаются трещины на языке. Глаза запавшие, глазные яблоки мягкие. На фоне общей бледности, иногда с мраморным оттенком, кожных покровов выделяются ярко-красные щеки (диабетический рубеоз). Подкожный жировой слой снижен. Ребенок вялый, заторможенный, при развитии комы –без сознания. Дыхание глубокое, шумное, ритмичное. В акте дыхания участвует вспомогательная мускулатура. При аускультации в легких может выслушиваться жесткое дыхание, при присоединении вторичной инфекции – влажные хрипы. Тоны сердца приглушены, на пике интоксикации может выслушиваться систолический шум на верхушке. Характерна тахикардия. Артериальное давление обычно не изменено, однако, при развитии гиповолемического шока характерно его снижение. Живот чаще всего втянут, болезненный при пальпации, при выра- женном кетоацидозе могут быть положительными симптомы раздражения брюшины из-за мелкоточечных кровоизлияний в брюшину и раздражающего воздействия кетокислот. В общем анализе крови у детей с декомпенсированным сахарным диабетом отмечается повышение уровня гемоглобина и эритроцитов, может быть лейкоцитоз, нейтрофиллез. Характерно повышение гематокритного числа. Отмечается сокращение времени кровотечения и свертывания крови. В общем анализе мочи характерно повышение удельного веса, может быть протеинурия, лейкоцитурия и гематурия. Сахар мочи ++++. В зависимости от степени кетоацидоза в анализе мочи выявляется различная степень ацетонурии. В биохимических анализах крови характерно увеличение гликемии выше 6 ммоль\л, снижение рН, снижение содержания электролитов (за исключением калия, который может быть в норме за счет гемоконцентрации), может быть незначительное повышение мочевины, остаточного азота, креатинина. Диагностика сахарного диабета. При наличии характерной клинической картины, необходимо провести исследование гликемии: при уровне сахара крови до 5.6 ммоль/л диагноз сахарного диабета маловероятен. При уровне гликемии от 5,6 до10 ммоль/л необходимо определение глюкозы в крови натощак, при нормальных значениях проводится стандартный тест толерантности к глюкозе - если же уровень гликемии натощак не выше 10 ммоль/л, то проводят определение глюкозы в крови в течение суток с обычной пищевой нагрузкой. При уровне гликемии выше 10 ммоль/л диагноз сахарного диабета не подлежит сомнению. Методика проведения СГТТ: тест должен проводиться в спокойной обстановке. Не следует менять характер питания (ограничивать или исключать углеводы) в течение 3-х дней до проведения теста. Утром, натощак пациенту проводят определение гликемии. При уровне гликемии выше 6 ммоль\л тест не проводится! Затем ребенок выпивает раствор глюкозы, приготовленный из расчета сухого вещества 1,75 г/кг массы ребенка (при дефиците массы на фактическую, при избытке – на долженствующую) через 2 часа проводится повторное определение гликемии. Таблица 20 Диагностические критерии СТТГ Время определения гликемии Венозная кровь Капиллярная кровь сахарный диабет Натощак более 5,6 ммоль\л более 5,6 ммоль\л Через 2 часа более 10 ммоль\л более 11,1 ммоль\л нарушение толерантности к глюкозе (НТГ) Натощак менее 5,6 ммоль\л 5,6 –6,0 ммоль\л Через 2 часа 5,6 до 10 ммоль\л 7,8 –11,1 ммоль\л Лечение сахарного диабета у детей В настоящее время терапия сахарного диабета включает 3 равнозначных компонента: диетотерапию, инсулинотерапию, режим адекватных физических нагрузок. Диетотерапия. Энергетическая ценность суточного рациона у детей с сахарным диабетом не отличается от средних физиологических норм. Углеводы должны составлять не менее 50 % -60 % от суточной энергетической потребности, 25 –30 % составляют жиры и 15 -20% белки. Из питания детей с сахарным диабетом полностью исключается сахар, изделия из пшеничной муки тонкого помола. Углеводосодержащие продукты учитываются в рационе по системе хлебных единиц. 1 хлебная единица – это количество продукта, в котором содержится 12 грамм углеводов. В зависимости от количества углеводов в 100 гр. продукта можно рассчитать необходимое количество продукта для данного больного. В суточном рационе больного с сахарным диабетом должно быть достаточное количество клетчатки, которая поступает в основном с сырыми овощами и фруктами. Доказано, что употребление продуктов богатых клетчаткой вместе с углеводами снижает скорость их всасывания в кишечнике и уменьшает поступление в кровь. Вместо сахара больным сахарным диабетом можно употреблять в пищу сахарозаменители. Они делятся на две группы: калоригенные (ксилит, сорбит, фруктоза)– они также повышают сахара в крови и не используются в детской диабето- логии; и некалоригенные (производные аспартама –«Сладекс», «Суррель», «Ирбис»; препараты сахарина – «Свитли», «Сукразид», «Милфорд Тиа»; производные цикламата натрия – «Цукли»). Препараты 2 группы превосходят сахар по сладости в 200 –400 раз, поэтому для создания сладкого вкуса требуются малые дозы , которые не учитываются в суточном рационе. Инсулинотерапия. В детской диабетологии в настоящее время во всем мире используется схема «базис - болюсного» введения инсулина. У ребенка с сахарным диабетом нет эндогенного инсулина, и поэтому цель инсулинотерапии заместительная, т.е. имитирующая нормальное выделение инсулина. Достигается данная цель путем введения инсулина средней продолжительности действия 2 раза в сутки (утром и на ночь) – базальная инсулинотерапия и короткого инсулина 3 раза в день перед основными приемами пищи – пиковая инсулинотерапия. Данная схема является наиболее физиологичной, однако, и у нее есть некоторые недостатки. Продолжительность действия коротких инсулинов в среднем 4-6 часов, что может привести к развитию гипогликемических состояний через 2-2,5 часа после приема пищи, инсулины средней продолжительности действия также не являются безпиковыми, т.е. у них отмечается пик действия через 4-5 часов с момента введения, что часто приводит к ночным гипогликемиям. Для снижения риска развития гипогликемических состояний в дневное время в диетотерапии используют введение дополнительных приемов пищи – 2 завтрак, полдник, 2 ужин. В настоящее время для лечения детей используются аналоги инсулиновых препаратов – инсулины ультракороткого действия – Хумалог, Ново-Рапид, Апидра, которые начинают действовать сразу же после введения и продолжительность их действия не превышает 2 часов, что практически не отличается от действия эндогенного инсулина. Для создания постоянной концентрацими инсулина в сыворотке крови применяют пролонгированные безпиковые аналоги инсулина - Лантус и Левемир. Лантус действует 24 часа и вводится 1 раз в день в любое удобное для больного время. Левемир также не имеет пика действия, однако, продолжительность его действия в среднем 12 –14 часов, что диктует необходимость двухкратного введения данного инсулина. В последние 10 лет для терапии сахарного диабета 1 типа используются инсулиновые помпы, которые через миникатетер осуществляют непрерывное введение ультракоротких инсулинов с запрограммированной скоростью, что позволяет избегать частых инъекций инсулина. Режим физических нагрузок. Больные сахарным диабетом 1 типа нуждаются в ежедневных физических нагрузках под контролем гликемии. Предпочтительными видами спорта для них являются: теннис, легкая атлетика, лыжный спорт. Также достаточную физическую нагрузку обеспечивают занятия танцами. При проведении занятий необходимо проводить мониторинг гликемии с помощью глюкометра. При гликемии выше 13 ммоль/л занятия физическими упражнениями противопоказаны. При значениях сахара крови ниже 13 ммоль/л необходима дотация углеводов ежечасно в зависимости от уровня гликемии. Осложнения сахарного диабета Выделяют острые или ранние осложнения сахарного диабета (гипергликемические комы). Также к данной группе относятся осложнения инсулинотерапии- гипогликемические состояния и кома. К поздним осложнениям сахарного диабета относятся: микроангиопатии (диабетическая нефропатия и диабетическая ретинопатия), поражение нервной системы (полинейропатия и автономная нейропатия), поражение других органов и систем. Диабетическая нефропатия. Диабетическая нефропатия (ДН) является основной причиной смертности больных сахарным диабетом 1 типа. Патогенез развития ДН многофакторный. При сахарном диабете наблюдается дисфункция почечных сосудов – диаметр приносящей артериолы намного превышает диаметр выносящей, что приводит к резкому повышению внутриклубочкового давления. Кроме того, при прохождении через почечные клубочки мочи с повышенным содержанием сахара происходит прочное связывание глюкозы с белковыми молекулами. Имеющиеся нарушения приводят к повреждению эндотелия клубочков и нарушению их функции. Проявляется диабетическая нефропатия в виде появления микроальбуминурии, а затем, и протеинурии и прогрессирующего снижением функции почек. Диагностируется данное осложнение путем определения микроальбуминурии, проведения исследо- вания клиренса эндогенного креатинина, определения азотистых шлаков в крови. Для лечения данного осложнения используются ингибиторы ангиотензин-превращающего фермента (эналаприл, рамиприл) в суточной дозе от 2,5 мг до 10 мг под контролем артериального давления. На поздних стадиях диабетической нефропатии применяются плазмоферез, гемодиализ, пересадка почки. Диабетическая ретинопатия. Диабетическая ретинопатия начинает развиваться у больных с сахарным диабетом через 5 – 7 лет от манифестации заболевания. Развивается данное осложнение в результате поражения сосудов сетчатки повышающего их ломкость и приводящее к ретинальным кровоизлияниям. Сетчатки испытывает выраженный кислородный голод, что приводит к появлению новых сосудов – неоваскуляризации. Новообразованные сосуды отличаются повышенной ломкостью, что приводит к кровоизлияниям в сетчатку, таким образом, замыкая порочный круг. В области кровоизлияний образуются грубые рубцы и сращения со стекловидным телом, что может привести к отслойке сетчатки. Диагноз диабетической ретинопатии ставится на основании осмотра глазного дна при обязательном расширении зрачка. Лечение заключается в проведении лазерной фотокоагуляции сетчатки, что позволяет снизить потребность клеток в кислороде и замедлить снижение зрения. Диабетическая нейропатия. Диабетическая нейропатия развивается вследствие гликирования нейроцитов, а также клеток стенок интраневральных сосудов, что приводит к нарушению передачи импульса по нервным волокнам. Различают два основных вида нейропатии: сенсорно-моторную и автономную. Для сенсомоторной нейропатии характерно поражение чувствительных нервных волокон и моторных нервных волокон. Клинически данный вид нейропатии проявляется в виде парестезий по типу носок и перчаток, а также снижением всех видов чувствительности (болевой, температурной, тактильной и т.д.). Может быть болевой вариант нейропатии, характеризующийся резкими жгучими болями в конечностях. Автономная нейропатия связана с поражением вегетативной нервной системы. Выделяют следующие формы автономной нейропатии: а) желудочно-кишечная (нарушение моторики желудочно-кишечного тракта – рефлюксы, дискинезии, немотивированные ночные поносы). б) мочеполовая (нарушение уродинамики, атония мочевого пузыря, недержание мочи, импотенция). в) кардиоваскулярная (тахикардия покоя, «ригидный сердечный ритм», аритмии, ортостатический коллапс, головокружения, безболевая ишемия миокарда). г) снижение чувствительности к гипогликемическим состояниям. д) гипергидроз при еде, дисгидроз конечностей. Диагностика поражений нервной системы проводится невропатологом путем проведения специальных тестов, электромиографии. Лечение данного осложнения проводится препаратами, улучшающими метаболизм нервного волокна: препаратами липоевой кислоты (липамид, эспа-липон, берлитион); витаминными препаратами (витамины группы В, жирорастворимые формы витамина В1 – бенфотиамин). Синдром Мориака. Встречается только у детей и подростков с сахарным диабетом и характеризуется резким снижением темпов физического и полового развития, гепатомегалией. Острые осложнения сахарного диабета. У детей наиболее часто развиваются гипергликемическая кетоацидотическая кома и гипогликемическая кома. Кетоацидотическая кома. Данное осложнение часто развивается у детей в дебюте сахарного диабета. При наличие данного заболевания к развитию кетоацидоза и кетоацидотической комы могут привести следующие причины: снижение дозы инсулина или прекращение инсулинотерапии; острые инфекционные заболевания; стрессы и оперативные вмешательства. Развитие кетоацидоза достаточно медленное, в течение нескольких дней. Ранними клиническими симптомами являются признаки декомпенсации диабета, при отсутствии адекватного лечения к ним присоединяются признаки кетоацидоза (тошнота, резкая слабость, сонливость, появление запаха ацетона в выдыхаемом воздухе, дыхание Куссмауля). У больного нарастает угнетение ЦНС, конечной стадией которого является кома. При исследовании крови отмечается гипергликемия, гиперкетонемия, повышение мочевины и мочевой кислоты, остаточного азота, снижение уровня калия, признаки метаболического ацидоза. В моче глюкозурия, ацетонурия, протеинурия. Лечение кетоацидотической комы осуществляется в отделение реанимации или палате интенсивной терапии. Проводится ежечасное определение сахара крови и мочи, рН крови, подсчет ЧСС, ЧД; определение электролитов крови каждые 2 часа; проведение ЭКГ. Обязательно налаживается оксигенотерапия. Вводимые растворы должны быть подогреты до 37°С. Проводится регидратационная терапия из расчета: 50 –150 мл/кг в зависимости от тяжести комы, которую осуществляют введением изотонического раствора натрия хлорида. В первые 6 часов лечения вводят 50% от рассчитанного суточного объема, в следующие 6 часов – 25%, и оставшиеся 25% жидкости вводится в течение 12 часов. При достижении уровня гликемии 14ммоль\л изотонический раствор натрия хлорида заменяется на введение 5% раствора глюкозы, чередуемого с 0,9% Na Cl. При изначально низком уровне АД инфузионную терапию начинают плзмозамещающими растворамми с низкой молекулярной массой (Рефортан 6%, Стабизол, Стерофундин). Параллельно с регидратацией проводится инсулинотерапия. Вводится только инсулин короткого действия. Первоначальная доза инсулина составляет 0,1 ЕД/кг массы тела (при длительном существовании сахарного диабета эта доза может быть увеличена до 0,2 –0,4 ЕД/кг). Первая доза инсулина вводится внутривенно струйно в 10 –20 мл изотонического раствора натрия хлорида, затем проводится внутривенное капельное введение инсулина на физ. растворе в дозе 0,1 Ед/кг час. При достижении уровня гликемии 12 – 14 ммоль\л доза вводимого инсулина составляет: 0,03 –0,06 Ед\кг·час. Необходимо проводить коррекцию электролитных нарушений, особенно гипокалиемии с помощью введения раствора калия хлорида из расчета 0,2 –0,3 г сухого калия хлорида на кг массы с каждым литром вводимой жидкости. При снижении уровня рН проводится коррекция кислотно-щелочного равновесия путем введения 4% раствора гидрокарбоната натрия из расчета 2,5 мл\кг массы тела. Вводятся кокарбоксилаза, аскорбиновая кислота, панангин. Наиболее грозным осложнением кетоацидоза является отек мозга. Он проявляется через 4 –6 часов от начала лечения. Характерно ухудшение состояния, выраженная головная боль, головокружение, тошнота, рвота, нарушение зрения, напряжение глазных яблок, лихорадка судороги. Лечение представляет значительные трудности: замедляется скорость введения жидкости в два раза, вводится раствор маннитола из расчета 1 –2 г\кг массы, можно ввести 20 – 40 мг лазикса. также возможно введение дексаметазона из расчета 0,5 мг\кг. Гипогликемическая кома. В отличие от гипергликемической комы гипогликемия развивается в течение нескольких часов. Развитию данного осложнения способствуют: снижение потребляемой пищи при неизменной дозе инсулина, необычно высокая физическая нагрузка, употребление алкоголя, нарушение функции печени. У больных появляется резкое чувство голода, изменение настроения (может быть как эйфория, так и резкий негативизм), больной становится капризным, появляется тремор конечностей и всего тела, нарушение зрения (диплопия, ощущения тумана перед глазами). При отсутствии адекватной помощи сознание больного снижается, появляется тризм жевательной мускулатуры, судороги. Для купирования гипогликемии в начале ее развития необходимо дать больному углеводистую пищу из расчета 1-2 ХЕ (стакан молока, сока, кусочек хлеба, кашу, картофельное пюре, фрукты). При появлении гипогликемии в транспорте можно дать ребенку конфету или 1 –2 кусочка сахара. При сохраняющихся симптомах гипогликемии повторно произвести дачу углеводов через 20 –30 мин. При отсутствии сознания проводят внутривенное струйное введение 40% раствора глюкозы 20 –80 мл и/или глюкагон подкожно. При неэффективности проводимой терапии вводится преднизолон 1 мг/кг. Вопросы для тестового контроля № п/п 1. 2. Содержание вопросов К контринсулярным гормонам относятся: а) паратгормон, б) тироксин, в) глюкогон, г) холецистокинин, д) адреналин К инсулинам короткого действия относятся: а) хумулин Н, б) суспензия цинк- Эталоны ответов б, в, д в, д 3. 4. 5. 6. 7. 8. 9. 10. инсулина, в) хумулин R, г) протофан, д) актрапид Основные симптомы сахарного диабета у детей: а) ожирение, б) жажда, в) полиурия, г)судороги, д) появление стрий на коже К поздним осложнениям сахарного диабета у детей относятся: а)синдром диабетической стопы, б) ретинопатия, в) гиперлактацидемическая кома, г)нефропатия, д) иридоциклит Для кетоацидотической комы характерно: а) сухость кожных покровов, б) повышение артериального давления, в) гипергидроз ладоней, г)глубокое, шумное дыхание, д) запах ацетона в выдыхаемом воздухе Для гипогликемической комы характерно: а) быстрое развитие симптомов, б) выраженная сухость кожи, в) полиурия, г) повышенная судорожная готовность, д) запах ацетона в выдыхаемом воздухе Для диагностики диабетической нефропатии необходимо использовать: а)определение сахара в моче, б) пробу Реберга, в) определение микроальбуминурии, г) экскреторную урографию, д) микционную цистографию К некалоригенным сахарозаменителям относятся: а) акарбоза, б)сорбит, в) ксилит, г) аспартам, д) сахарин Доза глюкозы при проведении стандартного теста толерантности к глюкозе: а) 1г/кг, б) 1,75 г/кг, в) 75 г, г) 100 г, д) 100 мг/кг Начальная доза инсулина при выведении больного из кетоацидотической комы составляет: а) 1 ЕД/кг, б)2 ЕД/кг, в) 0,1 ЕД/кг, г) 0,8 ЕД/кг, д) 10 –20 ЕД б, в б, г а, г, д а, г б, в г, д б в Ситуационные задачи № п/п 1 Содержание задач Эталоны ответов Девочка 10 лет поступила в приемное отделение центральной районной больницы в тяжелом состоянии. Ребенок доставлен бабушкой, у которой девочка гостила последние 6 дней, поэтому подробный семейный анамнез и анамнез данного заболевания уточнить невозможно. Бабушка отметила, что девочка значительно похудела за последние 3 месяца. В течение недели она стала вялая, жаловалась на головные боли, слабость, отсутствие аппетита, много пила жидкости (до 3-4 литров в сутки), ночью отмечался энурез. Накануне вечером у ребенка была двухкратная рвота, не связанная с приемом пищи. Утром не смогла встать с постели из-за сильной слабости, была сонлива, неохотно разговаривала с окружающими, отмечалась рвота выпитой жидкостью 3 раза, боли в животе без четкой локализации. Участковым педиатром заподозрен острый аппендицит и вызвана машина "Скорой помощи". При осмотре в приемном покое девочка на вопросы не отвечает, рефлексы сохранены. Кожные покровы и видимые слизистые сухие, яркая гиперемия слизистой губ. Кожа с "мраморным" оттенком на конечностях, отмечается яркая гиперемия щек. Подкожный жировой слой резко истончен. Дыхание глубокое, ритмичное, шумное. "Фруктовый" запах в выдыхаемом воздухе. ЧД 32 в минуту. В легких дыхание проводится по всем полям, жесткое. Сердечные тоны приглушены, ЧСС 120 в минуту, АД 80/40 1.Сахарный диабет, инсулинзависимый (1 тип), тяжелое течение, стадия декомпенсации. Кетоацидотическая кома. Диагноз сахарного диабета выставлен на основании жалоб на потерю массы тела, полидипсию, полиурию (о чем свидетельствует энурез), слабость, снижение аппетита, головные боли. Данных осмотра: сухость кожи и слизистых, снижение подкожного жирового слоя. Результатов обследования: признаков сгущения крови в виде повышения гемоглобина и форменных элементов крови на фоне замедленного СОЭ; повышения сахара крови до 28 ммоль/л. Диагноз кетоацидотической комы подтверждается отсутствие сознания, наличием симптомов эксикоза, дыхания Куссмауля, запаха ацетона в выдыхаемом воздухе, яркой гиперемией щек (диабетический рубеоз), тахикардией и снижением артериального давления. 2.В течение первых суток необходимо провести следующие исследования: сахар крови и мочи ежечасно, ацетон мочи ежечасно, подсчет гематокритного числа, определение тромбоцитов, времени свертывания крови, кровоточивость, определение КЩС крови, определение электролитов крови, ЭКГ, общий анализ мочи, печеночные пробы, определение мочевина, мочевой кислоты, креатинина крови 3. В первый час лечения: инсулин короткого действия (актрапид, хумулин Р) в дозе 0,1 Ед/кг, что составит 2 ЕД в/в струйно на 20 мл 0,9 % раствора хлорида натрия; реополиглюкин (альбумин 10%) для купирования ангидреми-ческого шока в дозе 10 мл/кг , мм.рт.ст. Пульс слабого наполнения и напряжения, ритмичный. Живот напряжен, пальпация затруднена из-за напряжения мышц передней брюшной стенки. Печень определяется перкуторно на +2,5 см ниже реберной дуги. В течение последних 4 часов девочка не мочилась. Вес 20 кг. Проведено обследование: Общий анализ крови: Hb 145 г/л, эр. 5,1 ·10 12 /л, Le 10,2 · 10 9 /л, э – 2%, п –1 %, сегм. - 57%, лимф. –26%, мон. – 4%, СОЭ – 5 мм/час. Глюкоза крови – 28 ммоль/л. Вопросы: 1.Поставить предварительный диагноз и дать его обоснование. 2. Какие исследования необходимо провести данной больной в первые сутки лечения? 3.Составьте план лечения на первый час и на первые сутки. 2 В больницу доставлен ребенок 8 лет в бессознательном состоянии. Из беседы с мамой выяснено, что мальчик болеет сахарным диабетом в течение 5 лет, постоянно получает инсулинотерапию в "базисболюсном" режиме. Сегодня вечером после обычной инъекции инсулина отказался от ужина, съел салат из капусты и выпил стакан чая. После ужина в течение 2 часов играл в футбол. Перед сном был возбужден, громко разговаривал, отмечалась выраженная эмоциональная лабильность. Спал неспокойно, вскрикивал, в 2 часа ночи на фоне диффузного гипергидроза появились тонико - клонические судороги. Была вызвана бригада «Скорой помощи», введен реланиум внутримышечно, судороги купировались, однако ребенок был без сознания. Доставлен в детскую больницу. При осмотре: состояние тяжелое, без сознания. Кожные покровы бледные, холодные, резкий гипергидроз. Повышенная судорожная готовность. Дыхание поверхностное, ЧД 24 в мин. Cor: тоны приглушены, ЧСС 128 в мин., АД 100/50 мм. рт. ст. Живот мягкий, безболезненный. Проведено обследование: сахар крови – 2,1 ммоль/л, сахар мочи отрицательный. Вопросы: 1.Диагноз и его обоснование. 2.Что по вашему мнению привело к развитию данного состояния у ребенка? 3.Какое лечение необходимо было провести данному ребенку на догоспитальном этапе? Какое лечение необходимо назначить при поступлении в стационар? что составит 200 мл в/в струйно; 0,9% раствор натрия хлорида в/в капельно из расчета 10 мл/кг, что составит 200 мл, в капельницу добавить 150 мг кокарбоксилазы и 2 мл 5% раствора аскорбиновой кислоты; гепарин в/в струйно на физ. растворе в дозе 750 Ед ( из расчета 150 Ед/кг/сут в 4 приема. В первые сутки: инсулин короткого действия из расчета 0,1 ЕД/кг/час до снижения уровня гликемии до 14 ммоль/л, затем 0,03 –0,06 ЕД/кг/час; инфузионная терапия из расчета 2000 мл/сут, до снижения гликемии до 14 ммоль/л вводится физ.раствор, затем чередуется введение физ.раствора и 5% глюкозы; коррекция ацидоза: вводится 4% гидрокарбонат натрия из расчета 2 мл/кг, что составит 40 мл в/в капельно под контролем КЩС; коррекция гипокалиемии введением калия хлорида из расчета 0,2 –0,3 г сухого калия хлорида на кг массы (4,0 – 6,0 г), что при применении 4% раствора составит соответственно 100 – 150 мл, а при применении 7,5 % раствора 53,0 мл – 80,0 мл. 1. Сахарный диабет, инсулинзависимый, тяжелое течение, стадия декомпенсации. Гипогликемическая кома. 2. Развитие гипогликемического состояния, а затем и гипогликемической комы было обусловлено нарушением диеты (отсутствие поступления углеводов), увеличением физической нагрузки. 3. На догоспитальном этапе необходимо было дать ребенку раствор глюкозы per os (сладкий чай, сок). Во время транспортировки бригадой «Скорой помощи» ввести внутривенно струйно 40% раствор глюкозы до выхода из комы. При поступлении в стационар необходимо назначить раствор глюкозы 40% в/в струйно до выхода из комы, при неэффективности ввести глюкагон п/к и/или преднизолон из расчета 1-2 мг/кг в/м. Рекомендуемая литература: Основная: 1. Дедов И.И., Петеркова В.А. Детская эндокринология. М.: УП-Принт, 2006. – 595 с. Дополнительная: 1. Никитина И. Л. Детская эндокринология. Ростов на Дону, «Феникс», 2006. – 224с. 2. Самошкина Е.С, Солдатов О.М. Неотложные состояния при сахарном диабете у детей. Методические указания для студентов лечебного и педиатрического отделений, Саранск, 2001. –20с. Занятие № 11. ОСТРЫЕ РЕСПИРАТОРНЫЕ ВИРУСНЫЕ ИНФЕКЦИИ. МЕНИНГОКОККОВАЯ ИНФЕКЦИЯ. Цель занятия: изучить особенности эпидемиологии, клиники гриппа и других ОРВИ у детей (в дифференциально-диагностическом плане); ознакомиться с различными клиническими вариантами менингококковой инфекции, освоить лечебную тактику при менингококкцемии на догоспитальном этапе, а также основы интенсивной терапии при генерализованных формах менингококковой инфекции (МИ). Вопросы для самоподготовки: 1. Возрастные особенности реактивности детского организма. 2. Особенности клиники, течения, эпидемиологии и диагностики острых респираторных вирусных инфекций у детей. 3. Грипп. Этиология, эпидемиология, клиника, лечебная тактика. 4. Дифференциально-диагностические симптомы гриппа, парагриппа, аденовирусной, респираторно-синцитиальной и риновирусной инфекции. 5. Этиология, эпидемиология и классификация менингококковой инфекции. 6. Особенности клинической картины различных форм МИ у детей. 7. Лечебная тактика догоспитального этапа и интенсивная терапия генерализованных форм МИ у детей. Острые респираторные вирусные инфекции (ОРВИ) – объединяют большую группу высококонтагиозных острых вирусных болезней, характеризующихся общими симптомами интоксикации и поражением слизистых оболочек различных отделов респираторного тракта. К ОРВИ относятся: грипп, парагрипп, аденовирусная, риновирусная, респираторносинцитиальная, риновирусная инфекции и некоторые другие. Заболеваемость ОРВИ высокая, резко возрастает во время эпидемических вспышек и остается значимой среди всех инфекций и в межэпидемический период среди детей. Летальность при неосложненных формах равна нулю и становится значительной при тяжелых осложненных формах во время эпидемий гриппа. Классификация: - По клинической форме: манифестные и стертые, бессимптомные. - По тяжести: легкая, среднетяжелая, тяжелая. - По течению: неосложненные и осложненные. - По локализации процесса: ринит, аденоидит, синусит, отит, евстахиит, фарингит, тонзиллит, ларингит, трахеит, бронхит, бронхиолит, пневмония. - Осложнения: специфические (стеноз гортани, обструктивный бронхит, дыхательная недостаточность, вирусные поражения ЦНС, сердца, почек); неспецифические в виде присоединения вторичной бактериальной инфекции (пневмония, отит, ларингит, бронхит, трахеит, плеврит, тонзиллит, синуситы, а также обострение хронических соматических заболеваний). Грипп – чрезвычайно заразное острое инфекционное заболевание, характеризующееся симптомами выраженной интоксикации, катаром верхних дыхательных путей, частым развитием осложнений, обусловленных вторичной бактериальной флорой. Этиология. Возбудитель гриппа относится к семейству ортомиксовирусов, имеет относительно большие размеры и содержит РНК. Выделяют 3 серотипа вируса: А,В,С. Принадлежность к определенному подтипу обусловлена наличием антигенов: гемагглютинина (13 подтипов) и нейроминидазы (10 подтипов). Вирусы гриппа устойчивы к низким температурам и замораживанию, быстро погибают при нагревании. Эпидемиология. Источник инфекции – больной человек (в том числе типичными, стертыми формами, так как они не изолируются от коллектива). Путь передачи преимущественно воздушно-капельный, значительно реже контактно-бытовым: через игрушки, соски, посуду. Восприимчивость к гриппу всеобщая. После перенесенного заболевания формируется нестойкий типоспецифический иммунитет. Возможно суперинфицирование или повторное заболевание особенно у ослабленных детей. Клиника. Инкубационный период составляет при гриппе А – 12-48 часов, при гриппе В – до 3-4 суток.Различают следующие клинические формы болезни: 1) типичный грипп – по тяжести его подразделяют на легкую, среднетяжелую и тяжелую (токсическую) формы; 2) атипичный грипп (гипертоксическая и стертая формы). Типичный грипп у детей младшего и старшего возраста начинается внезапно, без продромы, с подъемом температуры до высоких фебрильных цифр, сопровождается ознобом, общим недомоганием, тянущими болями в мышцах. Затем появляется головная боль, преимущественно в области лба, надбровных дуг, боль в глазных яблоках, животе и пояснице. Ребенок или очень вял (лежит «пластом») или возбужден, бредит. Лицо гиперемировано, склеры инъецированы. Характерно доминирование симптомов интоксикации над катаральными явлениями. В первые два дня катаральные явления отсутствуют или слабо выражены (заложенность носа, отечность и зернистость слизистых мягкого неба, инъекция сосудов миндалин). Имеются выраженные признаки трахеита, характеризующегося сухим, мучительным кашлем и болями за грудиной по ходу трахеи. Со стороны легких у больных гриппом выслушиваются кратковременные сухие хрипы. Определяется тахикардия, выслушиваются громкие, напряженные тоны, АД повышено. Лимфоузлы мало реагируют, печень и селезенка не увеличены. Со стороны крови при гриппе в первые дни: лейкопения, лимфоцитоз, эозинофилия, нормальная СОЭ или несколько повышена. Такое состояние продолжается от нескольких часов до 3-х суток, затем появляется насморк, кашель с мокротой, резкая слабость, потливость, при неосложненном течении болезни температура литически снижается, исчезают симптомы интоксикации, в то время как астенический синдром может сохраняться до 10-14 дней. У новорожденных и детей первого года жизни течение гриппа имеет ряд особенностей: постепенное начало, симптомы интоксикации и катаральные явления нерезко выражены, отказ от груди, падение массы тела, высокая летальность. Для гипертоксической формы гриппа (наблюдается чаще у детей 1-3 лет) характерны гипертермический, менингоэнцефалитический, геморрагический синдромы, молниеносное течение и летальный исход. При стертой форме ребенок остается практически здоровым, однако имеется нарастание титра антител к вирусу гриппа. Осложнения при гриппе могут возникнуть в любые сроки от начала болезни. Наиболее часто встречаются риниты, фарингиты, ларингиты, трахеиты, бронхиты, бронхиолиты; к госпитализации и смертности приводят синуситы и пневмония (вирусная и бактериальная); обострения хронических заболеваний сердца, легких, почек на фоне инфекции Диагноз. Опорными диагностическими признаками гриппа являются: 1) указание на контакт; 2) острое начало с симптомов интоксикации; 3) достижение максимума развития интоксикации в первые двое суток; 4) появление скудных катаральных явлений на 1-2 дня позже симптомов интоксикации; 5) лейкопения, нормоцитоз, сдвиг лейкоформулы влево. Лечение. Обязательной госпитализации подлежат дети с тяжелыми формами гриппа, а также с осложненным течением. При легких и среднетяжелых формах проводят симптоматическую терапию: жаропонижающе средства, которые назначаются ранее здоровым детям в возрасте старше 3 месяцев: при температуре >39,0 ºС, и/или при дискомфорте, мышечной ломоте и головной боли, детям с фебрильными судорогами в анамнезе, с тяжелыми заболеваниями сердца и легких, а также детям 0-3 месяцев жизни: при температуре >38-38,5 ºС. Наиболее безопасным жаропонижающим для детей является, парацетамол, его разовая доза - 10-15 мг/кг, суточная - 60 мг/кг. Ибупрофен 5-10 мг/кг на прием также эффективен, но он чаще да- ет побочные эффекты, чем парацетамол. Противовирусные препараты назначают с первых часов заболевания. Основная цель лечения ринита - улучшение носового дыхания. При остром рините у детей не рекомендуется применять сосудосуживаюшие препараты короткого действия: эфедрин, нафазолин и тетризолин из-за возвратного отека слизистой оболочки носа. Предпочтение отдается сосудосуживающим препаратам более длительного действия: оксиметазолин, ксилометазолин. Сосудосуживающие капли используют первые 3 дня, при более длительном применении они могут усиливать насморк, а также вызывать побочные явления. В раннем возрасте используют 0,01% и 0,025% растворы. Детям старше 6 лет можно назначать назальные спреи, позволяющие при меньшей дозе равномерно распределить препарат. Наиболее эффективными и безопасными являются препараты на основе морской воды (Аквамарис, Маример, Аквалор и.т.д.). Из оральных средств от насморка следует использовать не содержащие симпатомиметики (фенилэфрин, псевдоэфедрин) препараты, например, Фервекс для детей. Основным противогриппозным средством, действующим также и на ряд других вирусов, является ремантадин, который подавляет репродукцию всех штаммов гриппа типа А. Ремантадин также ингибирует репродукцию респираторно-синцитиальных (РС) и парагриппозных вирусов. Рекомендуется; 5-дневный курс из расчета 1,5 мг/кг/сут в 2 приема детям 3–7 лет; по 50 мг 2 раза детям 7–10 лет - 3 раза в сутки - старше 10 лет. В раннем возрасте ремантадин используют в виде альгирема (0,2% сироп): у детей 1–3 лет по 10 мл; 3–7 лет - по 15 мл: 1-й день 3 раза, 2–3-й дни - 2 раза, 4-й - 1 раз в день. Также возможно назначение арбидола, ингибирующего слияние липидной оболочки вирусов гриппа с мембраной эпителиальных клеток и являющегося индуктором интерферона: детям 2–6 лет по 50 мг на прием, 6–12 лет по 100 мг, старше 12 лет - по 200 мг на прием 4 раза в сутки. При тяжелом течение возможно назначение ингибиторов нейраминидазы: осельтамивира (Тамифлю) или занамивира (Реленза). Тамифлю разрешен к применению у детей с 1 года: детям весом до 15 кг назначают по 30 мг 2 раза в день, с массой тела 15-23 кг по 45 мг 2 раза в день, с массой 23-40 кг по 6мг 2 раза в день, детям с массой более 40 кг, подросткам и взрослым назначается по 75 мг 2 раза в день в течение 5 дней. Возможно назначение гриппферона, эффективность которого максимальна в первые часы заболевания- вводят в виде капель в нос в течение 5 дней, детям до года — по 1 капле 5 раз в день (разовая доза 1000 МЕ, суточная доза - 5000 МЕ), детям от 1 до 3 лет по 2 капли 3–4 раза в день (разовая доза 2000 МЕ, суточная - 6000–8000 МЕ), от 3 до 14 лет — по две капли 4–5 раз в день (разовая доза - 2000 МЕ, суточная – 8000-10 000 МЕ). Профилактика. Большое значение для профилактики заболевания в коллективе имеет ранняя изоляция больного гриппом. В эпидочагах эффективно применение препаратов интерферона. Детям старшего возраста можно использовать ремантадин (25 мг 2-3 раза в день 3 дня). В настоящее время широко используются гриппозные вакцины (Ультравак, Моногриппол, Гриппол, Инфлювак, Бегривак). Дифференциально-диагностические симптомы гриппа, парагриппа, аденовирусной, респираторно-синцитиальной и риновирусной инфекций приведены в таблице 21. Таблица 21 Дифференциально-диагностические симптомы гриппа и других острых респираторных заболеваний (Кубарь О., Злыдников Д., 1988, с изменениями) Признак 1. Начало заболевания 2. Симптомы интоксикации 3. Лихорадка 4. Катаральные явления 5. Лимфаденит 6.Гепатомегалия 7. Внешний вид 8. Осложнения 9.Специфическое лечение 10. Профилактика Грипп Внезапное, острое Доминируют (сильная головная боль, боль в глазах, мышцах, озноб, вялость, «разбитость», тошнота, рвота) Высокая с 1-го дня Выражены со 2-3-го дня: заложен нос, выделения из носа, кашель сухой, сухость и першение в горле Региональный, редко Нет Одутловатость, гиперемия лица, склерит Бронхит, пневмония, со стороны ЛОР-органов, нервной и сердечнососудистой систем, почек; обострение хронических заболеваний Ремантадин, арбидол, иммуноглобулин, в перспективе – адапромин, дейтифорин Вакцинопрофилактика, ремантадин, арбидол и др Парагрипп Аденовирусная инфекция РС-вирусная инфекция Риновирусная инфекция Постепенное, реже острое Слабо выражены (головная боль, однократная рвота) Постепенное и острое Острое и постепенное Острое выражены умеренно или сильно (умеренная головная боль, слабость) Слабо выражены (умеренная головная боль, слабость) Отсутствуют Субфебрильная с постепенным развитием Выражены с первого дня: кашель сухой, грубый, осиплость голоса, слабая гиперемия зева Нет Нет Обычный Высокая, длительная Умеренная с постепенным развитием Выражен сухой кашель, явления бронхообструкции, бронхиолит Отсутствует или субфебрильная Резко выражены: обильное слизистое отделяемое из носовых ходов, чихание, слабая гиперемия зева Нет Нет Мацерация кожи возле носовых отверстий Со стороны ЛОР-органов; обострение хронических заболеваний Бронхит, обострение хронических заболеваний Интерферон, иммуноглобулин Нет Выраженные с экссудативными проявлениями выделения из носа, яркая гиперемия зева, отек миндалин, налеты, конъюнктивит Часто, генерализованный Бывает Бледность отечность лица, конъюнктивит Ангина, отит, синусит, миокардит; обострение хронических заболеваний Мазь флореналь, бонафтоновая, теброфеновая, интерферон, иммуноглобулин Нет Бывает региональный Бывает Бледность кожных покровов Пневмония, обострение хронических заболеваний Иммуноглобулин, интерферон Нет Интерферон Нет Менингококковая инфекция – острое инфекционное заболевание, протекающее в виде локализованных (назофарингит, носительство) и генерализованных форм (гнойный менингит, менингококкемия) и смешанные формы, представляющие сочетание менингита и менингококкцемии. У детей встречаются в основном генерализованные форы менингококковой инфекции. Этиология. Возбудитель – менингококк (грамотрицательный диплококк). Различают несколько серогрупп менингококка A, B, C, D и другие. Микроб не устойчив, быстро погибает во внешней среде. Большинство штаммов менингококка чувствительны к пенициллину, левомицетину, эритромицину и тетрациклину. Вирулентные свойства менингококка определяются эндотоксином. Эпидемиология. Менингококковая инфекция относится к антропонозам, к группе капельных инфекций. Источником инфекции является больной и носители. Механизм передачи – воздушно-капельный (аэрозольный). Контагиозный индекс составляет 10-15%. Продолжительность иммунитета точно не установлена. В невосприимчивости немалая роль принадлежит бытовой иммунизации (носительство менингококка). Иммунитет после перенесенного заболевания достаточно стойкий, типоспецифический, поэтому повторные заболевания редки. Классификация: По форме: локализованная – назофарингит; генерализованная – менингит, менингоэнцефалит, менингококкемия, смешанные формы; редкие формы – пневмония, артрит и др. По тяжести: легкой, средней степени и тяжелая. По течению: гладкое (неосложненное) и осложненное. Осложнения: острая надпочечниковая недостаточность – синдром УотерхаузаФридериксена, отек мозга с вклинением, эпендиматит, гидроцефалия, пневмония, отит и др. Клиника. Диагностировать менингококковый назофарингит на основании клинической картины, без указания на соответствующий эпиданамнез, затруднительно. В клинической картине заболевания наиболее типичными симптомами являются заложенность носа, першение в горле, гиперемия и отечность задней стенки глотки с гипертрофией лимфоидных образований на ней, отечность боковых валиков и слизь в небольшом количестве. Гиперемия имеет синюшный оттенок. Менингококковый менингит среди генерализованных форм встречается до 40%. Заболевание развивается остро, бурно, даже у детей первого года жизни. Температура в первые часы достигает 39-40°С. Преобладающими симптомами у детей раннего возраста являются: повторная рвота (часто не связанная с приемом пищи), психомоторное возбуждение, судороги, гиперестезия. Наиболее существенные (ранние) признаки внутричерепной гипертензии – выбухание и напряжение большого родничка, положительный симптом Лессажа («подвешивания»), гиперкинезы (тремор рук). У старших детей определяются менингеальные симптомы (ригидность затылочных мышц, симптомы Брудзинского, Кернига). В периферической крови - лейкоцитоз, сдвиг лейкоформулы влево до палочкоядерных форм и метамиелоцитов, значительное ускорение СОЭ (до 30-40 мм в час). При исследовании мочи часто выявляются альбуминурия, цилиндрурия, появляются эритроциты. Спинномозговая жидкость опалесцирующая или мутная (белого, желтоватого или желто-зеленого цвета). Количество клеток увеличено, как правило, до нескольких тыс. в 1 мкл, преимущественно за счет нейтрофилов (до 70100%). Общее содержание белка в ликворе повышается до 0,6-1,0 г/л и больше. Уровень сахара и хлоридов может быть понижен. Среди генерализованных форм различают менингококцемию, которая может протекать в легкой, среднетяжелой, тяжелой и молниеносной формах в виде менингококкового сепсиса; менингококковый менингит и менингококцемию + менингит. Для менингококцемии характерно острое, внезапное начало, быстро нарастает температура (до 39-40°С), интоксикация (беспокойство, затем вялость, нечастая рвота, снижение аппетита). Критериями тяжести являются степень выраженности интоксикации, характер, величина, рас843 пространенность, наличие некрозов и продолжительность элементов сыпи, из которых может высеваться менингококк. У большинства больных сыпь появляется сначала на нижней половине тела. Типичная локализация – нижние конечности, ягодицы, бедра, живот. При легкой форме элементы представлены розеолами, папулами, мелкими геморрагиями, которые бесследно исчезают к 3-му дню болезни. При среднетяжелой форме элементы преимущественно крупные, геморрагические, звездчатой формы, часто с поверхностным некрозом в центре. Сыпь более продолжительная — до 7–10 дней. Для тяжелых и септических молниеносных форм характерны обширные кровоизлияния на коже с глубокими некрозами и их отторжением, при которых могут формироваться косметические дефекты на теле. Эти формы часто сопровождаются кровотечениями: маточными, носовыми, желудочно-кишечными, а также кровоизлияниями на глазном дне. Отмечаются поражения сердца (эндокардит, миокардит, панкардит), суставов, легких, печени, почек, надпочечников. Гипертоксическая (молниеносная, злокачественная) форма менингококцемии протекает с развитием ИТШ, который связан с массивной бактериемией, интенсивным распадом микробов и токсинемией. На первый план при шоке выступают нарушения гемодинамики, особенно на микроциркуляторном уровне. Этой форме свойственно острейшее начало (гипертермия, озноб, рвота, психомоторное возбуждение, быстро сменяющееся угнетением ЦНС), раннее появление геморрагической сыпи (через 6-12 часов от начала заболевания), множественные высыпания (в центре с некрозом), которые быстро, буквально на глазах, сливаются, образуя обширные геморрагии багрово-цианотичной окраски, напоминающие трупные пятна. Температура снижается, отмечаются бледность, одышка, выраженная тахикардия , конечности становятся холодными, пульс нитевидный или вообще не прощупывается. Систолическое артериальное давление снижается до 40-60 мм рт. ст., диастолическое – до 20-10 мм рт. ст. Характерна олигурия. При обширных кровоизлияниях в надпочечники развивается синдром УотерхаусаФридериксена (острая надпочечниковая недостаточность), проявляющийся резким снижением артериального давления, нитевидным пульсом, аритмией, поверхностным неритмичным дыханием, олигурией, развитием тробомбогеморрагического синдрома. При этом элементы сыпи быстро сливаются, образуя обширные геморрагии, багрово-цианотичной окраски, напоминающие трупные пятна. По степени нарушения гемодинамики и микроциркуляции (особенно в надпочечниках, почках, легких) выделяют три степени ИТШ. Для ИТШ I степени характерны гипертермия, тахикардия, быстрое нарастание высыпаний; для ИТШ II степени – умеренное снижение АД, часто нормальная температура, олигурия, обильные высыпания, сопровождающиеся некрозами, особенно на ягодицах и ногах; для ИТШ III степени – падение АД, особенно диастолического (до 10 мм рт. ст.), холодный пот, затемненное сознание, резко выраженные микроциркуляторные нарушения на конеч ностях (застойные пятна, цианоз), анурия. Диагноз. Для подтверждения менингококкового менингита решающее значение имеет спинномозговая пункция. Из лабораторных методов используются бактериоскопия мазков крови (толстая капля) на обнаружение менингококка, бактериологическое исследование ликвора. Из серологических методов наибольшей чувствительностью обладает РПГА. Лечение необходимо начинать сразу после установления диагноза. На догоспитальном этапе при подозрении на менингококцемию (в т. ч. и смешанную форму) проводится борьба с гипертермией в зависимости от варианта лихорадки. При «розовой» лихорадке внутрь или ректально вводят парацетамол в разовой дозе 10–15 мг/кг, при неэффективности — ибупрофен (Нурофен) в разовой дозе 5–10 мг/кг массы тела. Одновременно проводятся физические методы охлаждения, но не более 30 минут. При неэффективности вводят литическую смесь в составе: 50% раствор анальгина + антигистаминный препарат (пипольфен) внутримышечно в возрастной дозе. При «бледной» лихорадке больного согревают, вводят в/м спазмолитики (папаверин, но-шпа) и литическую смесь. При выраженной централизации кровообращения в терапию добавляют 0,25%-ный раствор дроперидола 0,1–0,2 мл/кг в сочетании с антипиретиками. При судорожном синдроме наряду с 853 указанной терапией вводят в/м реланиум из расчета 0,1 мл/кг. При отсутствии эффекта включают в терапию дроперидол в сочетании с анальгином, оксибутират натрия. Для предупреждения токсического шока вводят преднизолон в/м или внутривенно (в/в) в дозе 2 мг/кг. При выраженном менингеальном синдроме — 25%-ную сернокислую магнезию 1 мл/год жизни или лазикс – 1-2 мг/кг в/м. Введение антибиотика в течение первого часа транспортировки не рекомендуется, а в случае длительной транспортировки стартовым препаратом является левомицетина сукцинат в разовой дозе 25 мг/кг, который вводится не более 2 сут. Состояние больного оценивается под постоянным контролем АД, частоты пульса, дыхания, диуреза, окраски и температуры кожных покровов, нарастания количества и качества элементов экзантемы и сознания больного. При подозрении на молниеносный вариант генерализованной формы МИ госпитализация осуществляется реанимационной бригадой, которая проводит немедленные реанимационные мероприятия на дому и при транспортировке больного и продолжается в отделении реанимации и интенсивной терапии (ОРИТ). Противошоковый эффект достигается введением высоких доз гидрокортизона в сочетании с преднизолоном или его аналогами. Проводится инфузионная терапия, состав которой определяется показателями коллоидно-осмотического давления (альбумина 45–52 г/л и натрия 140–145 ммоль/л). Базовыми растворами являются 5%-ная глюкоза, физиологический раствор или раствор Рингера. Соотношение вводимых коллоидов/кристаллоидов - 1:3. Вводится физиологический раствор с целью купирования гиповолемии, при резком падении АД струйно, а при умеренном его снижении — в/в капельно. Под контролем кислотно-основного состояния (КОС) вводится 4%-ный бикарбонат натрия в/в медленно, капельно по показателю дефицита оснований (ВЕ) в количестве, равном массе тела (в кг) умноженной на ВЕ и поделенной на 2. Назначаются ангиопротекторы инстенон, кавинтон, актовегин, сулодексид с учетом развития генерализованного васкулита с поражением эндотелия сосудов. Постоянно должна проводиться оксигенация вплоть до искусственной вентиляции легких (ИВЛ), начиная с момента оказания помощи на дому. Пенициллин назначается в дозе 300 тыс. ед./кг массы тела на 6 введений после отмены левомицетина сукцината, а у детей до 3 мес — 500 тыс./кг на 8 введений. Более комплаентным и альтернативным пенициллину является цефтриаксон (Роцефин), который вводится однократно в течение суток в/в или в/м в дозе 100–150 мг/кг массы в течение 5 дней при менингококцемии, а при менингите до 10 дней. При синдроме диссеминированного внутрисосудистого свертывания (ДВС-синдроме) назначаются при гиперкоагуляции трентал, реополиглюкин, стабизол, рефортан а при гипокоагуляции - свежезаготовленная плазма, ингибиторы протеолиза. При отеке/набухании головного мозга проводится постоянно дегидратационная терапия (лазикс, маннитол 15%-ный) только после стабилизации центральной гемодинамики. При синдроме Уотерхауса - Фридериксена необходима госпитализация в реанимационное отделение на фоне проведения неотложных лечебных мероприятий: в/в струйно - гидрокортизон 20-30 мг/кг, или преднизолон 15-20 мг/кг (суточная доза). Первая доза препарата составляет 50% от суточной, оставшаяся доза распределяется равномерно через каждые 2 часа в течение первых 6 часов. С целью регидратации в/в струйно необходимо ввести плазмозамещающие растворы в дозе 10-15 мл/кг; затем наладить введение в/в капельно 5-10% раствора глюкозы и 0,9% раствора натрия хлорида в соотношении 1:1 или 1:2 (при резко выраженной дегидратации) из расчета 80-100 мл/кг/сут. При сохраняющейся гипотензии необходимо введение допамина 8-10 мкг/кг/мин. Антибиотикотерапия проводится левомицетином сукцинатом натрия (25 мг/кг в разовой дозе, 80-100 мг/кг/сут.). Критерии выздоровления: Выздоровление при всех формах менингококковой инфекции констатируют после полного исчезновения всех симптомов заболевания и двухкратного отрицательного результата посева слизи носоглотки на менингококк, проведенного после окончания курса антибактериальной терапии. Только после этого ребенок считается не заразным для окружающих. 863 Диспансеризация. Реконвалесценты генерализованных форм инфекции наблюдаются педиатром, врачом общей практики, невропатологом (не менее 3 лет): в течение первого года – 1 раз в 3 мес., второго – 1 раз в 6 мес., и 1 раз в конце третьего года. Занятия физкультурой в школе не ранее, чем через 6 мес. Освобождение от прививок на 1 год. Профилактика. В очаге менингококковой инфекции на контактных накладывается карантин на 10 дней с момента разобщения с больным. Детям первого года жизни показано введение донорского иммуноглобулина. Вакцинация проводится по эпидпоказаниям. 873 Вопросы для тестового контроля: № п/п 1 2 3 4 5 6 7 8 9 10 Содержание вопросов Наиболее частой причиной развития синдрома крупа у детей является: а) грипп; б) парагрипп; в) аденовирусная инфекция; г) респираторный микоплазмоз. Какой ОРВИ не свойственны кишечные расстройства, увеличение лимфоузлов, печени и селезенки: а) аденовирусной инфекции; б) респираторносинцитиальной инфекции; в) гриппу. .Типичная локализация сыпи при менингококкемии: а) разгибательные поверхности суставов; б) лицо, верхний плечевой пояс; в) сгущение в местах естественных складок; г) ягодицы, бедра, живот; д) живот, боковые поверхности туловища. Для детей раннего возраста при менингококковой инфекции характерно наличие следующих неврологических симптомов: а) Брудзинского; б) Бабинского; в) Бабкина; г) Лессажа; д) Кернига. Для клиники гриппа у детей характерно: а) острое начало; б) субфебрильная температура; в) интенсивная головная боль; г) рвота; д) выраженные катаральные явления. Механизм передачи менингококковой инфекции: а) водный; б) трансмиссивный; в) контактно-бытовой; г) фекально-оральный; д) воздушно-капельный. Наиболее характерное место размножения вируса при РС - инфекции: а) слизистая носа; б) слизистая гортани; в) эпителий бронхов; г) мозговые оболочки; д) эпителий бронхиол. Инкубационный период при гриппе А составляет: а) несколько часов; б) 2-3 дня; в) 5-7 дней; г) несколько недель; д) 3 месяца. Для клиники парагриппа характерны следующие клинические симптомы: а) долгое отсутствие катаральных явлений; б) выраженные симптомы интоксикации; в) частое развитие ложного крупа; г) грубый сухой кашель; д) слизистогнойное отделяемое из носовых ходов. Для менингококкового менингита характерны следующие изменения в ликворе: а) лимфоцитарный плеоцитоз; б) нейтрофильный плеоцитоз; в) повышение глюкозы; г) повышение белка; д) снижение белка. Эталоны ответов б в г г а, в, г д в, д а, б в, г, д б, г Ситуационные задачи № п/п 1. Содержание задач Эталоны ответов Алеша К., 5 лет заболел остро. Резко поднялась температура до 39С. Отмечался озноб, общее недомогание, боли в мышцах. Затем появилась головная боль, преимущественно в области лба, надбровных дуг, боль в глазных яблоках, животе и пояснице. Ребенок был очень вялым (лежал «пластом»). После дачи парацетамола температура тела несколько снизилась, но через 2 часа вновь повысилась до фебрильных цифр. Была вызвана бригада «Скорой помощи». При осмотре ребенок вялый, лицо гиперемировано, склеры инъецированы. Носовое дыхание не затруднено. В зеве гиперемия. В легких дыхание везикулярное, хрипов нет. Тоны сердца ясные. Живот мягкий, безболезненный. Печень и селезенка не увеличены. Вопросы: 1.Предварительный диагноз. 1.В данном случае имеет место ОРВИ, грипп, средней степени тяжести, фарингит. 2.Необходимо дифференцировать с другими ОРВИ (парагрипп, аденовирусная инфекция), пневмонией, менингококковой инфекцией, дизентерией, корью, дифтерией. 3.Лечение: постельный режим, обильное питье, жаропонижающие при температуре тела выше 39С, лейкоцитарный интерферон, противовирусный препарат рибамидил 10 мг/кг/сут в 3-4 приема 3-5 дней. 4.Путь передачи воздушно-капельный. 883 2. 2.Дифференциальный диагноз. 3.Лечение. 4.Указать пути передачи данной инфекции. Игорь А., 1 год 6 мес., заболел остро, внезапно. Поднялась температура тела до 39,9°С в 20 час., плачет, беспокоится, отмечалась однократная рвота. Через час на коже бедер появилась единичная геморрагическая сыпь. При осмотре отмечается гиперестезия, ребенок кричит. Носовое дыхание не затруднено. В зеве гиперемия задней стенки глотки, зернистость. В легких дыхание везикулярное, хрипов нет. Тоны сердца приглушены. В общем анализе крови Hb – 130 г/л, лейкоциты – 15,6х10 9/л; СОЭ – 30 мм/ч. Вопросы: 1.Ваш предварительный диагноз. 2.Наметить план обследования ребенка. 3.Неотложные мероприятия. 4.Указать основные лабораторные методы диагностики. 1. Менингококковая инфекция, генерализованная форма, менингококкемия. 2. План обследования: - общеклиническое исследование, включающее общий анализ крови, мочи в динамике; спинномозговая пункция; консультация невропатолога; 3. Антибактериальная терапия - левомицетина сукцинат в/м из расчета 25 мг/кг (разовая доза). Необходимо ввести в/м преднизолон из расчета 2мг/кг (разовая доза) для мембраностабилизирующего действия. Жаропонижающие средства (анальгин 0,15 в/м). Дезинтоксикационная терапия – в/в капельно реополиглюкин 10 мл/кг, затем глюкоза, альбумин с учетом диуреза. Мочегонные – лазикс 2 мг/кг в сутки. 4. Из лабораторных методов используются бактериоскопия мазков крови (толстая капля) на обнаружение менингококка, бактериологическое исследование ликвора. Из серологических методов наибольшей чувствительностью обладает РПГА. Рекомендуемая литература: Основная: 1. Нисевич Н.И., Учайкин В.Ф. Инфекционные болезни у детей. - М.: "Медицина", 2008, 790с. Дополнительная: 1. Детские инфекционные болезни. – В.Н.Самарина, О.А.Сорокина. – С.-Петербург: Невский диалект, 2000. - 317 С. 2. Инфекционные болезни у детей./ Под редакцией члена-корреспондента РАМН, профессора В.В.Ивановой. – Москва: Медицинское информационное агентство, 2002. – 923 С. 3. Инфекционные болезни у детей // Под редакцией профессора Э.Н. Симованьян - Ростов на Дону: Феникс, 2007 - 766 с. – (Высшее образование). Занятие № 12. ВОЗДУШНО-КАПЕЛЬНЫЕ ИНФЕКЦИИ Цель занятия: изучить особенности эпидемиологии, клиники и дифференциальной диагностики кори, краснухи, ветряной оспы, эпидемического паротита и коклюша; вопросы профилактики данных заболеваний. Вопросы для самоподготовки: 1. Особенности этиологии, эпидемиологии, клинического течения и профилактики ветряной оспы у детей. 2. Корь. Этиология, эпидемиология, клиническое течение, профилактика. 3. Краснуха. Особенности эпидемиологии и клинического течения. Дифференциальный диагноз с корью. 4. Этиология, эпидемиология, клинические проявления и профилактика эпидемического паротита у детей. 5. Коклюш. Особенности эпидемиологии, клиники и профилактики. 893 Ветряная оспа острое инфекционное заболевание, характеризующееся сыпью на коже и слизистых оболочках в виде однокамерных пузырьков с серозным содержимым. Этиология. Возбудитель ветряной оспы (ВО) относится к герпесвирусам, содержит ДНК и по своим свойствам аналогичен вирусу опоясывающего герпеса. Эпидемиология. Источником инфекции является только человек, больной ВО или опоясывающим герпесом. Ветряной оспой заболевают в основном дети в возрасте до 6-8 лет. Восприимчивость к ВО очень высокая. Передача инфекции происходит преимущественно воздушно-капельным путем. ВО легко распространяется на большие расстояния, в связи с чем ВО относится к «летучим» инфекциям. Клиника. Инкубационный период при ВО составляет от 10 до 23 дней (в среднем 14 дней). Заболевание начинается с повышения температуры. Одновременно или к концу первых суток появляется характерная сыпь. Иногда бывают продромальные симптомы (субфебрильная температура, общее недомогание). «Ветряночная» сыпь проходит через несколько фаз развития: пятно, папула, пузырек (везикула), корочка, пигментное пятно. Сыпь появляется на различных участках кожи, включая волосистую часть головы, и слизистых оболочках (в ротовой полости, дыхательных путях, половых органах). Подсыпание ветряночных элементов происходит толчкообразно в течение 2-5 дней и сопровождается подъемами температуры. В связи с повторностью высыпаний и появлением элементов на различных участках тела возникает локальный («ложный») полиморфизм. Главной особенностью ветряночной сыпи, позволяющей быстро ставить диагноз, является разновременность отдельных волн высыпаний. На определенном участке кожи могут образоваться элементы, относящиеся к различным фазам развития (пятна, пузырьки, корочки). Корочки отпадают после эпителизации, не ранее 1-2-х недель от начала заболевания. Критериями тяжести ВО являются: количество высыпных элементов, их величина, длительность и выраженность температурной реакции, характер и тяжесть осложнений. Классификация: Выделяют следующие формы ВО: а) типичные (легкая, среднетяжелая, тяжелая); б) атипичные (абортивная, рудиментарная). Наиболее тяжелыми формами являются геморрагическая, гангренозная и генерализованная. ВО может иметь осложненное течение. К специфическим осложнениям относятся энцефалит, менингоэнцефалит, миелит, миокардит, гепатит и др. Диагноз. К опорным диагностическим признакам относятся: 1) осенне-зимняя сезонность; 2) контакт с больным ВО или опоясывающим герпесом; 3) характерная ветряночная сыпь с наличием полиморфизма. Используют серологические методы (РСК, РН, ИФА). Лечение. Госпитализации подлежат больные с тяжелыми и осложненными формами ВО, легкие и среднетяжелые формы заболевания лечатся на дому. На время острого периода (6-7 дней) рекомендуется постельный режим, молочно-растительная диета, обильное питье. Для профилактики бактериальной инфекции проводят местную обработку спиртовым раствором анилиновых красок: 1 % раствором бриллиантового зеленого, 1-2 % раствором перманганата калия. Проводится симптоматическая терапия. Больным с тяжелыми формами ВО назначают противовирусные препараты: ацикловир (зовиракс, виролекс), алпизарин, хелепин и др. Показано применение специфического или нормального иммуноглобулина (0,2 мл/кг), интерферона, дезинтоксикационной терапии. При бактериальных осложнениях рекомендуются антибиотики. Кортикостероидные препараты при ВО назначать не следует. Профилактика. Изоляция больного ВО должна составлять не менее 9 дней. Больной становится не заразен для окружающих уже через 5 дней после появления последнего пузырькового элемента. На контактных детей в возрасте до 7 лет, не болевших ВО, накладывается карантин с 11-го по 21-й день от момента разобщения с больным ВО. Апробируется вакцина против ветряной оспы. 903 Корь острое инфекционное заболевание, характеризующееся интоксикацией, поражением нервной системы, верхних дыхательных путей (кашель, насморк и др.), высыпанием пятнисто-папулезной сыпи, повышением температуры, воспалением слизистых оболочек глаз, полости рта, угнетением иммунитета. Этиология. Возбудитель кори относится к группе миксовирусов, нестоек во внешней среде, но потоками воздуха с капельками слизи может переноситься на расстояния. Эпидемиология. Источник инфекции больной человек. Передача инфекции происходит воздушно-капельным путем. Восприимчивость к кори очень высокая. Контагиозный индекс составляет 95-96 %. После перенесенной кори создается стойкий пожизненный иммунитет. Клиника. Инкубационный период при кори в среднем составляет 8-10 дней (до 17 дней). У детей, получавших с профилактической целью иммуноглобулин, инкубационный период удлиняется до 21 дня. Клиническая картина типичной кори включает последовательное развитие трех основных периодов: катарального, высыпаний и пигментации (реконвалесценции). Катаральный период обычно продолжается 3-4 дня, характеризуется катаральным воспалением верхних дыхательный путей и общей интоксикацией. Температура тела поднимается до фебрильных цифр (38-39 0С) и сохраняется в течение всего катарального периода. Отмечается вялость ребенка, сонливость, снижение аппетита (вплоть до анорексии), может быть рвота. Появляются конъюнктивит, отечность век, слезотечение, светобоязнь, блефароспазм, на слизистой оболочке щек, мягкого и твердого неба коревая энантема. Патогномоничным симптомом при кори являются пятна Бельского-ФилатоваКоплика. Они обнаруживаются на слизистой оболочке рта и переходной складке у малых коренных зубов за 1-2 дня до высыпания на коже. Это мелкие пятнышки серовато-белого цвета, окруженные красным венчиком и напоминающие рассыпанную манную крупу (встречаются у 65-70 % больных). Выявление этого симптома позволяет поставить диагноз кори уже в катаральном периоде. Период высыпания начинается на 4-5-й день болезни и продолжается 3-4 дня. Коревая сыпь имеет пятнисто-папулезный характер, располагается на неизмененном фоне кожи, склонна к слиянию. Высыпание происходит этапно, в течение 3-4-х дней. В первый день сыпь покрывает лицо, включая область вокруг рта, шею, верхнюю часть туловища. На вторые сутки она распространяется на все туловище и частично на руки, на третий день на остальные части рук и ноги. Период пигментации продолжается 1-1,5 недели. Сыпь бледнеет и пигментируется в той же последовательности, в какой отмечались высыпания. Ее исчезновение сопровождается отрубевидным шелушением. Выделяют типичную и атипичную корь. По тяжести течения корь подразделяют на легкую, среднетяжелую, тяжелую. Критериями тяжести являются выраженность интоксикации и развитие осложнений. Атипично протекает митигированная корь (в случаях введения контактным детям иммуноглобулина). При этом не наблюдается выраженной интоксикации, температура часто остается нормальной, катаральные явления выражены слабо, пятна Бельского-Филатова нередко отсутствуют, сыпь необильная, бледная, мелкая, этапности высыпаний и осложнений не отмечается. У подростков и взрослых корь, как правило, протекает более тяжело по сравнению с детьми дошкольного и школьного возраста. Наиболее частыми осложнениями при типичной кори являются ларингиты, ларинготрахеиты, пневмонии, отиты, ангины, стоматиты, колиты, энтероколиты. В последние годы участились осложнения со стороны нервной системы (коревые энцефалиты, энцефаломиелиты). Диагноз типичной кори не представляет особых затруднений. К опорным диагностическим признакам относятся: 1) контакт с больным корью; 2) наличие продромального периода; 3) наличие выраженных катаральных явлений; 4) пастозность лица; 5) пятна Бельского-Филатова-Коплика; 6) 3-4-дневный период высыпания с характерной этапностью. 913 Используются серологические методы диагностики (РТГА). Нарастание титра антител в 4 раза и более в парных сыворотках бесспорно подтверждает диагноз. Лечение больных корью проводится в основном в домашних условиях. Госпитализации подлежат дети с тяжелым и осложненным течением заболевания, а также дети из закрытых детских учреждений, общежитий. Основное внимание уделяется созданию хороших санитарно-гигиенических условий. В диете: исключение трудноусвояемой пищи, особенно при лихорадочном состоянии. Ребенок должен получать достаточное количество жидкости. Показано назначение витаминов в виде свежих соков и готовых препаратов. Жаропонижающие средства используются по показаниям, нужно избегать их планового назначения, антибиотики применять не рекомендуется. При подозрении на осложнение больного целесообразно госпитализировать. Профилактика. Заболевшие корью изолируются на срок не менее 4-х дней от начала высыпания, при осложнении пневмонией не менее 10 дней. Для детей, не болевших корью, длительность разобщения устанавливается с момента контакта с больным корью в течение 17 дней, а для получивших иммуноглобулин 21 день. Для детей, переболевших корью, привитых живой коревой вакциной, и для взрослых разобщение не применяется. Иммунопрофилактика проводится только тем контактировавшим с больным корью детям, у которых имеются противопоказания к прививкам, или детям, не достигшим прививочного возраста. Доза иммуноглобулина 3 мл (вводится в/м). Обязательные прививки против кори живой коревой вакциной проводятся не болевшим корью с 12-месячного возраста совместно с вакцинацией против краснухи и эпид.паротита. Краснуха острое инфекционное заболевание, характеризующееся катаральными явлениями со стороны верхних дыхательных путей, мелкопятнистой экзантемой, увеличением затылочных и заднешейных лимфатических узлов. Этиология. Возбудителем краснухи является РНК-содержащий вирус. Эпидемиология. Источник инфекции больной человек, путь передачи воздушно-капельный. Восприимчивость детей к краснухе высокая. Наиболее часто болеют дети в возрасте от 1 года до 7-8 лет. После перенесенного заболевания вырабатывается стойкий иммунитет. Клиника. Инкубационный период при краснухе 15-24 дня. Продромальный период у детей может отсутствовать или составлять 1-2 дня. Появившиеся легкие катаральные явления со стороны верхних дыхательных путей не имеют тенденции к усилению. Температура чаще субфебрильная. С первых дней заболевания отмечается генерализованная лимфаденопатия с обязательным вовлечением в процесс затылочных и заднешейных лимфатических узлов. К числу постоянных признаков краснухи относится сыпь. У большинства больных она является первым симптомом заболевания. Сыпь появляется на лице, за ушами и быстро, в течение нескольких часов, распространяется по всему телу. Сыпь при краснухе мелкопятнистая, бледно-розового цвета без тенденции к слиянию, на неизменном фоне кожи. Сыпь появляется на спине, ягодицах, разгибательной поверхности конечностей вокруг суставов. Сыпь сохраняется 2-3 дня и исчезает без пигментации. В периферической крови отмечается лейкопения, относительный лимфоцитоз и появление плазматических клеток. Осложнения при краснухе развиваются редко (энцефалиты и менингоэнцефалиты). Диагностика краснухи основывается на клинических симптомах и серологических данных четырехкратное нарастание титра антител в реакции РПГА. К опорным диагностическим признакам относятся: 1) подъем заболеваемости в районе; 2) характерная мелкопятнистая сыпь; 3) слабая выраженность катаральных явлений и интоксикации; 4) увеличение и болезненность затылочных лимфатических узлов; 5) характерные изменения крови (лейкопения, лимфомоноцитоз, плазматические клетки. Краснуху следует дифференцировать от кори, аллергической сыпи, энтеровирусной экзантемы, инфекционного мононуклеоза, скарлатины (см. таблицу 19). Лечение больных краснухой проводится, как правило, в домашних условиях. Используется симптоматическая терапия. Больные изолируются на 5 дней с момента появления сыпи. 923 Активная профилактика краснухи проводится вакциной «Рудивакс». Детей, бывших в контакте с больным краснухой, не разобщают. Эпидемический паротит общее инфекционное заболевание, характеризующееся поражением железистых органов (чаще слюнных желез, реже поджелудочной железы, яичек, яичников), а также ЦНС (менингит, менингоэнцефалит). Этиология. Возбудитель вирус, из семейства парамиксовирусов, неустойчивый во внешней среде. Эпидемиология. Источник инфекции больной человек. Заражение происходит воздушно-капельным путем. Восприимчивость к паротитной инфекции высокая. Индекс контагиозности 30-50 % и выше. Болеют дети старше года и взрослые. Иммунитет стойкий, пожизненный. Клиника. Инкубационный период продолжается от 11 до 21 дня. Болезнь, как правило, начинается остро, с повышения температуры тела до 38-39 0С и более, появления припухлости и болезненности околоушных слюнных желез, усиливающейся при жевании и открывании рта. Процесс обычно носит двусторонний характер, однако, возможно одностороннее поражение или вовлечение в процесс только подчелюстных желез (субмаксиллит). Могут поражаться подъязычная слюнная железа, поджелудочная, половые железы (яички, яичники) и др. Поражение поджелудочной железы проявляется болями в эпигастральной, околопупочной областях, рвотой, тошнотой, снижением аппетита. Уровень диастазы в моче повышается до высоких цифр. Поражение половых желез отмечается чаще у взрослых и подростков в период полового созревания. Обычно орхит бывает односторонним. Яичко увеличивается в размерах, отмечается отечность и гиперемия мошонки. При вовлечении в процесс оболочек головного мозга появляются головная боль, повторная рвота, головокружение, иногда судороги, повышение температуры тела. Менингеальные симптомы выражены умеренно. Давление спинномозговой жидкости повышено, ликвор прозрачный или опалесцирующий, плеоцитоз умеренный (от 300-700 до 2000 клеток в 1 мкл), лимфоцитарного характера (количество лимфоцитов 96-98 %). В периферической крови выявляются лейкопения, лимфоцитоз, отмечается нормальная или умеренно повышенная СОЭ. Различают типичные и атипичные формы, по тяжести легкие, среднетяжелые, тяжелые. Диагноз. К опорным диагностическим признакам эпидемического паротита относятся: 1) острое начало заболевания с подъемом температуры; 2) остро развившееся припухлость и болезненность околоушных узлов; 3) боли в животе, повышение диастазы мочи; 4) возникновение на фоне паротита или вслед за ним орхита, серозного менингита, панкреатита. Лабораторная диагностика паротита проводится редко. Используются РСК, РЗГА в парных сыворотках. Лечение. Госпитализируются больные с тяжелыми и комбинированными формами заболевания. Этиотропного лечения нет. Терапия симптоматическая, определяется характером и степенью проявлений болезни: постельный режим, обильное питье, уход за ротовой полостью, механически щадящая диета, сухое тепло на пораженные слюнные железы, жаропонижающие, десенсибилизирующие препараты, поливитамины. Лечение панкреатита, орхита, менингита проводится в соответствии с характером поражения. Профилактика. Изоляция больного на 9 дней от начала заболевания. В детских учреждениях устанавливается карантин на 21 день. Дети в возрасте до 10 лет, имевшие контакт с больным, в детское учреждение не допускаются с 11-го по 21-й день с момента контакта. Специфическая профилактика паротитной инфекции проводится живой вакциной детям в возрасте 12-18 месяцев, совместно с вакцинацией против кори и краснухи. 933 Таблица 22 Дифференциальный диагноз заболеваний с синдромом экзантемы (Брюханова Л.К. и соавт., 1998) Заболевание Корь Время появления сыпи На 3-4-й день заболевания, в течение 3-4-х дней распространяется с лица на конечности Характер сыпи Пятнистопапулезная на неизмененном фоне кожи Локализация сыпи Зависит от дня высыпания, 1-й день лицо, 2й день туловище, 3-й день все тело Краснуха На 1-2-й день, одномоментно По всему телу, преимущественно на разгибательных поверхностях конечностей Скарлатина В первые сутки, высыпание одномоментное Мелкопятнистая, пятнистопапулезная, на неизмененном фоне кожи Мелкоточечная, на гиперемированном фоне кожи, бывают петехии Псевдотуберкулез Чаще на 3-4 день заболевания, одномоментно Энтеровирусная экзантема На 2-5 день болезни Мелкоточечная на гиперемированном фоне. Симптомы «капюшона», «перчаток», «носков» Полиморфная, пятнистая Исход сыпи Угасает поэтапно (сверху вниз), пигментация сыпи, шелушение Пигментации нет Другие симптомы Лихорадка, катаральные явления со стороны ВДП, конъюнктивит, блефарит, светобоязнь, пятна Бельского-Филатова Общее состояние мало нарушено, увеличение заднешейных лимфатических узлов По всему телу, преимущественно внизу живота и кожных складок, носогубный треугольник бледный По всему телу, сгущается в кожных складках, носогубный треугольник бледный Пигментации нет, на 2-й недели заболевания шелушение на пальцах (крупнопластинчатое) Без пигментации, шелушение как при скарлатине Лихорадка, интоксикация, ангина, шейный лимфаденит (тонзиллярные узлы) Чаще на туловище, руках Исчезает через 1-2 дня Катаральные явления со стороны ВДП, диарея. Возможны миалгия, серозный менингит, герп.ангина Длительная лихорадка, мышечные и суставные боли, увеличение печени и селезенки Коклюш острое инфекционное заболевание, ведущим симптомом которого является приступообразный спазматический кашель. Этиология. Возбудитель коклюшная палочка Борде - Жангу, неустойчивая во внешней среде. Эпидемиология. Источник инфекции больной человек, особенно больные стертыми формами. Путь передачи воздушно-капельный. Восприимчивость к коклюшу высокая с самого рождения ребенка. Индекс восприимчивости 70 %. Иммунитет стойкий, пожизненный. Клиника. Инкубационный период от 2-х до 14 дней (чаще 5-8 дней). В течение болезни выделяют три периода: начальный или катаральный (2-14 дней), спазматический (2-4 недели), период разрешения (1-2 месяца). Катаральный период: начало постепенное, появляются сухой кашель, иногда субфебрильная температура, насморк. Общее состояние обычно не страдает. Постепенно кашель усиливается, становится навязчивым, приобретает приступообразный характер. Спазматиче943 ский период начинается с появления приступов спазматического кашля, характерным симптомом является глубокий свистящий вдох (реприз), прерывающий кашлевые толчки, что обусловлено спастически суженной голосовой щелью. Репризы возникают повторно (от 2-х до 15). Приступ кашля заканчивается выделением вязкой стекловидной мокроты, иногда рвотой. Во время приступа лицо краснеет, синеет, вены шеи набухают, глаза слезятся, голова вытягивается вперед, язык высовывается до предела изо рта. В тяжелых случаях во время кашля бывают носовые кровотечения, кровоизлияния в склеру, апноэ, непроизвольное мочеиспускание и дефекация. В зависимости от тяжести заболевания число приступов варьирует от 5 до 50 в сутки. Постепенно приступы кашля становятся реже, кашель приобретает «обычный» характер (период разрешения). При объективном осмотре определяются одутловатость лица, бледность кожи, иногда кровоизлияния на коже и конъюнктиве глаз, язвочка на уздечке языка; коробочный перкуторный звук над легкими, иногда сухие проводные хрипы; характерны изменения периферической крови при коклюше: выраженный лейкоцитоз и лимфоцитоз при нормальной СОЭ. Выделяют типичные и атипичные (стертые и бессимптомные) формы коклюша. По тяжести они могут быть легкими, среднетяжелыми, тяжелыми. Критериями тяжести является количество приступов кашля, их продолжительность, число репризов, нарушение общего состояния. Осложнения: специфические апноэ, поражения ЦНС, проявляющиеся энцефалопатией, судорогами, менингизмом, эмфизема; сегментарные и долевые ателектазы в легких, носовые кровотечения, кровоизлияния на коже, в конъюнктиву глаз; неспецифические обусловленные наслоением вторичной инфекции (бронхит, пневмония, отит и др.). Диагноз. К опорным диагностическим признакам коклюша относятся: 1) контакт с больным коклюшем; 2) сухой навязчивый, упорно нарастающий кашель при нормальной температуре и отсутствии катаральных явлений; 3) периодически возникающая рвота после кашля; 4) характерные репризы; 5) лейкоцитоз, лимфоцитоз; 6) приступы апноэ у детей первых месяцев жизни. Для лабораторной диагностики решающее значение имеет выделение возбудителя. Материал для исследования берут с задней стенки глотки с помощью сухого тампона. Серологические методы (реакция агглютинации, РСК, РПГА) служат для ретроспективной диагностики. Лечение. Госпитализируются дети раннего возраста, больные тяжелой формой коклюша и при наличии осложнений. Антибиотики эффективны в самом начале болезни (в катаральном периоде) и в течение 2-4-х недель спазматического кашля. Кроме того, они показаны у детей раннего возраста, при тяжелых и осложненных формах коклюша. Назначаются эритромицин, ампициллин, гентамицин в возрастных дозировках. Курс лечения 7-10 дней. Лечение пенициллином, оксациллином и другими антибиотиками при коклюше неэффективно. Симптоматическая терапия включает препараты, подавляющие кашель (тусупрекс, либексин, микстуры с белладонной и др.), антигистаминные препараты (димедрол, супрастин и др.), муколитические препараты, бронхолитики (эуфиллин, эфедрин), ингаляции с протеолитическими ферментами. Горчичники и тепловые процедуры на грудную клетку не показаны, так как могут провоцировать приступы кашля. Полезен прием успокаивающих отваров трав валерианы, пустырника. Показано проведение дыхательной гимнастики и массажа. В тяжелых случаях кортикостероиды (1,5-2 мг/кг преднизолона), нейролептики (аминазин), транквилизаторы (седуксен). Профилактика. Больные коклюшем изолируются на 25-30 дней от начала заболевания. Для контактных детей в возрасте до 7 лет устанавливается карантин на 14 дней от момента последнего контакта с больным, однократно берется посев на коклюшную палочку. Детям до 1 года, не болевшим и не привитым, вводится иммуноглобулин в дозе 6,0 мл (по 3,0 мл через день). Активная иммунизация против коклюша проводится вакциной АКДС с 3 месяцев. 953 Вопросы для тестового контроля: № п/п 1 Эталоны ответов Сыпь при ветряной оспе проходит несколько фаз развития (расставьте в правиль- г, а, д, б, ном порядке): а) папула; б) корочка; в) пигментное пятно; г) пятно; д) везикула. в 2 Какие из общих свойств присущи детским капельным инфекциям: а) всеобщая а, б, в восприимчивость; б) высокая контагиозность; в) стойкий иммунитет, возникающий после заболевания. Специфическая профилактика проводится при: а) кори; б) эпид. паротите; в) а, б, в коклюше; г) ветряной оспе. 3 4 5 6 7 8 9 10 Содержание вопросов Для какой из инфекций характерен катаральный период: а) краснухи; б) эпид. па- в ротита; в) кори; г) ветряной оспы. При эпидемическом паротите поражаются: а) миндалины; б) железистые органы; б в) лимфатические узлы. Для краснухи характерны: а) пятнисто-папулезная сыпь; б) повышение темпера- а, б, в туры тела; в) увеличение лимфатических узлов; г) ангина; д) везикулезная сыпь. Для лечения краснухи применяются : а) антибиотики; б) преднизолон; в в) комплексы витаминов; г) препараты железа. Вирус кори во внешней среде: а) устойчив; б) неустойчив; в) может распростра- б, в няться на расстояния. Кашель с репризами характерен для: а) кори; б) коклюша; в) эпидемического па- б ротита; г) инфекционного мононуклеоза; д) краснухи. Инкубационный период при коклюше составляет: а) 5-8 дней; б) 15-18 дней; в) а 2-3 дня; г) 20-30 дней; д) 4-6 дней. Ситуационные задачи: № п/п 1. 2. Содержание задач Эталоны ответов Виталий В., 4 лет заболел вечером 18 апреля, когда появилось снижение аппетита и субфебрильная температура, к концу первых суток появилась сыпь. Температура тела повысилась до 40 градусов. Сыпь появлялась на различных участках кожи, включая волосистую часть головы, и слизистые оболочки (в ротовой полости) в виде везикул. Подсыпание элементов происходило толчкообразно в течение 2-5 дней и сопровождалось подъемами температуры. Отмечался полиморфизм сыпи. В зеве легкая гиперемия. В легких дыхание везикулярное, хрипов нет. Тоны сердца ясные, ритм правильный, ЧСС – 128 в минуту. Живот при пальпации мягкий, безболезненный. Стул и диурез не нарушены. Вопросы: 1.Предварительный диагноз. 2.Указать инкубационный период данной инфекции. 3.Пути передачи. 4.Лечение. 1.Ветряная оспа. Типичная форма. Средней степени тяжести. 2.Инкубационный период при ветряной оспе составляет 10-23 дня, в среднем 14 дней. 3.Ветряная оспа передается воздушно-капельным путем, очень легко переносится на большие расстояния. 4.Лечение: На время острого периода (6-7 дней) рекомендовать постельный режим, молочнорастительная диета, обильное питье. Местная обработка элементов сыпи спиртовым раствором анилиновых красителей – 1% раствор бриллиантового зеленого. Рекомендовано назначение противовирусных препаратов - ацикловир. Использовать интерферон и иммуноглобулин. 1.В данном случае имеет место катаральный период кори. 2.Инкубационный период при кори в среднем составляет 8-11 дней. 3.Воздушно-капельный путь передачи инфекции. Контагиозный индекс составляет 95-96 %. 4.Лечение больных корью проводится в домашних условиях. Необхо- Наталья Р., 4 лет заболела остро, температура тела поднялась до 39 0С. Отмечалась вялость ребенка, сонливость, снижение аппетита. Со слов матери у ребенка отмечалась отечность век, слезотечение, светобоязнь. При осмотре на слизистой оболочке рта и переходной складке у малых коренных зубов обнаружены мелкие пятнышки серовато-белого цвета, окруженные красным венчиком и напоминающие рассыпанную манную крупу. Кожные покровы 963 бледно розового цвета, чистые. В легких дыхание везикулярное, хрипов нет, ЧД – 34 в минуту. Тоны сердца ясные, ЧСС – 140 в минуту. Вопросы: 1.Предположительный диагноз. 2.Указать инкубационный период при данной инфекции. 3.Назвать пути передачи инфекции и контагиозный индекс .4.Лечение. димо создать хорошие санитарногигиенические условия. В диете: исключение трудноусвояемой пищи, ребенок должен получать достаточное количество жидкости. Показано назначение витаминов в виде свежих соков и готовых препаратов. Жаропонижающие средства в виде препаратов парацетамола. Рекомендуемая литература: Основная: 1. Нисевич Н.И., Учайкин В.Ф. Инфекционные болезни у детей. - М.: "Медицина", 2008, 790 с. Дополнительная: 1. Детские инфекционные болезни. – В.Н.Самарина, О.А.Сорокина. – С.-Петербург: Невский диалект, 2000. - 317 с. 2. Инфекционные болезни у детей./ Под редакцией члена-корреспондента РАМН, профессора В.В. Ивановой. – Москва: Медицинское информационное агентство, 2002. – 923 С. 3. Инфекционные болезни у детей / под редакцией профессора Э.Н. Симованьян - Ростов на Дону: Феникс, 2007, - 766 с. – (Высшее образование). Занятие № 13. ДИФТЕРИЯ, СКАРЛАТИНА. Цель занятия: изучить особенности течения скарлатины, научиться дифференцировать скарлатину с другими заболеваниями, протекающими с синдромом экзантемы. Изучить особенности дифтерии, осложнения, лечение и профилактику. Вопросы для самоподготовки: 1. Этиология, эпидемиология скарлатины 2. Патогенез скарлатины 3. Клиническая картина и диагностика 4. Осложнения скарлатины 5. Лечение и профилактика скарлатины 6. Этиология, эпидемиология, патогенез дифтерии 7. Клиническая картина дифтерии 8. Осложнения и прогноз 9. Диагноз и дифференцированный диагноз 10. Лечение дифтерии 11. Профилактика дифтерии Скарлатина – острое инфекционное заболевание, характеризующееся интоксикацией, ангиной и мелкоточечной экзантемой. Этиология и эпидемиология: одна из клинических форм стрептококковой инфекции. Возбудитель – В- гемолитический стрептококк группы А, продуцирующий токсин, который одинаков более чем у 100 типов стрептококка. Отчетливо выявляется сезонность – осень-зима. Дети до года болеют редко, т.к. имеют трансплацентарный иммунитет. Максимальная заболеваемость отмечается в возрастной группе от 3 до 8 лет. Основной источник инфекции – больной скарлатиной, ангинами, другими формами стрептококковой инфекции (назофарингит, рожа, импетиго, пневмония), а также реконвалесценты и носители стрептококка. Основной путь передачи инфекции - воздушно-капельный. Распространению стрептококка группы А способствуют запыленность воздуха, тесный контакт, и длительное пребывание источника инфекции в коллективе. Контактно-бытовой путь передачи – заражение через игрушки, предметы и вещи встречается преимущественно в детских дошкольных учреждениях. Возможна передача стрептококка пищевым путем – через молочные продукты, кремы. 973 Иммунитет: после перенесенной скарлатины вырабатывается стойкий антитоксический иммунитет. Патогенез: Входными воротами при скарлатине чаще всего являются небные миндалины, реже стрептококк проникает через поврежденную кожу. Из места внедрения он может распространятся лимфогенным, гематогенным путем. При скарлатине выделяют три тесно связанных между собой звена патогенеза: токсический, септический, аллергический. Размножение стрептококка в месте внедрения сопровождается выделением эритрогенного токсина и выраженной интоксикацией, что наблюдается в течение первых дней болезни и соответствует токсическому компоненту патогенеза. С самим возбудителем связывают септический компонент, что проявляется первичным воспалением в месте входных ворот , а также гнойными осложнениями (ангина, лимфаденит, отит и т.д.). Аллергическое звено патогенеза проявляется на 2-3 неделе болезни и обусловлено сенсибилизирующими субстанциями возбудителя, относящимися к веществам белковой природы. Аллергизация способствует развитию осложнений (гломерулонефрита, миокардита, синовиита, ревматических заболеваний). В патогенезе скарлатины имеет значение смена фаз вегетативной нервной деятельности, с чем связаны изменения со стороны сердечнососудистой системы. В начальной фазе – отмечает и повышение тонуса симпатического отдела вегетативной нервной системы, которая сменяется «вагус» - фазой. Изменения со стороны сердечно-сосудистой системы выявляется в период «вагус»-фазы. Клиническая картина: инкубационный период 2-7 дней. Заболевание начинается остро, с повышения температуры тела до 38-40, появляется головная боль, рвота и боль в горле (при глотании), увеличение подчелюстных лимфоузлов. К концу 1-х или на 2 сутки появляется мелкоточечная сыпь на гиперемированном фоне кожи. Сыпь в первые дни болезни ярко-красная, а к 3-4 дню бледнеет до слабо-розовой. Она локализуется преимущественно на сгибательных поверхностях конечностей, передней и боковых поверхностях шеи, боковых поверхностях груди, на животе, пояснице, внутренних и задних поверхностях бедер и голеней. На лице сыпь густо располагается на щеках, не покрывая бледный носогубный треугольник. Более насыщена сыпь на боковых поверхностях туловища, внизу живота, в естественных складках кожи в подмышечных паховых, локтевых, подколенных областях, могут быть петехии. Отчетливо выражен белый дермографизм. Характерна сухость кожи в сочетании отечностью кожных сосочков – «шагреневая кожа». Сыпь держится 3-7 дней и исчезает не оставляя пигментации, после сыпи начинается шелушение (ушные мочки, шея). Типично крупно-пластинчатое шелушение, особенно на ладонях и стопах. Ангина – постоянный симптом скарлатины. Типичной является яркая гиперемия ротоглотки – «пылающий зев», четко отграниченное и не распространяется на слизистую твердого неба, иногда выявляется мелкоточечная энантема на мягком небе. Ангина чаще носит катаральный характер, но может быть лакунарной или фолликулярной. Язык вначале густо обложен серо-желтым налетом, а со 2-3 дня начинает очищаться и становится красным с выраженными сосочками «малиновый язык». Регионарные лимфатические узлы увеличены, умеренно болезненны. Со стороны сердечно-сосудистой системы в первые дни болезни тахикардия и повышение АД (симпатикус - фаза), а в конце 1-й недели – брадикардия, расширение границ сердца, появление систолического шума, снижение АД (вагус - фаза). Изменения обычно держаться в течение 2-4 недель. В периферической крови в начальном периоде может быть лейкоцитоз нейтрофильного характера со сдвигом влево, повышение СОЭ. Типичные формы скарлатины по тяжести подразделяются на легкие, среднетяжелые и тяжелые. Критериями тяжести являются степень выраженности начального синдрома интоксикации и изменения в месте входных ворот. Легкая форма скарлатины в современных условиях встречается наиболее часто и характеризуется слабо выраженным синдромом интоксикации, умеренными изменениями 983 в зеве в виде катаральной ангины. Состояние детей остается удовлетворительным, температура тела не превышает 37,5-38,5С или нормальная. Возможны кратковременная головная боль, недомогание, боль в горле при глотании, однократная рвота. Мелкоточечная сыпь неяркая и необильная, угасает к 3-4 дню болезни, изменения в зеве сохраняются 4-5 дней. Среднетяжелая форма характеризуется значительной интоксикацией, температура повышается до 38,6-39,0С , рвота обычно повторная. Выражены изменения в зеве – ангина с яркой отграниченной гиперемией, нередко с нагноившимися фолликулами и выпотом в лакунах. На слизистых оболочках мягкого неба может наблюдаться точечная энантема. Мелкоточечная сыпь яркая, обильная, на гиперемированном фоне и держится 5-6 дней. У больных появляется тахикардия, приглушенность I тона. Тяжелая форма протекает с резко выраженными симптомами интоксикации (токсическая форма) или с тяжелыми септическими поражениями (септическая форма). Токсическая форма скарлатины развивается бурно и характеризуется резко выраженными симптомами интоксикации, температура тела повышается до 40С и выше, наблюдается повторная рвота, головная боль, возбуждение, потеря сознания, судороги. Сыпь яркая на гиперемированном фоне кожи, нередко с геморрагиями. Рано появляются и быстро нарастают симптомы поражения сердечно-сосудистой системы. Уже в первые сутки болезни возможно развитие инфекционно-токсического шока. Септическая форма скарлатины характеризуется развитием воспалительных и гнойно-некротических изменений, исходящих из первичного очага. Осложнения: По характеру подразделяют на специфические и неспецифические. Из специфических осложнений выделяют ранние (септические) и поздние (аллергические) осложнения. К септическим осложнениям относят шейный лимфоаденит, аденофлегмона шеи, отит, синусит, артрит, остеомиелит, менингит, к аллергическим, возникающим на 2-3 неделе болезни относят диффузный гломерулонефрит, синовит, аллергический миокардит, ревматизм. Неспецифические осложнения обусловлены другим этиологическим фактором (стафилококком, пневмококком и др.). Прогноз при скарлатине зависит от возраста и тяжести течения. Более неблагоприятен у детей раннего возраста, особенно при септической форме. Дифференциальный диагноз: проводится с псевдотуберкулезом, иерсиниозом, корью, краснухой, медикаментозной аллергией, энтеровирусной инфекцией с экзантемами, дифтерией зева, лакунарной ангиной. Лечение: Лечение может проводится как в стационаре, так и в домашних условиях. Госпитализации подлежат дети в возрасте до 2-х лет, больные со среднетяжелыми и тяжелыми формами, при наличии осложнений и сопутствующих хронических заболеваний, по эпидпоказаниям. Режим – постельный на весь острый период болезни, диета – соответственно возрасту, преимущественно молочно-растительная. Антибактериальная терапия обязательна у для всех больных независимо от тяжести заболевания. Наиболее эффективно назначение пенициллина – бензилпенициллина натриевая соль в дозе 500 000 – 100 000 ЕД/кг/сут в/м или в/в, длительность 7-10 дней. Можно использовать ампициллин. При легкой форме скарлатины можно использовать феноксиметилпенициллин для приема через рот в суточной дозе 100 мг/кг в 4 приема. При непереносимости антибиотиков пенициллинового ряда используют эритромицин (30-40 мг/кг/сут), рокситромицин, сумамед, цефалоспорины I поколения (цефалексин, цефазолин). При тяжелых формах скарлатины проводится дезинтоксикационная терапия в виде в/в капельного введения 10% р-ра глюкозы, 10% р-ра альбумина, гемодеза, реополиглюкина. Из симптоматических средств назначают препараты укрепляющие сосудистую стенку (аскорутин, дицинон), десенсибилизирующие (тавегил, супрастин, фенкарол), витамины. Лечение осложнений проводят по общим правилам с использованием антибиотиков, активных в отношении стрептококков, а при необходимости антибиотиков широкого спектра действия. 993 Профилактика: специфическая профилактика не разработана. Основное профилактическое мероприятия – раннее выявление и изоляция больных, проведение текущей и заключительной дезинфекции. Переболевших допускают в детский коллектив не ранее 22 дня от начала болезни, после исследования общего анализа крови, мочи, по показаниям ЭКГ. Дифтерия - острое инфекционное заболевание, характеризующееся явлениями общей интоксикации с преимущественным поражением сердечно-сосудистой и нервной систем, а также образованием фибринозной пленки на месте внедрения возбудителя. Этиология. Возбудители - токсигенные штаммы дифтерийной палочки (коринебактерии дифтерии, бациллы Лёффлера). Нетоксигенные штаммы способностью к токсинообразованию не обладают и заболевание не вызывают. Коринебактерии дифтерии устойчивы к воздействию различных факторов окружающей среды. Эпидемиология. Источником инфекции являются больной дифтерией или здоровый носитель токсигенной дифтерийной палочки. Передача инфекции осуществляется преимущественно воздушно-капельным путем, возможен и контактный механизм передачи. Контагиозный индекс составляет 6-15%. Наибольшее число заболеваний регистрируется в осенне-зимний период. Иммунитет после заболевания продолжается, как правило, не более 6 месяцев - 1года. В естественных условиях невосприимчивость к дифтерии связана с бытовой иммунизацией. Однако, основным способом создания коллективного иммунитета у населения является активная иммунизация против дифтерии (вакцины АКДС, АДС-М, АД-М). Патогенез. Начальные этапы патогенеза дифтерийного процесса связаны с адгезией и колонизацией коринебактерий дифтерии. Через 2-4 дня инкубационного периода бактерии кроме дифтерийного токсина (относится к группе бактериальных нейротоксинов) начинают продуцировать ряд факторов, к которым относится дерматонекротизин (некротоксин), вызывающий некроз клеток в месте локализации возбудителя, гемолизин и ферменты – гиалуронидаза, нейропептидаза и др. Из-за нарушения микроциркуляции повышается проницаемость сосудов, что приводит к формированию экссудата. Под воздействием тромбокиназы. Освобождающейся при некрозе эпителия, богатый фибрином экссудат свертывается, образуя на поверхности слизистой оболочки фибринозную пленку. В зависимости от характера экссудата, выстилающего слизистую оболочку в месте поражения воспаление может быть крупозным и дифтеритическим. Крупозное воспаление развивается на слизистой оболочке, покрытой однослойным цилиндрическим эпителием, - в дыхательных путях. Дифтеритическое воспаление развивается на слизистых оболочках, покрытых многослойным плоским эпителием, - в ротоглотке. В таком случае некротизируется не только эпителиальный покров, но и подслизистая ткань; пленка при этом плотно соединяется с тканями и с трудом отделяется. Только развитие дифтеритического воспаления может привести к развитию токсических форм заболевания. Дифтерийный токсин также вызывает парез лимфатических сосудов, что является причиной формирования отека. Токсин, образующийся на месте размножения, попадает в лимфо- и кровоток, разносится по всему организму и очень быстро фиксируется различными тканями, но специфически поражает сердечную мышцу, нервную систему, почки. Клиника. Дифтерия - классическая токсикоинфекция. Все клинические и морфологические проявления связаны с воздействием дифтерийного экзотоксина. Болеют дифтерией не только дети, но и взрослые. Среди детей заболевание встречается в основном у непривитых против дифтерии. Привитые заболевают при снижении противодифтерийного иммунитета, но заболевание у них протекает чаще стерто и легко. Инкубационный период при дифтерии 2-10 дней. Входными воротами служат слизистые оболочки зева, носа, верхних дыхательных путей, реже глаз, половых органов, а также поврежденные кожные покровы. Наиболее частой локализацией дифтерийного процесса (90-95% от всех случаев заболевания) являются дифтерия зева (ротоглотки), которая подразделяется на локализо100 3 ванную (налеты на миндалинах), распространенную (налеты выходят за пределы слизистой миндалин, распространяясь на дужки, малый язычок, заднюю стенку глотки) и токсическую (преобладают симптомы интоксикации). Локализованная форма дифтерии ротоглотки в свою очередь подразделяется на островчатую и пленчатую. При локализованной дифтерии ротоглотки начало заболевания, как правило, постепенное. Больные жалуются на нерезкую боль в горле при глотании, головную боль, слабость, недомогание. При осмотре больного обращает на себя внимание бледность, безболезненное открывание рта, в зеве слабая или умеренная гиперемия. Характерен отек миндалин, дужек, язычка. На миндалинах имеются налеты в виде островков (островчатая форма) или сплошных участков (пленчатая форма). Налеты беложелтого цвета (иногда серого), с четкими контурами, снимаются с трудом, плохо растираются (как бы "пружинят"), фибринозная пленка возвышается над поверхностью слизистой оболочки ("плюс ткань"). После снятия налетов возможна кровоточивость поверхности слизистой. Отсутствие ряда из этих признаков не исключает дифтерии, особенно у привитых детей. Характерна слабая реакция регионарных (подчелюстных) лимфатических узлов. Для распространенной формы дифтерии ротоглотки характерна выраженная интоксикация, распространение фибринозных налетов за пределы миндалин – на язычок, мягкое небо, слизистую полости рта, большая их величина и толщина. Чаще встречается симптом кровоточивости. Токсическая форма дифтерии ротоглотки отличается от локализованной и распространенной обязательным наличием отека подкожной клетчатки шеи. В зависимости от его распространенности выделяют три степени: при I степени - отек до середины шеи, при II степени - доходит до ключицы (с одной или с обеих сторон), при III степени - спускается на грудную клетку. Обнаружение отека подкожной клетчатки является важным (или даже решающим) признаком для диагноза, терапии и исходов заболевания. Обязательное условие для диагностики - наличие массивных фибринозных налетов на миндалинах и за их пределами. Выражена интоксикация (слабость, рвота, анорексия и др.). Общее состояние больного тяжелое, отмечаются высокая температура (39-400С), слабость, адинамия. Выделяют также субтоксическую и гипертоксическую (молниеносную) формы. При субтоксической дифтерии отмечается отек подкожной клетчатки шеи, располагающийся вокруг регионарных лимфатических узлов. Гипертоксическая форма характеризуется внезапным началом, резко выраженной интоксикацией (температура до 40 - 410C, частая рвота, затемнение сознания, нередко судороги), гемодинамическими и микроциркуляторными нарушениями. Развивается инфекционно-токсический шок (слабый пульс, падение АД, тахикардия, одышка, олигурия, геморрагический синдром). Может возникнуть синдром острой надпочечниковой недостаточности (синдром Уотерхауза-Фридериксена). В ротоглотке обширные налеты, которые как бы "замуровывают" миндалины, просвета между ними нет. Отек подкожной шейной клетчатки соответствует токсической дифтерии III степени. Смерть может наступить в первые 3-4 дня болезни при явлениях сердечной недостаточности и коллапса. Ранняя диагностика дифтерии ротоглотки основывается только на клинических симптомах. Отрицательный результат бактериологического исследования при типичной клинической картине дифтерии не является поводом к отмене клинического диагноза дифтерии. Примеры постановки диагноза. 1. Дифтерия ротоглотки, локализованная (островчатая) форма. 2. Дифтерия ротоглотки, токсическая форма 1 степени. Осложнения дифтерии связаны со специфической интоксикацией и развиваются, как правило, при токсических формах, при поздно начатом лечении противодифтерийной сывороткой. Наиболее частые осложнения дифтерии: инфекционно-токсический шок, миокардит, полирадикулоневриты изолированное поражение черепных нервов, инфекци101 3 онно-токсический нефроз. Парез мягкого неба, возникающий после перенесенной "ангины", в большинстве своем является осложнением дифтерии ротоглотки, которая была несвоевременно распознана. Такие дети должны направляться в инфекционные стационары. Диагноз и дифференциальный диагноз. Дифтерию ротоглотки диагностируют на основе клинических данных, лабораторные методы исследования имеют лишь вспомогательное значение. Из методов лабораторной диагностики дифтерии наибольшее значение имеет бактериологическое исследование. Оно является обязательным у всех детей с наложениями на слизистой носа и ротоглотки. Для подтверждения диагноза решающее значение имеет выделение токсигенного штамма коpинебактерий дифтерии, особенно в сомнительных и сложных для диагностики случаях. Применяются и серологические методы исследования (РНГА, ИФА). Однако они являются ретроспективными. Дифференцировать дифтерию ротоглотки нужно в первую очередь от ангин, инфекционного мононуклеоза, эпидемического паротита и др. Большинство ангин кокковой этиологии имеют сходные общеинфекционные признаки: острое начало заболевания (температура 38-390C), интоксикация, боль в горле, болезненность регионарных лимфатических узлов. При осмотре зева определяются яркая гиперемия миндалин и их инфильтрация. При лакунарной ангине наложения находятся в лакунах и состоят из гноя, детрита, слизи, легко снимаются шпателем и растираются. Труднее дифференцировать от дифтерии лакунарные ангины, при которых налеты частично носят фибринозный характер. В таких случаях ребенка лучше направить в стационар с диагнозом "Лакунарная ангина, дифтерия ротоглотки?". Фолликулярная ангина у детей встречается реже, чем лакунарная. От дифтерии ее отличают более высокая температура, выраженная интоксикация и сильная боль в горле. Под слизистой миндалин определяются желтоватые нагноившиеся фолликулы, не снимающиеся шпателем. Пленчатую локализованную дифтерию ротоглотки приходится дифференцировать от некротической ангины. В отличие от дифтерии наложения грязно-серого цвета, бугристые. При снятии шпателем они крошатся и растираются. Может быть неприятный запах изо рта. Очень тяжело протекает флегмонозная ангина (паратонзиллит). Характерны симптомы, не свойственные дифтерии (резкая интоксикация и боль при глотании, вплоть до невозможности проглотить слюну, тризм). Поражение чаще всего одностороннее, отмечаются резкое выбухание миндалин в просвет зева, инфильтрация паратонзиллярной клетчатки. В отличие от токсической дифтерии зева фибринозных налетов на миндалинах, как правило, не бывает, отсутствует отек подкожной шейной клетчатки. Токсическую форму дифтерии приходится дифференцировать от инфекционного мононуклеоза (ИМ), при котором увеличиваются шейные лимфатические узлы (в виде пакетов), что оценивается как отек подкожной клетчатки. Лимфоузлы при ИМ плотноватые, мало болезненные, хорошо контурируются. Отек при дифтерии мягкой консистенции, легко изменяет локализацию при перемене положения тела. Поражение зева при ИМ вызывается бактериальной флорой и имеет признаки, характерные для ангин. Однако, налеты чаще рыхлые, белые, неравномерной толщины, легко снимаются. Заболевание развивается более медленно, чем дифтерия, при которой на 3-5-й день, несмотря на нарастание фибринозных налетов, температура часто становится нормальной. Для ИМ характерно на 1-2-й неделе заболевания увеличение печени и селезенки, в крови обнаруживаются атипичные мононуклеары. При подозрении на дифтерию больного надо госпитализировать. Токсическую форму дифтерии ротоглотки иногда принимают за эпидемический паротит (ЭП). Однако, чаще всего это связано с неправильной оценкой поражения зева и расположения отека. При ЭП отек находится спереди и сзади ушной раковины, плотный на ощупь и не имеет тенденции распространяться вниз на шею. В зеве фибринозные нале- 102 3 ты не наблюдаются. Ошибочный диагноз чаще всего является результатом неопытности врача или его "забывчивости" (зев не осматривается вообще). Дифтерия дыхательных путей (дифтерийный круп) - одна из наиболее тяжелых форм инфекции. Описание дифтерийного крупа приведено в разделе "Синдром крупа". Дифференциальную диагностику проводят с крупом, возникшим при ОРВИ. Другие локализации дифтерийного процесса (нос, глаза, кожа и др.) встречаются реже, нередко в виде комбинированных форм (с дифтерией ротоглотки). Лечение. Госпитализация больных при подозрении на дифтерию обязательна. Перед госпитализацией необходимо взять материал из зева и носа на дифтерийную палочку. В направлении на госпитализацию врач должен указать форму дифтерии, определить тяжесть заболевания и имеющиеся осложнения. Противодифтерийная сыворотка (используется высокоочищенная лошадиная гипериммунная сыворотка "Диаферм") на участке, как правило, не вводится. Немедленное введение противодифтерийной сыворотки (ПДС) обязательно при токсических формах дифтерии, если транспортировка больного в стационар по какимлибо причинам задерживается. Сначала проводится проба на чувствительность к лошадиному белку. Сыворотку, разведенную 1:100, вводят в объеме 0,1 мл внутрикожно в сгибательную поверхность предплечья. Через 20 минут неразведенную сыворотку вводят подкожно в объеме 0,1 мл, и если нет местной или общей реакции, лечебную дозу вводят через 30-45 минут внутримышечно. В случае положительной кожной пробы (диаметр покраснения и отека более 1 см) или при реакции на подкожное введение ПДС проводится дробная десенсибилизация (по инструкции). Если возникает необходимость вводить ПДС при токсических формах дифтерии в домашних условиях, то вначале делают внутримышечно инъекцию преднизолона (60-120 мг). Таблица 23. Дозы противодифтерийной сыворотки при различных формах дифтерии Клинические формы дифтерии Дифтерия ротоглотки Локализованная: островчатая пленчатая Распространённая Субтоксическая Токсическая Iстепени II степени III степени Гипертоксическая Дифтерийный круп: локализованный распространенный Редкие формы Изолированные Доза сыворотки (тыс. АЕ) первая на курс 10 – 15 15 – 40 30 – 50 40 – 60 10 – 20 30 – 50 50- 70 60 – 100 60 - 80 80 – 100 100 – 150 150 – 200 100 – 180 120 – 220 220 – 350 350-450 15 – 20 30 – 40 30 – 40 60- 80 (до 100) 10 –15 15 – 30 Эффективность ПДС зависит от сроков ее введения от начала заболевания. Противодифтерийную сыворотку вводят по Безредко. Первичная доза составляет 1/2 -1/3 от курсовой, вводится в/м при локализованных формах заболевания, в/в капельно – при токсических формах. Сыворотка вводится однократно (при локализованных формах) или 2-3 раза в сутки (при токсической дифтерии). Длительность лечения ПДС зависит от динамики исчезновения фибринозных налетов и шейного отека (до 2-3-х дней при токсических формах). Важно учитывать суммарную дозу сыворотки. При так называемой "лабораторной" 103 3 дифтерии сыворотка вводится только при наличии в зеве фибринозных налетов. Отсутствие наложений в зеве является условием отказа от применения ПДС. В последнее время используются специфический иммуноглобулин (с высоким содержанием дифтерийных антитоксинов), гипериммунная противодифтерийная плазма, при этом доза ПДС уменьшается. При дифтерии обязательно назначаются антибиотики: при локализованных формах - макролиды (эритромицин, сумамед, клацид, рулид), при токсических формах - цефалоспорины 1-2 поколения, пенициллин, аминогликозиды. Продолжительность антибиотикотерапии составляет от 5-7 до 8-10 дней. Патогенетически при токсических формах обосновано применение кортикостероидных препаратов. Назначают преднизолон (до 5-l0 мг на 1 кг массы в сутки), дексаметазон, гидрокортизон и др. (расчет дозировки проводится по преднизолону). Основной способ введения - внутривенный, длительность применения - от 1-2 до 3-5 дней. Детоксикация проводится путем внутривенного введения реополиглюкина, гемодеза, нативной плазмы, альбумина, 5-10 % растворов глюкозы с кокарбоксилазой, аскорбиновой кислотой. В отличие от других острых инфекций, сопровождающихся интоксикацией, при дифтерии необходимо более тщательно соразмерять объемы вводимых жидкостей с состоянием сердечно-сосудистой системы (опасность развития ранних миокардитов) и возможность перегрузок. В качестве энергосберегающих препаратов применяют калийинсулиновые смеси, панангин, неотон в/в капельно 1 г/сут, цитохромы и др.. Следует воздержаться от использования сердечных гликозидов (коргликона, строфантина), вазопрессивных препаратов (эфедрина, адреналина), так как они увеличивают нагрузку на сердечную мышцу при развитии ранних миокардитов. Имеются данные об эффективности гемосорбции, перитонельного гемодиализа (при токсической дифтерии). Все более широкое применение находят медикаментозные средства, обладающие ангиагрегантным действием (трентал, курантил), ингибиторы протеаз (контрикал, трасилол и др.). Обязательно назначение витаминов: аскорбиновая кислота (внутривенно, внутрь), витамины В1, В6, А и др., десенсибилизирующая терапия. Лечение гипертоксических форм дифтерии проводится в реанимационном отделении. Основные мероприятия направлены на борьбу с ИТШ. Лечение носителей токсигенных коринебактерий дифтерии (КБД) проводится в стационаре только после повторного их высева антибиотиками и антибактериальными препаратами (эритромицин, декаметоксин - септифрил, тетрациклин и др.). Курс лечения 5-7 дней. Дозы антибиотиков возрастные. Носители нетоксигенных КБД изоляции и лечению не подлежат. Изоляция больного дифтерией прекращается после клинического выздоровления и двукратного исследования (с отрицательным результатом) отделяемого из зева и носа, проводимого с 2-х дневным промежутком. Постстационарное лечение и диспансеризация. Реконвалесценты подлежат диспансерному наблюдению, цель которого - выявить поздние осложнения и провести реабилитационные мероприятия. Осложнения при дифтерии могут наблюдаться при любой форме дифтерии, в том числе локализованной. Это обусловлено тем, что у привитых детей и взрослых дифтерия имеет сходство с ангиной, часто диагноз ставится только после бактериологического обследования. Кроме того, позднее введение (после 5-го дня) ПДС, как правило, не предотвращает возможность развития осложнений (миокардит, парез мягкого неба и др.). Диспансерное наблюдение проводят участковый врач или врач общей практики с привлечением кардиолога, невропатолога, оториноларинголога. Сроки диспансеризации определяются тяжестью, форм дифтерии и характером осложнений. После перенесенной локализованной и распространенной формы диспансерное наблюдение продолжается от 1 до 3-х месяцев, при токсической 1 степени - до 6 месяцев, при токсической II-III степени - не менее 1 года. В первый месяц после выписки из стационара ребенка наблюдают 2 раза в месяц, затем - 1 раз или реже (по состоянию ребенка). Примерный объем ла104 3 бораторного обследования: анализ крови, мочи, ЭКГ, АСТ, СРБ и бактериологические анализы. Профилактика. В очаге дифтерийной инфекции заболевание ангиной с наложениями или крупом рассматривают, как подозрение на дифтерию. Такие больные подлежат провизорной изоляции, также как и носители токсигенных каринобактерий дифтерии. Все бактерионосители должны быть осмотрены врачом - оториноларингологом. Антибиотики (тетрациклин, эритромицин, левомицетин), назначают только после повторного высева токсигенных каринобактерий дифтерии. Курс лечения продолжается от 5 до 7 дней, дозы возрастные. Изоляцию носителей токсигенных каринобактерий дифтерии прекращают после двукратного бактериологического обследования с отрицательным результатом. Носители нетоксигенных каринобактерий дифтерии не подлежат госпитализации и лечению антибиотиками. По контакту с больным и носителями токсигенных каринобактерий дифтерии немедленно проводят одномоментное, однократное бактериологическое обследование. Необходимо медицинское наблюдение за детьми, бывшими в контакте с дифтерией, в течение 7 дней с момента изоляции больного или носителя. С целью полного выявления всех больных дифтерией и особенно со стертыми формами проводят обязательное активное наблюдение за больными ангиной в течение не менее 3 дней от начала заболевания. Все больные ангиной подлежат бактериологическому обследованию на коринебактерии дифтерии. Основой профилактики дифтерии является активная иммунизация. Вакцинацию АКДС-вакциной начинают делать детям с трехмесячного возраста. Вопросы для тестового контроля № п/п 1 2 3 4 5 6 7 8 9 10 Содержание вопросов Укажите характер сыпи при скарлатине: а/ пятнисто-папулезная; б/ мелкоточечная; в/ на неизмененном фоне кожи; г/ на гиперемированном фоне кожи; д/ появляется на 1-2 сутки болезни; е/ наиболее выражена в естественных складках кожи; ж/ появляется на 5-6 день болезни Поздние осложнения скарлатины это: а/ диффузный гломерулонефрит; б/ аллергический миокардит; в/ ревматизм; г/ отит; д/ лимфаденит Антибиотиками выбора при скарлатине являются: а/ канамицин; б/ тетрациклин; в/ пенициллин; г/ эритромицин; д/ ампициллин Доза антитоксической сыворотки, вводимой больному зависит от: а/ массы ребенка; б/ клинической формы; в) возраста; г) длительности заболевания Локализованную дифтерию ротоглотки характеризуют: а/ температура свыше 40°С ; б/ резкая боль при глотании; в/ гиперемия зева с синюшным оттенком; г/ налеты не выходящие за пределы миндалин; д/ незначительное увеличение регионарных лимфатических узлов; е/ отек клетчатки шеи Типичными осложнениями токсической дифтерии являются: а/ пневмония; б/ миокардит; в/ сепсис; г/ полирадикулоневрит; д/ гломерулонефрит; е/ менингит Легкая форма скарлатины характеризуется: а/ умеренными изменениями в зеве в виде катаральной ангины; б/ температура тела не превышает 37,538,5 С ; в/ многократная рвота; г/ однократная рвота; д/ обильная мелкоточечная сыпь; е/ неяркая и необильная сыпь Легкая форма скарлатины характеризуется: а/ яркая отграниченная гиперемия зева; б/ температура тела 38,6-39,0 С ; в/ однократная рвота; г/ повторная рвота; д/ неяркая и необильная сыпь; е/ обильная мелкоточечная сыпь Курсовая доза противодифтерийной сыворотки при распространенной форме дифтерии ротоглотки: а/ 50-70 тыс. АЕ; б/ 30-40 тыс. АЕ в/ 80-90 тыс. АЕ; г/ 100-120 тыс. АЕ; д/ 150-200 тыс. АЕ Курсовая доза противодифтерийной сыворотки при токсической форме дифтерии I степени: а/ 50-70 тыс. АЕ; б/ 30-40 тыс. АЕ; в/ 100-180 тыс. АЕ; г/ 100-120 тыс. АЕ; д/ 150-200 тыс. АЕ 105 3 Эталоны ответов б, г, д, е а, б в, г, д б в, г, д б, г а, б, г, е а, б, г, е а в Ситуационные задачи № п/п 1 2 Содержание задач Эталоны ответов По вызову на дому осмотрена девочка 5-и лет. Заболевание началось остро, с повышения температуры тела до 37,5С, отмечались однократная рвота и боль в горле (при глотании). На 2 сутки от начала заболевания появились высыпания на коже. Девочка посещает детское дошкольное учреждение, где отмечался подобный случай заболевания. При осмотре ребенка: мелкоточечная необильная сыпь на гиперемированном фоне кожи, которая локализовалась преимущественно на сгибательных поверхностях конечностей, боковых поверхностях груди, на животе, внутренних и задних поверхностях бедер и голеней; на лице сыпь располагается на щеках, носогубный треугольник бледный. При пальпации увеличение подчелюстных лимфоузлов. При осмотре зева – умеренная гиперемия ротоглотки, четко отграниченная. Анализ крови: Нb – 120 г/л, эритроциты – 4,0 х1012 г/л, лейкоциты – 15,2х109 г/л, э- 2 %, п – 1%, с – 59 %, л – 43%, М – 4%, СОЭ – 20 мм/ч Вопросы: 1.Ваш предполагаемый диагноз? 2. Тактика лечения. 3. Профилактические мероприятия. По вызову на дому осмотрен мальчик 6-и лет. Заболевание началось постепенно постепенное: жалобы на нерезкую боль в горле при глотании, головную боль. Температуры тела повысилась до 37,5С. Родители отмечали слабость, недомогание ребенка, плохой аппетит. При осмотре больного обращает на себя внимание бледность, безболезненное открывание рта, в зеве отечность миндалин, небных дужек, умеренная гиперемия с цианотичным оттенком. На миндалинах имеются налеты в виде островков налеты беложелтого цвета с четкими контурами, снимаются с трудом, возвышаются над поверхностью слизистой оболочки ("плюс ткань"). Отмечается слабая реакция регионарных (подчелюстных) лимфатических узлов. Вопросы: 1.Поставить предварительный диагноз. 2.Тактика лечения. 3.Какова продолжительность диспансерного наблюдения после перенесенного заболевания? 1.Диагноз: Скарлатина, типичная форма, легкой степени тяжести 2.Лечение: Лечение в домашних условиях. Режим – постельный на весь острый период болезни, диета – соответственно возрасту, преимущественно молочно-растительная. Антибактериальная терапия - назначение пенициллина – бензилпенициллина натриевая соль в дозе 100 000 ЕД/кг/сут в/м, 4 раза/ сутки, длительность 7 дней (можно использовать феноксиметилпенициллин для приема через рот в суточной дозе 100 мг/кг в 4 приема). Из симптоматических средств назначают препараты укрепляющие сосудистую стенку (аскорутин). 3. Профилактика: основное профилактическое мероприятия – изоляция больной, проведение текущей и заключительной дезинфекции, установить карантин в детском саду 7 дней с момента изоляции. Ребенка допускают в детский коллектив не ранее 22 дня от начала болезни, после исследования общего анализа крови, мочи. 106 3 1. Диагноз: Дифтерия ротоглотки, локализованная (островчатая) форма.. 2. Лечение: Обязательная госпитализация в стационар. Постельный режим. Необходимо введение противодифтерийной сыворотки. Сначала проводится проба на чувствительность к лошадиному белку. Сыворотку, разведенную 1:100, вводят в объеме 0,1 мл внутрикожно в сгибательную поверхность предплечья. Через 20 минут неразведенную сыворотку вводят подкожно в объеме 0,1 мл, и если нет местной или общей реакции, лечебную дозу вводят через 30-45 минут внутримышечно, курсовая доза 20 тыс. АЕ, однократно. Показано применение антибактериальной терапии – эритромицин перорально 30-50 мг/кг, курс 7 дней. Обязательно назначение витаминов: аскорбиновая кислота (внутрь), витамины В1, В6, А и др., назначается жаропонижающая, десенсибилизирующей терапии. 3. Диспансерное наблюдение 1 месяц с осмотром кардиолога, невропатолога, отоларинголога. Рекомендуемая литература. Основная: 1.Н.И. Нисевич, В.Ф. Учайкин. Инфекционные болезни у детей. - М., Медицина, 2008. – 790 с. Дополнительная: 1. Инфекционные болезни у детей // Под редакцией В.В. Ивановой- М., Мед. Информационное агентство, 2002. 2. Инфекционные болезни у детей / под редакцией профессора Э.Н. Симованьян - Ростов на Дону: Феникс, 2007, - 766 с. Занятие № 14. ОСТРЫЕ ВИРУСНЫЕ ГЕПАТИТЫ Впервые желтуха, как болезнь эпидемиологического характера была описана Гиппократом в раннем западноевропейском литературном источнике и датирована 751 г. Желтуха - одно из наиболее ярких проявлений вирусного гепатита, заболевание является одним из распространенных среди вирусных инфекций, имеющих тяжелые последствия. Цель занятия: изучить особенности течения острого вирусного гепатита, в зависимости от нозологической формы, научиться дифференцировать каждую форму острого гепатита от других заболеваний печени и желчевыводящих путей на основе этиологии, эпидемиологии, патогенеза, клиники, лабораторного исследования, понять принципы терапии, профилактики и диспансеризации заболевания. Вопросы для самоподготовки: 1. Этиология, эпидемиология вирусных гепатитов. 2. Патогенез вирусного гепатита А. 3. Нозологические формы острого гепатита. 4. Клиника вирусного гепатита. 5. Дифференциальная диагностика на основе серологических маркеров. 6. Принципы профилактики и лечения гепатитов. 7. Диспансерное наблюдение после перенесенного острого вирусного гепатита. Острые вирусные гепатиты – это группа острых вирусных инфекций, протекающих с диффузным воспалением печени, включающая несколько самостоятельных нозологических форм, имеющих свои патогенетические, клинические и эпидемиологические особенности. В настоящее время известно множество разновидностей вирусного гепатита (табл. 23). Таблица 23 Сравнительная характеристика вирусных гепатитов A (HAV), B (HВV), C (HСV), D(HDV) и E (HEV). ВозбудиHAV HBV HCV HDV HEV тель Геном Семейство Инкубационный период, дни РНК Пикорнавирусы ДНК Гепаднавирусы РНК Флави- и пестивирусы РНК Вироид РНК Калицивирусы 15 - 45 30 - 180 15 - 150 30 - 180 15 - 60 Путь передачи Фекальнооральный Острая атака Зависит от возраста + Сыпь Парентеральный половой, перинатальный Мягкая или тяжелая Парентеральный, половой перинатальный Парентеральный, перинатальный (случаи) Фекальнооральный Обычно мягкая Мягкая или тяжелая Обычно мягкая + + + + 107 3 Серодиагностика Анти- HAV Ig АнтиHBcIgM HBsAg, HBV-ДНК Анти-HCV HCV-РНК Анти-HDV IgM, HDV- РНК Анти-HEV IgM Максимальная активность АлАТ, МЕ/л Профилактика 800 - 1000 1000 - 1500 300 - 800 1000 - 1500 800 - 1000 Вакцинация - - - Лечение Симптоматическое Вакцинация Симптоматическое, противовирусное Симптоматическое, противовирусное Симптоматическое, противовирусное Симптоматическое При сборе анамнеза необходимо уточнить национальную принадлежность, контакты, недавние путешествия, инъекции, наличие татуировок, лечение у стоматолога, трансфузии, гомосексуализм, употребление в пищу моллюсков, применение больным лекарств в течение 2 мес. до начала заболевания. Вирусный гепатит А - наиболее распространен. Вирус попадает в организм через инфицированные предметы обихода, реже с пищей или через инфицированную воду (водный путь заражения). Заболевание носит циклический характер с четкой сменой периодов заболевания и, как правило, наступает выздоровление. Появлению желтухи предшествует продромальный период длительностью от 3-4 суток до нескольких недель. Больной предъявляет жалобы на плохое самочувствие, диспепсические явления, отсутствие аппетита, тошноту. В поздние сроки отмечается субфебрилитет, боль в правом верхнем квадранте живота, усиливающаяся при резком движении, выраженное нарастание слабости к вечеру, измождение, головная боль, которая в сочетании с ригидностью затылочных мышц у детей заставляет заподозрить менингит. К концу продромального периода темнеет моча и обесцвечивается кал и отмечается клиника желтухи с развитием которой нормализуются: температурная кривая, аппетит, прекращается рвота, исчезает дискомфорт в области живота. В течение нескольких дней отмечается преходящий зуд. У 70% больных пальпируется мягкий край увеличенной печени, поколачивание в области задних отделов нижних ребер справа вызывает болезненные ощущения. На коже могут появляться преходящие сосудистые звездочки. Длительность желтушного периода составляет 1-4 недели, затем состояние больного улучшается вплоть до полного выздоровления, хотя может в течение нескольких недель сохраняться слабость, повышенная утомляемость, а в тяжелых случаях неврологические осложнения. Клиническое выздоровление и восстановление биохимических показателей обычно происходят в течение 6 месяцев после начала заболевания. Однако острый гепатит В и С могут переходить в хронический. Нередко, для гепатита А характерно течение длительного холестаза, сопровождающегося поздним появлением кожного зуда (в течение 3 нед.), нарастающей желтухой на протяжении 8 – 29 недель. Рецидивы заболевания наблюдаются в 1,8 – 15 % случаев и обусловливаются чрезмерной активностью больного. Редкой формой заболевания является фульминантный гепатит, при котором желтуха или не успевает появиться или развивается выраженная с угрожающей повторной рвотой, печеночным запахом, сопором, сонливостью, «хлопающим» тремором, ригидностью затылочных мышц, развитием коматозного состояния, характерного для острой печеночной недостаточности, выраженными изменениями в системе свертывания крови. Заболевание заканчивается смертью больного в течение 10 дней. Фульминантное течение наблюдается при вирусном гепатите А, В и Е. Таблица №22 Классификация клинических проявлений и исходов вирусных гепатитов. 108 3 Выраженность клинических проявлений а) клинические - желтушные, - стертые, - безжелтушные; б) субклинические (иннапарантные) варианты Цикличность течения а) острое; б) затяжное (подострое); в) хроническое Тяжесть Осложнения а) легкая форма; б) среднетяжелая форма; в) тяжелая форма; г)фульминант ная (молниеносная) форма а) острая печеночная энцефалопатия: ОПЭ I–II стадии (прекома), ОПЭ III–IV стадии (кома); б) обострения: - клинические, - ферментативные; в) функциональные и воспалительные заболевания желчных путей Исходы и последствия а) выздоровление; б) остаточные явления: -постгепатитная гепатомегалия, -затяжная реконвалесценция; в) затяжной гепатит; г) бессимптомное вирусоносительство; д) хронический персисти-рующий гепатит; е) хронический активный гепатит; ж) цирроз печени; з) первичный рак печени При лабораторном исследовании: билирубин появляется в моче до развития желтухи, позже он исчезает, несмотря на сохранение повышенного уровня в сыворотке крови. Уробилиногенурия обнаруживается в поздней преджелтушной фазе. На высоте желтухи лишь небольшое количество билирубина поступает в кишечник и уробилиноген исчезает, кал обесцвечивается. Повторное появление уробилиногена в моче свидетельствует о начинающемся выздоровлении и сопровождается восстановлением цвета кала. Уровень билирубина в сыворотке колеблется в широких пределах, повышение конъюгированной фракции отмечается рано даже при нормальном уровне общего билирубина. Активность щелочной фосфатазы (ЩФ) менее чем в 3 раза превышает верхнюю границу нормы, но при холестатическом варианте возрастает в 5 – 10 раз, протеинограмма изменена незначительно при тяжелых формах с дальнейшей гипоальбуминемией и умеренной гиперглобулинемией, уровень железа и ферритина повышены. У 1/3 больных в острой фазе болезни повышается уровень IgG и IgM. Активность сывороточных трансаминаз играет важную роль в ранней диагностике, выявлении безжелтушных форм и латентного течения гепатита в эпидемиологических очагах, максимально повышаясь в 20-50 раз выше нормы за 1-2 сут до или в первые дни возникновения желтухи, может оставаться повышенной в течение 6 мес. после полного выздоровления. Гепатит А. Этиология, эпидемиология: Гепатит А - острое воспаление печени, вызываемое РНК-содержащим симметричным кубическим пикорнавирусом (27 нм), передающееся энтеральным путем, обычно заканчивающееся самоизлечением. Заболевание составляет 2025 % клинически проявляющегося гепатита в экономически развитых странах. Наиболее часто заражаются дети 5-14 лет, инфицирование взрослых происходит при контакте с зараженными детьми. Распространению болезни способствуют перенаселение, несоблюдение правил личной гигиены и антисанитарные условия. К группе риска относятся: а) медицинский персонал (вследствие заражения от новорожденного с илеостомой, болеющего острым гепатитом А); б) больные гемофилией – при переливании обработанных детергентным растворителем концентраты фактора VIII, обусловленного вероятным инфицированием донорской плазмы HAV; в) дети в детских учреждениях; г) мужчины гомосексуалисты; д) лица, употребляющие в пищу замороженные фрукты – (водный, алиментарный путь передачи) в результате применения для удобрения почвы человеческих фекалий; е) лица, употребляющие в пищу сырые моллюски и устрицы из загрязненных водоемов. 109 3 Патогенез: Вирус, всасываясь из желудочно-кишечного тракта достигает печени, где и остается. Рис. .№ 6. Репликация вируса Вирусные белки синтезируются и упаковываются в пузырьки, которые выделяются в желчь. Вирус не оказывает прямого цитопатического действия, а повреждение гепатоцитов вызывается не репликацией вируса, а Т - клеточным иммунным ответом на инфекцию. Анти - HAV в сыворотке появляются после исчезновения вируса из кала, их титр достигает максимума в течение нескольких месяцев и обнаруживается в течение многих лет. Анти - HAV IgG, вероятно обеспечивают иммунитет против повторного инфицирования HAV. В диагностическом плане более важно выявление анти-HAV IgМ, наличие которых свидетельствует о текущей инфекции. Анти - HAV IgМ сохраняются лишь на протяжении 2-6 месяцев, и в редких случаях их низкий титр обнаруживают в течение 1 года от начала заболевания (Рис. № 7). Хроническое носительство HAV не выявлено. Вирусоносительство наблюдается часто, но в кале вирус обнаруживается периодически. Появление анти - HAV IgG свидетельствует о развитии стойкого иммунитета. Вирус Анти -HAV IgM в кале IgG Симптомы 800 40 АлАТ 400 20 Билирубин 0 0 0 20 40 60 80 100 Сутки Рис. № 7. Течение острого вирусного гепатита А Профилактические мероприятия: Больной острым вирусным гепатитом А является контагиозным в течение 2 недель до появления желтухи, а также при безжелтушном течении заболевания, т.е. еще до установления диагноза. По этой причине изоляция больных и контактировавших с ними лиц не влияет существенным образом на распростране110 3 ние гепатита. Вирус А относительно устойчив к инактивации теплом, эфиром или кислотой, но погибает при обработке формалином в разведении 1:4000 при t = 37 С в течение 72 ч, хлорировании в разведении 1:1000 000 в течение 30 мин и при воздействии микроволн. Пассивная иммунизация: Введение сывороточного человеческого иммуноглобулина объемом 5 мл в/м (детям 0,02 мл/кг) в течение 6 сут после инфицирования может служить мерой кратковременной (около 6 мес.) профилактики в 80 – 90 % случаев. Нецелесообразно проводить пассивную иммунизацию через 2 недели после контакта с инфекцией. Активная иммунизация: Иммуногенная вакцина, полученная путем инактивирования формальдегидом вирусных частиц при однократном введении 1 мл, обеспечивает быстрое (в течение 15 сут) формирование иммунитета. Повторное введение вакцины через 6 – 12 мес. в 95 % случаев формирует долговременный иммунитет. Высоко эффективно введение 1 дозы инактивированной вакцины у детей, а в Таиланде доказан протективный эффект длительностью не менее 1 года против HAV 2 доз вакцины. Вакцинации подлежат лица, относящиеся к группе риска. Гепатит В Этиология, эпидемиология: Гепатит В - острое воспаление печени, вызываемое ДНК-содержащим гепадновирусом (42 нм), передающееся парентеральным, половым, а также перинатальным путем, чаще сопровождается формированием длительного вирусоносительства и/или переходом в хронический гепатит и цирроз печени. Заболевание составляет 40-45 % клинически проявляющегося гепатита в экономически развитых странах. В настоящее время оно все чаще фигурирует как заболевание, передающееся половым путем, а также от инфицированной матери ее ребенку, если заболевание наблюдается в III триместре беременности и беременная становится не только HbsAg-положительной, но и одновременно HbeAg- положительной. Вероятность передачи HBV ребенку в I или II триместре беременности остается очень небольшой. В высокоэндемичных регионах заражение в детском возрасте происходит, вероятно, горизонтальным путем: через поцелуи, бытовые предметы (зубные щетки и лезвия) и при инъекциях, контакт в дошкольных учреждениях. Кровососущие членистоногие (москиты, постельные клопы) могут быть переносчиками инфекции. Парентеральное заражение возможно при использовании нестерильных инструментов, шприцев, игл наркоманами, стоматологами, косметических проколах ушей и маникюре, неврологическом обследовании, профилактических прививках, подкожных инъекциях, акупунктуре. К группе риска относятся обслуживающий больного персонал. Вирион гепатита В состоит из поверхностного слоя (1) и сердцевины (2) (Рис. № 8). Сердцевина (core) вируса формируется в ядре гепатоцитов и содержит ДНК-полимеразу, двухцепочечную ДНК, ядерный антиген и еантиген, а поверхностные частицы (HbsAg) – формируются в цитоплазме гепатоцитов. В сыворотке в свободном состоянии циркулируют сферические частицы и трубочки HbsAg. Описаны различные варианты генома HBV, которые образуются вследствие мутаций в разных рамках считывания. Рис. №8. Строение вириона гепатита В (HBV, частица Дейна). Отличить вирусный гепатит В от гепатита А в продромальную фазу или в клинической стадии без помощи лабораторных исследований не представляется возможным. Несколько лет назад было показано, что гепадновирусы могут поражать и другие органы 111 3 кроме печени, но дискутируется вопрос, является ли это следствием внепеченочной инфекции или опосредованно иммунологически. Клиническое течение острого гепатита В у взрослых более тяжелое, общая картина с другими формами острых гепатитов сходная. Лабораторные исследования включают определение трансаминаз, концентрацию билирубина и железа сыворотки крови, проведение электрофореза белков сыворотки. Точная диагностика возможна лишь с помощью дополнительных иммунологических исследований Рис. № 9. Динамика маркеров H BV В настоящее время определяются серологические маркеры вирусного гепатита В. (Рис.№ 9), (Табл. № 23). Профилактика пассивная проводится до заражения или в течение нескольких часов после него гипериммунным сывороточным глобулином с высоким титром антител. Вакцинация рекомбинантной вакциной проводится здоровым людям в/м в дозе 10 мкг (1 мл) дважды с интервалом 1 мес. с последующей ревакцинацией через 6 мес. после первого введения. При сохранении угрозы заражения следует проводить ревакцинацию через 5–7 лет. Контингент, подлежащий вакцинации против гепатита В: а) хирурги, стоматологи, студенты-медики; в) сотрудники больниц и лабораторий, контактирующие с кровью; в) больные и сотрудники онкологических, гематологических, гепатологических, нефрологических, психиатрических отделений; г) больные с психическими расстройствами; д) лица, случайно контактирующие с HBsAg-положительной кровью; е) лица, бывшие в тесном семейном и половом контакте с HBsAg-положительными носителями; ж) дети, рожденные от HBsAg-положительных матерей; з) дети при осуществлении расширенной программы иммунизации; и) наркоманы; к) мужчины – гомосексуалисты; л) лица, направляющиеся в районы высокого риска инфекции. Важно отметить, что именно эта форма гепатита часто переходит в хроническую, особенно это учитывается при пересадке органов. Гепатит Д HDV представляет маленькую частицу (36 нм), которая содержит РНК, покрытую HBsAg. HDV не способен к самостоятельной репликации, но может вызывать инфекцию при активации в присутствии вируса HBV. Заражение HBV и HDV может произойти одновременно (коинфекция), либо HDV может поражать хронического носителя HBsAg (суперинфекция). Передача вируса тесно связана с передачей вируса-помощника, т.е. HBV. Диагноз острого гепатита D ставят на основании повышенного титра в сыворотке анти-HDV IgG. Коинфекцию диагностируют по наличию в сыворотке анти-HDV IgM и высокого титра анти-HBc IgM, которые проявляются в течение 1 недели. Анти-HDV IgM исчезают к 5-6 неделе, что свидетельствует об излечении от HDV-инфекции, но могут персистировать на протяжении 12 нед – свидетельствует о хронизации процесса. При исчезновении анти-HDV IgM начинают выявляться анти-HDV IgG. Выявляют также HBsAg, однако в низком титре, или не обнаруживаются, снижение титра анти-HBc IgM, до выявления маркеров HDV может ошибочно ставится диагноз острого гепатита С. Клинически картина не отличима от гепатита В, однако может отмечаться двухфазный подъем активности АСТ, при этом второй пик обусловлен острым поражением HDV. Для суперинфекции HDV у носителей HBV характерны раннее появление в сыворотке анти-HDV IgM, почти одновременно с анти-HDV IgG, и персистенция обоих классов антител. У этих больных анти-HBc IgM обычно отсутствуют или выявляются в низких 112 3 титрах. HDV-инфекция угнетает репликацию HBV и у больных обычно отсутствуют HBeAg и HBV-ДНК. Вакцинация против гепатита В создает у реципиента иммунитет к HBV-инфекции и защищает против HDV-инфекции. Гепатит С Инкубационный период заболевания составляет от 5 до 12 нед, только у 25 % зараженных развивается желтуха, может протекать бессимптомно, у ВИЧ-инфицированных быстро прогрессирует. HCV-РНК может обнаруживаться в сыворотке через 1-2 нед после инфицирования. Активность сывороточных трансаминаз нарастает умеренно через 7-8 нед, превышая в 15 раз верхнюю границу нормы. При полном выздоровлении HCV-РНК в сыворотке не выявляется, но антитела персистируют в течение нескольких месяцев. Через год у большинства больных с посттрансфузионным гепатитом сохраняется повышенная активность трансаминаз. Разработка вакцин против HCV находится на начальном этапе. Гепатит Е HEV-РНк-содержащий вирус (32-34 нм), не покрытый оболочкой, клинически напоминает гепатит А, редко встречается у детей. Инкубационный период при заражении через кровь длится от 22 до 46 сут, а при фекально-оральном заражении от 34 до 46 сут. У 100 % больных возникает желтуха и отсутствуют внепеченочные проявления. HEV приводит к острой печеночной недостаточности в эндемичных районах, отмечается фульминантное течение заболевания. Летальность высокая среди беременных женщин в III триместре и составляет около 25%, проявляется острым геморрагическим синдромом, энцефалопатией и почечной недостаточностью. К профилактическим мерам относятся употребление чистой воды, соблюдение правил гигиены и повышение санитарной культуры. В связи с общим генотипом вируса возможна разработка вакцины. Таблица 23 Значение серологических маркеров в диагностике вирусных гепатитов. Маркер Анти-HAV IgM Анти-HAV IgG HBsAg HBcAg Анти-HBc IgM Анти-HBc IgG Анти-HBs HBeAg Анти-HBe ДНК– полимераза HBV-ДНК Анти- HDV IgM Анти- HDV IgG Значение Острый гепатит А Иммунитет к гепатиту А Гепатит А Гепатит В Появляется в крови через 6 нед после заражения в период клинической манифестации и исчезает через 3 мес. в фазу реконвалесценции, сохранение в сыворотке более 12 нед свидетельствует о переходе в хроническую форму, а более 6 мес. о вирусоносительстве Ядерный антиген, в периферической крови не выявляется, а методом иммунофлюооресценции выявляется в ядрах гепатоцитов Острый гепатит В (высокий титр) Хронический гепатит В (низкий титр), обнаруживаются после элиминации HBsAg из сыворотки в течение 6 мес. и более Контакт в анамнезе с больными гепатитом В (HBsAg-отрицательный) Хронический гепатит В (HBsAg-положительный) Выздоровление и формирование иммунитета, обнаруживаются после вакцинации. Появляются через 3 мес после начала заболевания в фазу реконвалесценции и сохраняются длительное время Продукт распада HbcAg, коррелирует с продолжающейся репликацией вируса и контагиозностью, ненадолго появляется в острой фазе, элиминируется раньше, чем HBsAg. Персистенция более 10 нед свидетельствует о хронизации Предвестник полного выздоровления, низкая контагиозность Активная репликации вируса при остром и хроническом гепатите (с наличием HbeAg) Продолжающаяся инфекция, следует определять у HbeAg –положительных и у анти-Hbeположительных пациентов, особенно при подозрении на хронический гепатит. Гепатит D Острая или хроническая инфекция, вызванная HDV Хроническая инфекция HDV (высокий титр с наличием анти- HDV IgM) Инфекция HDV в прошлом (низкий титр в отсутствие анти- HDV IgM) В преджелтушной стадии гепатит можно ошибочно принять за другие инфекционные болезни, синдром острого живота (аппендицит или гастроэнтерит). Наличие желчных 113 3 пигментов в моче, уплотнение и увеличение печени, и повышение активности сывороточных трансаминаз, исследование маркеров инфекции являются наиболее важными признаками в диагностике острого вирусного гепатита. В желтушной стадии дифференцируется с хирургическим внепеченочным холестазом, разграничение проводится с лекарственными реакциями на основании анамнеза. В постжелтушной стадии с хроническим гепатитом. Лечение вирусных гепатитов. Больные гепатитом в нашей стране госпитализируются. Основу терапии составляет постельный режим в период разгара болезни и рациональное питание. Пищевой рацион должен быть полноценным, но с ограничением тугоплавких жиров, экстрактивных веществ. Обработка пищи щадящая (паровая, отварная, молотая и др.). Обильное питье (5% раствор глюкозы и отвары легких желчегонных трав). В настоящее время разработаны протоколы лечения вирусных гепатитов В и Д, включающие назначение базисной терапии (ферменты, желчегонные, сорбенты, фитотерапия и т.д.) и назначение интерферонотерапии (виферон, интрон, реаферон и др.). Интерферонотерапия проводится длительно (от 6 мес. до 1 года), продолжительность курсов и дозы препаратов интерферона определяются индивидуально в зависимости от состояния функций печени, ее размеров и наличия маркеров вирусного гепатита. При выраженной интоксикации полезно проведение энтеральной дезинтоксикации (энтеродез по 2,5 – 5 г 4-5 раз в день 3-5 дней, с предварительным разведением в воде, чае, компоте). При повторных диспептических явлениях (тошнота, рвота) показана инфузионная терапия (глюкоза, электролиты), противорвотные препараты назначаются в низких дозах, ингибиторы протеаз, антибиотики. Кортикостероиды не оказывают влияния на степень печеночного некроза, скорость излечения и состояние иммунной системы, их применение оправдано лишь при холестатическом гепатите А в течение длительного периода выздоровления. Также используются урсофальк, урсосан, гепатофальк планта, адеметионин при мучительном зуде используются препараты, связывающие желчные кислоты или антигистаминные средства. Для лечения упорных болей в верхних отделах живота используются спазмолитики. Витамины. Возможно применение α-интерферона в старшем возрасте при вирусном гепатите С, с целью предупреждения хронизации процесса в дозе 5-6 млн ЕД 3 раза в нед в течение 3 мес., при гепатите В детям младшего возраста природный α-интерферон (вэлферон) до 10 МЕ/м2 3р/нед в течение 12 нед. Таблица 24 Диспансерное наблюдение реконвалесцентов вирусного гепатита Рекомендации Частота осмотра Кратность исследований - физикальный осмотр (жалобы, размеры печени и селезенки) - активность АЛТ, тимоловой и сулемовой пробы, билирубина - серологические маркеры Снятие с «Д» учета Вирусный гепатит А Через 1 мес. после выписки лечащим врачом стационара Через 1 мес. после выписки лечащим врачом стационара Через 1 мес. после выписки при отсутствии у реконвалесцентов клинических и биохимических отклонений; Через 3 мес. после выписки, реконвалесценты с остаточными явлениями берутся на учет в КИЗе, .где проводится повторное обследование Вирусный гепатит В Не позднее, чем через 1 мес. после выписки лечащим врачом стационара; в дальнейшем при отсутствии отклонений врачом КИЗа поликлиники через 3, 6, 9, 12 мес. после выписки при отсутствии отклонений в анализах наблюдение в КИЗе поликлиники через 3, 6, 9, 12 мес. после выписки из стационара При отсутствии хронизации процесса и двукратном отрицательном результате исследования на HBsAg, проведенного с интервалом 10 дней Рекомендации при выписке: 1) пищевой режим – диета № 5, освобождение от тяжелого физического труда и занятий спортом на 3-6 мес.; санторно - курортное лечение через 6 мес. после перенесенного заболевания. Противопоказаны профилактические прививки в течение 6 мес. (кроме противостолбнячной и антирабической вакцины), применение гепатотоксических препаратов, проведение плановых операций. Вопросы для тестового контроля: 114 3 № п/п 1 2 3 4 5 6 7 8 9 10 Содержание вопросов При типичной форме вирусного гепатита желтуха: а) наблюдается; б) не наблюдается Трансплацентарная передача вирусного гепатита В: а) возможна б) не возможна Передача вируса гепатита В осуществляется следующими путями: а) воздушно-капельный; б) пищевой; в) шприцевой; г) гемотрансфузионный При субклинической форме гепатита А отмечаются: а) увеличение печени; б) слабая иктеричность склер и кожи; в) повышение активности АЛТ в сыворотке крови; г) билирубинемия; д) выделение в моче желчных пигментов Характерными клинико-лабораторными показателями типичного гепатита А в период разгара являются: а) лихорадка; б) желтуха в) гепатомегалия; г) боли в мышцах и в суставах; д) увеличение показателя АЛТ При пальпации печени у больного гепатитом можно выявить: а) бугристую поверхность; б) увеличение размеров печени; в) острый край; г) плотно-эластическую консистенцию; д) болезненность во всех отделах Для безжелтушной формы острого вирусного гепатита характерен: а) повышенный уровень сывороточных трансаминаз; б) нормальный уровень сывороточных трансаминаз Гепатит Е наиболее неблагоприятно протекает у: а) детей раннего возраста; б) у детей школьного возраста и подростков; в) беременных женщин При вирусном гепатите А самочувствие больного с момента появления желтухи: а) ухудшается; б) улучшается При вирусном гепатите С часто отмечается: а) фульминантная форма; б) хронизация процесса; в) выздоровление Эталоны ответов а а в, г в б, в, д б, г, д а в б б Ситуационные задачи: № Содержание задач п/п 1. Больная Маша В..8 лет поступила в отделение с жалобами на тошноту, боли в животе, жидкий стул, повышение температуры тела до 38,4С. Из анамнеза известно, что вышеуказанные жалобы появились два дня назад. Ребенок от 1 беременности, которая протекала без особенностей. Роды в срок, в затылочном предлежании. Девочка развивалась соответственно возрасту, редко болела ОРВИ. Наследственность не отягощена. Объективно: общее состояние средней степени тяжести, кожные покровы умеренно бледные, чистые. Зев - слегка гиперемия. Носовое дыхание не затруднено. Тонус мышц сохранен. В легких дыхание везикулярное, хрипов нет. ЧД 26 в минуту. Тоны сердца ясные, ритм пра115 3 Эталоны ответов 1.Можно предположить, что имеет место вирусный гепатит А, преджелтушный период, либо безжелтушная форма острого вирусного гепатита А. 2.Лечение: Режим - постоянный. Диета - стол №5 по Певзнеру. Витамин Е, дезинтоксикационная терапия, внутривенное введение 10% раствора глюкозы с раствором Рингера (2:1). Кортикостероидные препараты преднизолон 1 мг/кг в течение 3-5 дней. Симптоматическая терапия - жа- 2. вильный. ЧСС - 96 в минуту. Живот при пальпации мягкий, болезненный в правом подреберье. Печень +3,0 см. из под края реберной дуги, селезенки не увеличена. Мочится достаточно, моча цвета пива с желтой пеной, стул ахоличный. В исследованиях крови: уровень билирубина (свободная форма) 10 мкмоль/л. АЛТ – 2,0ммоль/ч.л. АСТ – 2,4 ммоль/ч.л. Вопросы: О каком заболевании можно думать, чем обосновывается диагноз? Назначить лечение. Дифференциальный диагноз. Больной Сергей С., 10 лет поступил в отделение с жалобами на желтушное окрашивание кожных покровов, носовые кровотечения, кожный зуд, слабость, недомогание. Из анамнеза известно, что ребенок от 1 беременности, протекавшей на фоне токсикоза 2 половины, роды в срок без особенностей. Ребенок развивался не отставая от сверстников. Перенесенные заболевания: ОРВИ, острый аппендицит 3 месяца назад (проведена операцияаппендэктомия). Объективно: общее состояние средней тяжести. Кожные покровы, склеры желтые, отмечается зуд, расчесы. Носовое дыхание не затруднено, зев спокоен. Температура тела 36,8 С. В легких дыхание везикулярное. ЧД 20 в минуту. Тоны сердца ясные, ритм правильный, ЧСС - 96 в минуту. Границы сердца в пределах нормы. Живот при пальпации мягкий, болезненный в правом подреберье. Печень +2,0 см изпод края реберной дуги. Селезенка не увеличена. Лабораторные данные: в общем анализе - крови лейкопения, лимфоцитоз, СОЭ - 20 мм/ч. Билирубин крови - 80 мкмоль/л, АлАТ 3,2 мкмоль/ч.л., АСТ 2,4 мкмоль/ч.л. Протромбиновый индекс 0,4. Сулемовая проба 1,6 мл. Вопросы: 1.Поставить предположительный диагноз. 2.Наметить план обследования. 3.Назначить лечение.4.Дифференциальный диагноз. ропонижающие, мочегонные, транквилизаторы, ноотропы. 3.Дифференциальный диагноз: кишечные инфекции ОРВИ ревматизм острый аппендицит инфекционный мононуклеоз острый холецистит 1.Диагноз: Вирусный гепатит В, типичное течение средней степени тяжести, желтушный период. 2.Лабораторные исследования: трансаминазы, билирубин, железо сыворотки крови в динамике, ЭКГ, протеинограмма, серологические маркеры вирусного гепатита. В УЗИ органов брюшной полости, почек, копрограмма, общий анализ мочи, анализ мочи по Нечипоренко. 3.Лечение: Диета - стол №5 по Певзнеру. Режим - постельный. Витамин Е, дезинтоксикационная терапия, внутривенное введение 10% раствора глюкозы с раствором Рингера 2:1. Преднизолон 1 мг/кг 5 дней, затем отмена, постоянно снижая дозу; ингибиторы протеаз контрикал. 4.Дифференциальный диагноз: инфекционный мононуклеоз иерсиниоз токсический гепатит Рекомендуемая литература: Основная: 2. Нисевич Н.И., Учайкин В.Ф. Инфекционные болезни у детей. - М.: "Медицина", 2008, -790 с. Дополнительная: 1. Краснов В.В. Инфекционные болезни в практике педиатра. Нижний Новгород, 1997.-103 с. 116 3 2. Лечение вирусных гепатитов у детей. //Под ред. А.А.Баранова, В.Ф. Учайкина, Т.И.Чередниченко и др., М., 2003, 128 с. 3. Инфекционные болезни у детей / под редакцией профессора Э.Н. Симованьян Ростов на Дону: Феникс, 2007, - 766 с. – (Высшее образование). Занятие № 15. ОСТРЫЕ КИШЕЧНЫЕ ИНФЕКЦИИ Цель занятия: ознакомиться с вопросами эпидемиологии, этиопатогенеза наиболее распространенных кишечных инфекций у детей, изучить особенности клинических проявлений, диагностики и дифференциальный диагностики кишечных инфекций в детском возрасте, научиться составлять план лечения и профилактических мероприятий при кишечных инфекциях. Вопросы для самоподготовки: 1. Этиология сальмонеллеза, дизентерии, эшерихиозов. 2. Патогенез кишечных инфекций у детей. 3. Особенности клинических проявлений, диагностики дизентерии. 4. Классификация, клиника основных форм сальмонеллеза у детей. 5. Клинические проявления эшерихиозов у детей. Понятие о токсикозе с эксикозом. 6. Дифференциальный диагноз кишечных инфекций. 7. Принципы терапии острых кишечных инфекций у детей. Острые кишечные инфекции (ОКИ) – это большая группа инфекционных заболеваний человека с энтеральным (фекально-оральным) механизмом заражения, вызываемых патогенными (шигеллы, сальмонеллы и др.) и условно-патогенными бактериями (протей, клебсиеллы, клостридии и др.), вирусами (рота-, астро-, калици-, группы Норфолка и др.) и простейшими (амеба гистолитика, криптоспоридии, балантидия коли и др.), объединенных развитием диарейного синдрома. В общей структуре инфекционных заболеваний ОКИ составляют более 40% от всех госпитализированных больных, а в структуре инфекционной заболеваемости занимают второе место после ОРВИ и гриппа. В последние годы отмечается преобладание вирусных диарей в структуре всех ОКИ. Источником инфекции – является человек и/или животные. Пути передачи: контактнобытовой (новорожденные и дети первого года жизни), пищевой или водный (дети старшего возраста). При кишечных инфекциях, протекающих с бактериемией (например, брюшной тиф, кампилобактериоз), возможно внутриутробное инфицирование плода. Для кишечных инфекций характерна сезонность. Для большинства заболеваний бактериальной природы характерен летнеосенний подъем заболеваемости, для вирусных диарей – осенне-зимний период года. Иммунитет после перенесенных кишечных инфекций, как правило, видоспецифический и нестойкий. Передача антител от матери к плоду не происходит и поэтому дети оказываются высоко восприимчивыми к кишечным инфекциям уже с периода новорожденности. В современной клинической практике используется классификация диарейных заболеваний ВОЗ, дополненная и адаптированная для практического врача. Согласно классификации по механизмам развития различают «инвазивные» (экссудативные), «секреторные» и «осмотические» диареи, разграничение которых имеет большое практическое значении (таблица 24) Таблица 24 Классификация острых кишечных инфекций по типу диареи ИНВАЗИВНЫЙ (экссудативная диарея) Топический диаг- Возбудители ноз Гастрит, энтерит, Шигеллы, сальмонеллы, эшерихии (энтерогастро-энтерит, патогенные, энтеро-инвазивные), иерсинии, колит, энтероКампилобактер, клостри-дии, клебсиеллы, синеколит, гастрогнойная палочка, стафилококк, энтеро-бактер, проэнтероколит тей и другие условно-патогенные микроорганизмы. Дистальный колит Шигеллы, сальмонеллы , энтероинвазивные эшерихии, некротоксин продуцирующие штаммы: кло- 117 3 Клинические синдромы Синдром нейро-токсикоза (токсическая энцефалопатия). Синдром дегидратации (токсикоз с эксикозом). Инфекционнотоксический шок. Токсико-септический или токсико- стридий, кампилобактера, протея, дистрофический синдром синегнойной палочки «Гемоколит» Энтерогеморрагические эшерихии и Шига-токсин Гемолитико- уремический продуцирующие штаммы синдром (Гассера) шигелл, сальмонелл, иерсиний и др. СЕКРЕТОРНЫЙ ("водянистая» диарея без явлений метеоризма) Энтерит, гастроэн- Холерные (Эль-Тор, Бенгал), галофильные, НАГСиндром дегидратации терит вибрионы , энтеротоксигенные штаммы: эшерихий (токсикоз с эксикозом) (ЭТЭ), клебсиелл пневмо-ния, клостридий, кампилобактера, сальмонелл, иерсиний, стафилококка, протея, синегнойной палочки ОСМОТИЧЕСКАЯ(«водянистая» диарея с явлениями метеоризма) Энтерит, гастроэн- Ротавирусы, астро-, калици-, торо- и вирусы группы Синдром дегидратации терит Норфолка, респираторно-кишечные : корона-, адено- (токсикоз с эксикозом) и реовирусы СМЕШАННЫЙ ТИП (инвазивно-секреторный, инвазивно-осмотический) Возможно пораже- Бактериально-бактериальная или вирусноВозможно развитие люние любого отдела бактериальная микст-инфекция бого клинического кишечника синдрома При развитии «Инвазивного» типа диареи происходит адгезия микроорганизмов на поверхности энтероцитов с последующей инвазией возбудителя в клетки, а также в кровяное русло, развитие воспалительного процесса. Продукты жизнедеятельности бактерий, токсины приводят к транссудации через кишечную стенку белков, форменных элементов крови, потери ферментов и иммуноглобулинов, нарушается процесс расщепления углеводов, что способствует повышению осмолярности в просвете кишечника, нарушению всасывания воды и электролитов. Происходит усиление перистальтики и быстрое продвижение химуса. Наличие эрозивного или язвеннонекротического процесса в кишечнике с повышением чувствительности рецепторов и паретическим состоянием сфинктеров прямой кишки при дистальных колитах. «Осмотический» тип диареи возникает в результате проникновения в кишечник вирусов, которые проникая в энтероциты реплицируются и нарушают функцию клетки, кроме того повреждается щеточная кайма ворсинок и пристеночный слой слизи тонкой кишки. Развивается нарушение пристеночного и полостного пищеварения в тонком кишечнике, снижается выработка дисахаридаз (главным образом лактазы), что приводит к накоплению избыточного количества негидролизированных углеводов), а также специализированных белков переносчиков, с помощью которых осуществляется транспорт продуктов гидролиза пищевых субстратов (моносахаридов, аминокислот) из просвета кишки. Оставшиеся в просвете (невсосавшиеся) вещества с высокой осмотической активностью являются причиной нарушения реабсорбции воды и электролитов и развития водянистой диареи. Поступая в толстую кишку, эти вещества становятся субстратами для ферментации кишечной микрофлоры с образованием большого количества органических кислот, газообразного водорода, углекислого газа, метана и воды. Результатом являются повышенное газообразование в кишечнике (метеоризм) и снижение рН кишечного содержимого, поэтому синдром осмотической диареи у маленьких детей проявляется вздутием и болями в животе (коликами), появлением пенистого стула, отхождением газов. «Секреторные» диареи возникают в результате патогенного действия микробов с колонизацией микроворсинок слизистой эпителия кишки без их повреждения и без развития воспаления. Следствием такого типа взаимодействия возбудителей с кишечным эпителием являются процессы гиперсекреции, обусловленной ростом активности аденилатциклазы, повышением концентрации циклической АМФ в энтероцитах с усилением секреции воды в просвет кишечника. Отмечается снижение процессов реабсорбции жидкости при гиперпродукции кишечных гормонов, что усугубляет водно-электролитные и обменные нарушения. Снижение объема циркулирующей крови сопровождается гипоксией, метаболическим ацидозом, обменными расстройствами (в том числе аминокислотного баланса). Критериями тяжести при кишечных инфекциях являются степень проявлений общетоксического синдрома (вялость, слабость, температурная реакция и др.) и выраженность поражения различных отделов желудочно-кишечного тракта (боли в животе, рвота, кратность стула, его характер, наличие патологических примесей и др.). Выделяют легкие, среднетяжелые и тяжелые формы кишечных инфекций. Легкая форма ОКИ характеризуется умеренно выраженными проявлениями интоксикации (температура тела не выше 38- 38,5, снижение аппетита, недомогание, рвота однократно или вообще отсутствует) и диарейного синдрома (частота сту- 118 3 ла не превышает стул 6-8 раз в сутки). Среднетяжелая форма болезни проявляется выраженной интоксикацией (температура тела 38,5-390, головная боль, вялость и др.) и выраженным местным синдромом (рвота повторная, боли в животе, метеоризм, стул 10-12 раз, потери воды со стулом могут привести к появлению признаков обезвоживания – жажда, сухость языка и др.). Тяжелая форма ОКИ развивается преимущественно у детей раннего возраста из «группы риска», со сниженным иммунитетом. Характеризуется выраженным местным синдромом (стул «без счета», с большим количеством воды или других патологических примесей – слизи, зелени, гноя, крови), развитием целого ряда тяжелых синдромов (эксикоз II-III степени, гиповолемический шок, первичный токсикоз I-II-III степени, ИТШ I-II-III степени, гемолитико-уремический синдром, острая почечная недостаточность), своевременная диагностика которых очень важна для выбора адекватной тактики в отделениях реанимации и интенсивной терапии. Стертые ОКИ имеют минимальные клинические проявления со стороны ЖКТ (стул 3-4 раза в сутки, практически без воды и примесей) при отсутствии симптомов интоксикации и нарушения самочувствия. При субклинических формах – клинические проявления заболевания вообще отсутствуют. Выявляются эти атипичные формы обычно в очаге инфекции при целенаправленном обследовании контактных. Течение кишечных инфекций может быть острым (до 1 мес.), затяжным (до 3 мес), хроническое (свыше 3-х мес). Шигеллез. Инкубационный период колеблется от нескольких часов (пищевой путь) до 7 дней (контактно-бытовой путь), чаще составляет 2-3 дня. У детей старше года выделяют два клинических варианта манифестных форм шигеллеза. Колитический вариант, наиболее типичный, характеризуется острым началом с повышением температуры до фебрильных цифр, которая держится 3-5 дней. В течение первых суток заболевания может быть одно- или двукратная рвота, которая в последующие сутки обычно не повторяется. Ребенок становится беспокойным, вялым, отказывается от еды, плохо спит, жалуется на головную боль (при тяжелых формах могут иметь место явления менингизма, расстройство гемодинамики). Через несколько часов от начала заболевания появляются боли в животе, чаще схваткообразного характера без четкой локализации или в левой подвздошной области. Стул учащается, становится жидким, появляются патологические примеси в виде мутной слизи, зелени, а иногда и крови. В начале заболевания стул имеет каловый характер, к концу суток, чаще на 2 день болезни он становится скудным, теряет каловый характер и запах, приобретает вид "ректального плевка" – комочек мутной слизи (нередко гноя) с прожилками (или примесью) крови. В этот период болезни появляются характерные для шигеллезов тенезмы - тянущие боли в животе. Иногда позывы могут быть ложными. Отмечается податливость ануса с явлениями сфинктерита, реже – зияние ануса. Возможно развитие выпадения слизистой оболочки прямой кишки. При глубокой пальпации прощупывается болезненная или чувствительная сигмовидная кишка в виде уплотненного тяжа за счет ее спазма и инфильтрации. Гастроэнтероколитный вариант начинается с многократной, иногда неукротимой рвоты, лихорадки, сопровождающейся резкой головной болью, иногда явлениями менингизма, судорогами. Позже может развиться эксикоз I-II степени. Кишечная дисфункция появляется спустя несколько часов, стул имеет вначале энтеритный характер, лишь к концу первых, началу вторых суток - развивается типичный для дизентерии синдром дистального колита. Тяжелые формы заболевания протекают с развитием геморрагического колита. У детей первого года жизни возможно подострое начало болезни; чаще синдром энтероколита и энтерита редкость «колитической» формы болезни. Эквивалентами синдрома дистального колита являются беспокойство, натуживание ребенка во время дефекации, сучение ножками и покраснение лица; тяжесть болезни обусловлена нарушениями гемодинамики, водно-минерального и белкового обмена; К специфическим осложнениям шигеллеза относят инфекционно – токсический шок, острую почечную недостаточность, гемолитико – уремический синдром, выпадение слизистой прямой кишки, динамическую кишечную непроходимость, кишечное кровотечение, реактивный панкреатит, инвагинацию, трещины и эрозии заднего прохода, аппендицит, дисбактериоз кишечника. Такие специфические осложнения как прободение кишечника и развитие перитонита у детей практически не встречаются. Среди неспецифических осложнений, особенно у детей раннего возраста, встречаются отиты, бронхиты и пневмония (чаще как осложнения наслоившейся ОРВИ), инфекция мочевыводящих путей. Лабораторное подтверждение дизентерии осуществляется бактериологическим методом (выделение шигелл из испражнений) и серологическим (РПГА с эритроцитарным диагностикумом). Диагностически значимыми являются рост титров антител в 4 и более раз ко 2-й неделе заболевания, а также появление антител в диагностических титрах (1 : 200 и выше у детей старше года и 1 : 100 и выше - у больных до года). Экспресс – методы диагностики являются информативными и высокоспецифичными. Используют 119 3 иммунофлюоресцентный, иммуноферментный анализ, реакцию угольной агломерации, О – агрегатгемагглютинационную пробу, РСК, ПЦР и др. Сальмонеллезы. Источником инфекции являются животные и человек. Пути передачи: пищевой, контактно – бытовой, реже водный. Инкубационный период продолжается от нескольких часов до 5 – 8 суток. Типичная желудочно – кишечная форма встречается наиболее часто. Заболевание начинается остро с повышения температуры тела, развития симптомов интоксикации и кишечной дисфункции. Гастрит наблюдается чаще у детей старшего возраста. Заболевание начинается остро появляются многократная рвота, боли в животе, повышается температура тела. Одновременно нарастают слабость, головная боль, снижается аппетит. Живот вздут, болезненный в эпигастральной области. Стул не изменяется. Энтерит начинается постепенно с периодически возникающего беспокойства, снижения аппетита. Температура тела субфебрильная. Стул жидкий, пенистый, обильный до 5 – 10 раз в сутки. Отмечаются признаки токсикоза с эксикозом. Гастроэнтерит характеризуется длительной лихорадкой, выраженными симптомами интоксикации, учащением стула до 3 – 8 раз в сутки, рвотой. Стул жидкий, обильный, водянистый, пенистый с примесью слизи и зелени. У большинства больных развивается обезвоживание I – II степени. С первых дней болезни язык сухой, обложен белым налетом, живот вздут, отмечаются урчание, шум плеска по ходу кишечника. У части больных в начальном периоде преобладает нейротоксикоз. В ряде случаев развивается инфекционно – токсический шок. Энтероколит и гастроэнтероколит развиваются остро: температура тела повышается до 38,5 – 39,5° и сохраняется на этом уровне в течение 5 – 7 суток с периодическими повышениями и снижениями. У больных с гастроэнтероколитной формой сальмонеллеза отмечается рвота – нечастая (2 – 3 раза в сутки), но упорная, сохраняющаяся, как правило, в течение всего острого периода. С первых дней болезни стул частый, обильный, с неприятным запахом, темно – зеленого цвета (в виде «болотной тины»), с большим количеством слизи и прожилками крови. Живот вздут, при пальпации определяется разлитая болезненность, часто боли локализуются вокруг пупка и по ходу толстой кишки. Увеличиваются размеры печение и селезенки. Симптомы интоксикации достигают максимума к 3 – 5 м суткам. У половины больных наблюдаются признаки обезвоживания I – III степени. Характерны торпидное течение, продолжительная дисфункция кишечника, длительное бактериовыделение. Колит (дизентериеподобная форма) начинается остро, с повышения температуры тела, появления учащенного, жидкого, содержащего каловые массы стула. Сходство с дизентерией заключается в наличии примеси слизи, иногда и крови в испражнениях. Однако тенезмов и зияния ануса не наблюдается. В анализе крови в острый период отмечаются лейкоцитоз, нейтрофилез с палочкоядерным сдвигом, повышенная СОЭ. Тифоподобная форма встречается редко, преимущественно у детей школьного возраста и подростков, по клиническим проявлениям напоминает тифо-паратифозные заболевания. Септическая форма возникает чаще у новорожденных и детей раннего возраста с отягощенным преморбидным фоном. Осложнения могут быть специфического (инфекционно-токсический шок, ДВС – синдром, гемолитико-уремический синдром, миокардит, дисбактериоз кишечника) и неспецифического характера (бронхиты, пневмонии, отиты, синуситы и др.). Для диагностики используют бактериологический метод (выделение бактерий в испражнениях, рвотных массах, промывных водах желудка, крови, моче, ликворе, слизи из зева и носа). Для серологического исследования используют РНГА с эритроцитарным диагностикумом и цистеиновую пробу (на 5–7-е и 12– 15– е сутки болезни). Диагностическими титрами при определении суммарных антител в РНГА являются – 1:100 (у детей до 1 года) и 1:200 (старше 1 года). Эшерихиозы. Эшерихии подразделятся на несколько подгрупп: энтропатогенные (ЭПЭ), энтротоксигенные (ЭТЭ), энтероинвазивные (ЭИЭ), энтерогеморрагические (ЭГЭ); энтероагрегативные (энтеровыстилающие) (ЭАЭ) и диффузно-прикрепляющиеся (ДПЭ) . Чаще всего в педиатрической практике встречаются эшерихиозы, вызванные первыми тремя группами бактерий. ЭПЭ вызывают заболевание у детей в возрасте от 3 мес. до 1 года с отягощенным преморбидным фоном, находящиеся на искусственном вскармливании. Инкубационный период в среднем составляет 4-8 суток. Заболевание начинается с дисфункции кишечника по типу энтерита или гастроэнтерита, повышения температуры тела, нарушения общего состояния, появляются срыгивания или рвота (упорная, но нечастая – 2 – 3 раза в сутки). Стул имеет характер «водянистой диареи» - обильный, брызжущий, иногда смачивает всю пеленку, желтого цвета или бесцветный, с умеренным количеством слизи, перемешанной с калом и водой. Частота стула обычно нарастает к 5-7 дню болезни. Характерно развитие токсикоза с эксикозом, развитие осложнений (отит, анемия, гипотрофия, дисбактериоз кишечника, вторичный синдром мальабсорбции). У детей старше 3-х лет и взрослых развиваются эшерихиозы, вызванные ЭИЭ. Инкубационный период колеблется от нескольких часов до 1-3 суток. Заболева- 120 3 ние начинается остро с повышения температуры тела, головной боли, слабости, схваткообразных болей в животе, однократной рвоты. Одновременно или через несколько часов от начала заболевания возникает дисфункция кишечника по типу энтероколита – жидкий стул калового характера до 4-8 раз в сутки с примесью мутной слизи, иногда зелени и прожилок крови. Тенезмов и стула в виде «ректального плевка» не наблюдается. Энтеротоксигенными эшерихиозами чаще болеют дети в возрасте от 1 до 3 лет. Инкубационный период продолжается от нескольких часов до 3 суток. Заболевание, как правило, протекает по типу холероподобного гастроэнтерита. Отмечаются многократная рвота, частый (до 10-15 раз в сутки) водянистый брызжущий стул без патологических примесей, приступообразные боли в животе. Температура тела нормальная, дефекация безболезненная. У части больных развиваются явления токсикоза с эксикозом. Энтеротоксигенный эшерихиоз протекает доброкачественно, нормализация стула происходит на 4-6 сутки, выздоровление – на 7-10 сутки. Однако, у детей раннего возраста возможно развитие тяжелых форма заболевания, даже с летальным исходом. Ротавирусная инфекция одна из наиболее распространенных кишечных инфекций у детей. Инкубационный период короткий и длится от 15 часов до 1 – 3 дней. Заболевание начинается с одновременного появления повышенной температуры, интоксикации, диареи и рвоты. С первого дня болезни, чаще до проявлений рвоты и диареи, появляются симптомы катарального поражения верхних дыхательных путей, такие как гиперемия зева, слизистые выделения из носа, покашливание. Температура тела повышается до фебрильных цифр. Рвота предшествует жидкому стулу либо появляется одновременно с ним. Она может быть от 2 до 10-12 раз. С первых дней, либо через 1-2 дня от начала заболевания, появляется обильный кашицеобразный, но чаще водянистый стул желтоватой или белесовато-серой окраски, со зловонным кислым запахом, пенистый, без патологических примесей. Позывы к дефекации возникают внезапно, сопровождаются урчанием кишечника и болью в животе. При осмотре больного обращает на себя внимание выраженная бледность кожных покровов, появление «мраморного рисунка» кожи у детей первого года жизни, сухой обложенный язык, разлитая умеренная гиперемия ротоглотки, повторная рвота, как правило связанная с приемом пищи или воды. Тоны сердца приглушены, систолический шум на верхушке сердца. Вздутие живота и урчание при пальпации по ходу тонкого кишечника. Боли в эпигастрии или по всему животу без четкой локализации, умеренно выраженные или схваткообразные, сопровождающиеся урчанием в животе. На фоне многократного водянистого стула и рвоты развивается эксикоз II-III степени, гемодинамические нарушения. Дегидратация, дисбаланс электролитов, нарушение микроциркуляции обуславливают развитие метаболического ацидоза. Выделение вируса является основополагающим в лабораторной диагностике ротавирусной инфекции. Материалом для вирусологических исследований служат фекалии больных. С наибольшим постоянством вирус обнаруживают в фекалиях в первые 2-3 дня болезни. Наиболее широко применяемые методы – ИФА, РНГА и РЛА. Возможно обнаружение вирусных частиц с помощью электронной микроскопии (ЭМ), иммунноэлектронной микроскопии (ИЭМ), метода коагглютинации, иммуноцитохимической детекции ротавируса, иммунофлюоресценции, ПЦР. Эксикоз. Одним из наиболее частых и тяжелых осложнений кишечных инфекций у детей является обезвоживание (эксикоз). Выделяют изотонический, соледефицитный (гипотонический) и вододефицитный (гипертонический) типы обезвоживания. Изотонический тип характеризуется пропорциональной потерей солей и воды. Клинически выражается вялостью, слабостью, сонливостью ребенка. Кожа и слизистые оболочки сухие, тургор тканей снижен, диурез уменьшен. Уровень электролитов в крови нормальный, сгущение крови. Соледефицитный тип обычно развивается при длительном поносе, неадекватной инфузионной терапии. Клинически отмечается тяжелое состояние: вялость, адинамия, заторможенность, повторная рвота, вздутие живота, кожа холодная, бледная с мраморным рисунком, тонус мышц снижен, диурез уменьшен, артериальное давление низкое, тоны сердца приглушены, дыхание редкое. Уровень натрия и калия в крови снижен. Вододефицитный тип эксикоза проявляется выраженной жаждой, беспокойством, возбуждением. Кожа и слизистые оболочки сухие, тонус мышц умеренно снижен, дыхание учащено, диурез незначительно уменьшен. Уровень электролитов в крови повышен, небольшое сгущение крови. Также эксикоз разделяется по степени тяжести. Таблица 24 Оценка степени тяжести обезвоживания у детей с острыми кишечными инфекциями Признак Степень обезвоживания при острой потере массы тела До 5% (1 степень) 5-10% (2 степень) Более 10% (3 степень) Стул 3-5 раз в сутки До 10 раз в сутки Частый, без счета 121 3 Рвота Общее состояние Жажда Тургор тканей Редкая Средней тяжести Умеренная Сохранен Повторная Тяжелое Резко выраженная Снижен Слизистые оболочки Влажные Большой родничок Глазные яблоки Цианоз Тоны сердца Ритм сердца Нормальный Нормальные Отсутствует Громкие Нормальный Суховаты, слегка гиперемированы Слегка запавший Мягкие Умеренный Приглушены Умеренная тахикардия Многократная Очень тяжелое Может отсутствовать Кожная складка не расправляется Сухие, яркие Втянут Западают Резко выражен Глухие Выраженная тахикардия Артериальное дав- Нормальное или Диастолическое повы- Снижено ление слегка повышено шено ЦВД Нормальное Снижено Отрицательное Сознание Нормальное Возбуждение или сон- Нарушено ливость, вялость Реакция на боль Выражена Ослаблена Отсутствует Голос Нормальный Ослаблен Часто афония Конечности Теплые Холодные Очень холодные Температура тела Нормальная Часто повышена Часто снижена Диурез Сохранен Снижен Значительно снижен (менее 10мл/кг) Дыхание Нормальное Умеренная одышка Пародоксальное РН Норма 7,3 и ниже Резко снижено ВЕ Норма До -10 Ниже –20 Основные принципы терапии острых кишечных инфекций у детей Комплексное лечение ОКИ включает: лечебное питание, этиотропную терапию, патогенетическую (регидратационную) и симптоматическую терапию, а также ферментотерапию, коррекцию дисбиотических нарушений в кишечнике и иммунотерапию. Диетотерапия. Дети раннего возраста, находящиеся на естественном вскармливании должны получать грудное молоко. При искусственном вскармливании вид заменителя грудного молока зависит от типа диареи. При инвазивных и секреторных диареях рекомендуется использование адаптированных молочных смесей, обогащенных пробиотиками (НАН1, НАН2, Нутрилак Бифи, Бифидус и т.д), кисломолочных смесей («Нутрилон-низколактозный», «НАН-безлактозный», «Мамекс безлактозный»), при отсутствии атопического дерматита, пищевой аллергии и риска развития аллергических заболеваний можно рекомендовать смеси на основе соевого белка («Фрисосой»,Нутрилак Соя, Нутрилон Соя, Хумана СЛ и др) при тяжелом течении заболевание показаны смеси с частичным или полным гидролизом белка (НАН ГА, Нутрилак ГА, Фрисолак ГА, Алфаре, Нутрилон Пепти ТСЦ, Фрисопеп, Прегистимил и др). При осмотических диареях необходимо перевести ребенка на низколактозные и безлактозные смеси (НАН безлактозный, Нутрилак безлактозный, Энфамил лактофри), при грудном вскармливании добавить ферменты (Лактазим, Ти-лактаза). Объем питания зависит от степени тяжести заболевания: при легких степенях уменьшается на 15-20%, при среднетяжелой – на 2030%, при тяжелой: на 30-50%. кратность кормления также зависит от тяжести состояния и составляет от 6 до 10 раз в сутки с уменьшением разового объема. Недостающий объем питания восполняется за счет жидкости энтерально или парентерально. Детям старше года из питания исключают продукты усиливающие перистальтику кишечника (ржаной хлеб, сухари из ржаного хлеба, сдобные, хлебобулочные и кондитерские изделия, цельное молоко, йогурт, ряженка, сливки, каши на цельном молоке, бобовые, свекла, огурцы, квашеная капуста, овощи и фрукты без термической обработки, ягоды, виноград, крепкие мясные и рыбные бульона, жирные сорта мяса и рыбы, соленья, маринады). В острые период разрешается отварной рис, печеные яблоки, сухари из белого хлеба, бананы. При уменьшении проявлений кишечной дисфункции вводятся мясные суфле из курицы, кролика, говядины, картофельное пюре на воде, овощные супы, кисели, компоты из яблок и изюма, безмолочные каши, галетное не сдобное печенье. Регидратационная терапия. Основным патогенетическим методом лечения ОКИ является восполнение потерянной жидкости. При экси- 122 3 козе I и II степени используется метод оральной регидратации. При секреторной диарее препаратами выбора является Редирон и Глюкосолан (Цитроглюкосолан) характеризующиеся высоким содержанием солей и высокой осмолярностью. При осмотической и инвазивной диарее показаны гипосомолярные растворы – Гастролит и ORS-200. Пероральная регидратация при наличии обезвоживания I-II степени проводится в два этапа. I этап – в первые 6 часов от начала лечения проводится ликвидация водно-солевого дефицита, имеющего место к началу лечения. Таблица 25 Расчет количества жидкости для оральной регидратации Масса тела, кг Количество раствора в мл 1 степень эксикоза 2 степень эксикоза за 1 час за 6 часов за 1 час за 6 часов 5 42 250 66 400 10 83 500 133 800 15 125 750 200 1200 20 167 1000 266 1600 25 208 1250 333 2000 30 249 1500 400 2400 40 332 2000 530 3200 II этап – поддерживающая терапия, которая проводится в зависимости от продолжающихся потерь жидкости и солей со рвотой и испражнениями. Ориентировочный объем раствора для поддерживающей регидратации в последующие 18 часов первых суток оральной регидратации равен 80 100 мл/кг массы тела в сутки. Второй этап регидратации продолжается до прекращения диареи. Регидрон и другие солевые растворы можно сочетать с введением бессолевых растворов (чай, вода, отвар изюма и кураги без сахара, отвар шиповника, каротиновая смесь) в соотношении: 1:1 – при выраженной водянистой диарее; 2:1 – при потере жидкости, преимущественно с рвотой; 1:2– при потере с перспирацией (при гипертермии и умерено выраженном диарейном синдроме); при синдроме энтероколита при инвазивных ОКИ. Солевые и бессолевые растворы чередуется, но не смешиваются друг с другом. Показания к парентеральной регидратации: тяжелые формы обезвоживания (II и II-III степень) с признаками гиповолемического шока; инфекционно-токсический шок; сочетание эксикоза (любой степени) с тяжелой интоксикацией; олигоурия и анурия, не исчезающая в ходе первого этапа регидратации; неукротимая рвота; нарастание объема стула во время проведения пероральной регидратации в течение первых 2-х дней лечения; неэффективность пероральной регидратации в течение суток. Лечение больного проводится в отделении или палате интенсивной терапии с ежечасным мониторингом ЧСС, АД, количества введенной и потерянной жидкости. Объем вводимой внутривенной жидкости в первый день составляет 120 –180 мл/кг/сут и зависит от степени потери жидкости. После ликвидации обезвоживания объем инфузии уменьшается, но расширяется объем оральной регидратации. Состав водно-солевых растворов рассчитывают в зависимости от типа эксикоза. При изотоническом типе применяют солевые растворы (раствор Рингера, Лактосоль, Квартосоль и др.) и 10% раствор глюкозы в соотношении 1:1, при соледефицитном типе –2:1 и 3:1, при вододефицитном типе –1:2, 1:3. При наличии признаков гиповолемического шока в первый час лечения внутривенно вводятся коллоидные растворы (реополиглюкин, гемодез, альбумин) в объеме до 1/3 от общего объема инфузии, а также вводят глюкокортикоиды (преднизолон) из расчета 2-3 мг/кг внутривенно, антигистаминные препараты, сердечно-сосудистые средства. Этиотропная терапия кишечных инфекций зависит от патогенетических механизмов, лежащих в основе развития ОКИ, предполагаемой на основании клинико-эпидемиологических данных этиологии болезни, тяжести и фазы заболевания, возраста больных, сопутствующей патологии, особенностей иммунной реактивности организма. Антибиотики и химиопрепараты показаны: больным с инвазивными диареями в острой фазе болезни и при клинически выраженном обострении (рецидиве); при тяжелых формах ОКИ (независимо от этиологии и возраста); при среднетяжелых формах болезни детям до 2 лет, при шигеллезах - независимо от возраста, при явлениях геморрагического колита; при легких формах болезни детям до года «группы риска», при явлениях геморрагического колита; больным холерой, брюшным тифом и амебной дизентерией – не зависимо от возраста больного и тяжести болезни; больным любого возраста с генерализованными формами ОКИ. Препараты I ряда («стартовые») - эрцефурил, фуразолидон, макмирор, цефуросим, цефиксим или рифаксимин. Препараты II ряда («альтернативные») - обычно назначаются в стационаре при неэффективности препаратов 1 ряда, при среднетяжелых и тяжелых формах болезни, а также 123 3 в случае поступления в поздние сроки - амоксициллин/клавулановая кислота (детям первых месяцев жизни), препараты налидиксовой кислоты, аминогликозиды II поколения внутрь, по показаниям – в сочетании с парентеральным их введением; макролиды II поколения. Препараты III ряда («резерва») рекомендуются применять только в стационарных условиях : при тяжелых и генерализованных формах ОКИ детям «группы риска» - как стартовые; при среднетяжелых и тяжелых формах болезни – в случае неэффективности препаратов II ряда. Назначаются рифампицин, альфа нормикс (рифаксимин), цефалоспорины III-IY поколения (цефтибутен, цефтазидим и др.), фторхинолоны (ципрофлоксацин, норфлоксацин, офлоксацин - детям старше 12 лет, до 12 лет - только по витальным показаниям), карбапенемы (имипенем/циластатин, меропенем). При наличии клинического эффекта в острой фазе заболевания рекомендуются курсы лечения 5-7 дней. Клиническая неэффективность препарата в течение первых 3 дней является основанием для смены антибиотика или химиопрепарата. Иммунотерапия. Используют КИП (комплексный иммуноглобулиновый препарат), который содержит иммуноглобулины трех основных классов – IgG (50%), IgM (25%), IgA(25%) и характеризуется повышенной концентрацией антител к энтеробактериям (шигеллы Зонне, сальмонеллы, эшерихии), ротавирусам, а также к другим грамотрицательным микроорганизмам (псевдомонады, стафилококки, клебсиеллы и др.). Также применяют рекомбинантные интерфероны – Виферон - комбинированный препарат, выпускаемый в свечах. В его состав входят человеческий рекомбинантный α-итерферон, мембраностабилизирующие препараты и основа (масло какао). Доказана эффективность комбинированного препарата Кипферон, содержащего КИП и гамма-интерфероны. Энтеросорбенты. Показано назначение при появлении первых симптомов. Препаратом выбора является неосмектит (Смекта), который обладает этиотропным действием (абсорбция вирусных частиц и бактериальных токсинов), патогенетическим (дезинтоксикационный, антипиретический, антидиарейный) и при вирусных диареях мукопротективным эффектом. Также возможно назначение энтеросгеля и лактофильтрума. Пробиотики. Препараты содержащие пробиотические культуры оказывают этиотропное действие за счет механизмов микробного антагонизма, кроме того способствуют нормализации процессов пищеварения, кишечной моторики, выработки витаминов, секреторных иммуноглобулинов, эндогенного интерферона, повышения всасывания воды и электролитов (патогенетическое действие). Назначают препараты бифиформ, Нормобакт, Линекс, Йогулакт и т. д. Ферментотерапия. Заместительную ферментотерапию при ОКИ у детей следует проводить при наличии клинических и копрологических признаков нарушенного пищеварения с целью коррекции переваривающей и всасывательной функции ЖКТ. Препараты выбирают в зависимости от типа диареи: при «инвазивных» диареях препаратом выбора является панкреатин или его аналоги с низкой активностью панкреатических ферментов (мезим форте, пангрол 400 и др.). При гастритах показано назначение протеолитических ферментов (абомин и др.), гастроэнтеритах - ферментов на основе панкреатина, при колитах -ферменты с высокой амилолитической активностью (панцитрат, панзинорм); при «осмотическом типе» диареи следует назначать ферменты с высокой амилотической активностью (лактаза, ти-лактаза, ораза, сомилаза, панцитрат, пангрол 400, юниэнзим и др.). Также назначается симптоматическая терапия (жаропонижающие препараты, витаминотерапия и т. д.). Диспансерное наблюдение за детьми, перенесшими шигеллез и сальмонеллез. Дети в возрасте до 2 лет, находящиеся в домах ребенка, психоневрологических домах ребенка, школах – интернатах, других закрытых детских учреждениях после перенесенного шигеллеза и сальмонеллеза подлежат диспансерному наблюдению в течение 6 месяцев. В течение 1-го месяца клинико – бактериологическое обследование проводят двухкратно с 2-недельным интервалом, в дальнейшем – 1 раз в месяц. Дети старше 2 лет, а также школьники, переболевшие шигеллезом Флекснера 2а, подлежат диспансерному наблюдению в течение 3 месяцев с ежемесячным клиническим и бактериологическим обследованием. Школьники после перенесенного шигеллеза (за исключением шигеллеза Флекснера 2а) наблюдаются в течение 1 месяца после выздоровления. Бактериологическое обследование проводят дважды с интервалом 2-3 дня. Диспансерное наблюдение за реконвалесцентами хронической формы шигеллеза и больных с затяжным и хроническим течением сальмонеллеза всех возрастных групп осуществляют в течение 6 месяцев с ежемесячным однократным бактериологическим и копрологическим обследованием. Критериями клинического выздоровления являются: полное восстановление сна, аппетита, эмоционального статуса, обязательная прибавка массы тела, а также – стойкая нормализация температуры, стула, гемограммы, копроцитограммы. В связи с тем, что санация от возбудителя, полная репарация слизистой кишечника и восстановление его нарушенных функций наступают 124 3 значительно позднее, чем исчезают клинические проявления болезни, дети, получавшие стационарное лечение, нуждаются в наблюдении участкового врача и проведении необходимого обследования и долечивания в амбулаторных условиях. Профилактика острых кишечных инфекций. Основой профилактики ОКИ является соблюдение правил личной гигиены, гигиены питания и водоснабжения. Необходимо соблюдение санитарного режима в детских учреждениях. Изоляция больного осуществляется на дому, в тяжелых случаях проводится госпитализация. В очагах инфекции проводится дезинфекция, осуществляется ежедневный контроль температуры тела и характера стула у лиц, контактировавших с больным. 125 3 Таблица 26 Лечение кишечных инфекций у детей Легкая форма Среднетяжелая форма Вирусные инфекции безлактозные смеси или грудное молоко с препаратами лактазы, ферменты в возрастной дозировке 7-10 дней; пробиотики в возрастной дозировке в течение 14дней; энтросорбенты (Смекта по 1/2 -1 пакетику 3 раза в день, Энтеросгель: детям до 2-х лет по 20 мл 3 раза в день, 3-7 лет по 40 мл 3 раза в день, 7-12 лет по 60 мл 3 раза в день, старше 12 лет по 80 мл 3 раза в день разведенного в воде препарата; Лактофильтрум в дозе: детям с 6 мес до 1 года – по 1/3 таблетки 3 раза в день, с 1 года до 3лет – ½ таблетки 3 раза в день, от 3 до 7 лет – по 1 таблетке 3 раза в день, с 7 до 12 лет – по 1-2 таблетке 3 раза в день, старше 12 лет – 23 таблетки 3 раза в день.) по 3-4 дня безлактозная диета регидратация в зависимости от степени эксикоза (оральная гипоосмолярными растворами или инфузионная глкозо-солевыми растворами 2:1 до купирования эксикоза – 2-4 дня); этиотропные препараты (антиротавирусный иммуноглобулин АРИГ по 3 мл КИП по 1-2 дозы 1-2 раза в день, разведенный в воде или кипферон суппозитории по 1 суппозиторию 1 раз в день , с 1 года до 3-х лет 2 раза в день, старше 3-х лет по 1 суппозиторию 3 раза в день в течение 3 дней или циклоферон 3 дня); энтеросорбенты 5-7 дней; ферменты (10-14 дней); пробиотики в возрастной дозировке (10-14 дней) Тяжелая форма безлактозная диета (при развитии тяжелой мальабсорбции перевод на частичное парентеральное питание + гидролизаты белка); инфузионная глюкозо-солевыми растворами 1:1 и коллоидами в течение 3-5 дней; этиотропные препараты (КИП 5-10 дней или циклоферон 5-7 дней или кипферон 5-7 дней); энтеросорбенты 7-10 дней; ферменты (10-14 дней); пробиотики (10-14 дней) Антибактериальные препараты по показаниям: Перорально: нитрофураны (эрцефурил – до 2,5 лет по 100 мг 2-3 раза в сутки, старше 2,5 лет по 200 мг 3 раза в сутки; фуразолидон по 8-10 мг/кг/сут; макмирор 10-20 мг/кг/сут) или цефалоспорины 2-3 поколения (цефуросим (Зиннат) по 30 мг/кг/сут или цефиксим (Супракс) – 8 мг/кг/сут или рифаксимин (Альфа-нормикс) детям старше 12 лет по 600 мг каждые 8 часов) Парентерально: цефалоспорины 2-3 поколения (цефуроксим (Зинацеф) 50-10 мг/кг/сут или цефаксим (клафоран) 50-100 мг/кг/сут и т.д.) или фторхинолоны (детям старше 12 лет) – ципрофлоксацин 10 мг/кг/сут или карбопенемы Бактериальные инфекции диета; энтеросорбенты 3 дня; ферменты 7-10 дней; пробиотики 7-10 дней. При наличии отягощенного преморбидного фона подключить нитрофураны или рифаксимин детям старше 12 лет диета; регидратация (оральная или инфузионная терапия в зависимости от степени эксикоза до его купирования; энтеросорбенты 5-7 дней; пробиотики 10-14 дней; ферменты 10-14 дней; этиотропная терапия (нитрофураны или цефалоспоррины 2-3 поколения; КИП 126 3 диета; инфузионная терапия (регидратация и дезинтоксикация);энтеросорбенты 710 дней;пробиотики 1014 дней; ферменты 1014 дней; парентеральные и пероральные антибактериальные препараты: № п/п 1. 2. 3. 4. 5. 6. 7. 8. 9. 10. № п/п 1 2. Вопросы для тестового контроля Содержание вопросов Основной механизм инфицирования при кишечных инфекциях у детей является: а) воздушно-капельный, б) фекально-оральный, в) парентеральный Характер стула при сальмонеллезе: а) жидкий, скудный, много слизи, в виде «ректального плевка» б) жидкий, обильный, водянистый типа «рисового отвара» в) жидкий, с большим количеством слизи, зелени, типа «болотной тины» Локализация патологического процесса при энтероинвазивном эшерихиозе: а) желудок, б) тонкая кишка, в) толстая кишка, г) любой отдел ЖКТ Выраженная сезонность при ротавирусной инфекции: а) весенне-летняя, б) зимне-весенняя, в) осенне-зимняя Для патогенеза ротавирусной инфекции у детей раннего возраста характерно: а) развитие осмотической диарее, б) развитие инвазивной диареи, в) развитие секреторной диареи Чаще всего инвазивная диарея развивается при: а) вирусных инфекциях, б) холере, в) бактериальных инфекциях Холероподобное течение эшерихиоза вызывают: а)ЭПКП; б)ЭИКП; в)ЭТКП; г)все вышеперечисленные; д) данный характер течения не встречается при эшерихиозах При проведении оральной регидратации у ребенка с ротавирусной инфекцией препаратом выбора является: а) цитроглюкосолан, б) ORS-200, в) гастролит, г) регидрон, д) все вышеперечисленные Антибактериальные препараты для лечения кишечных инфекций у детей не назначаются: а) у детей первого года жизни «группы риска», б) у детей школьного возраста с легким течением шигеллеза, в) у детей дошкольного возраста при ротавирусной инфекции, г) у детей первых двух лет жизни При изотоническом эксикозе соотношение глюкозы и солевых растворов: а) 1:1; б) 1:2; в) 2:1; г) 3:1; д) глюкоза не вводится Эталоны ответов б б г б а в в б,в в а Ситуационные задачи: Содержание задач Эталоны ответов Ребенок 6 лет посещает детский сад. Заболел остро: повысилась температура тела до 39ºС, была повторная рвота и жидкий каловый стул с примесью слизи и зелени. На следующий день стул участился до 10 раз, появились болезненные позывы на дефекацию, стул приобрел слизистый характер с прожилками крови. При осмотре: состояние средней степени тяжести, температура тела 39,3ºС, вялый. Язык густо обложен белым налетом. Сухой. Дыхание везикулярное. Тоны сердца ясные, ритмичные. ЧСС 110 в мин. Живот втянут. При пальпации болезненность в левой подвздошной области, сигмовидная кишка спазмирована. Стул скудный с большим количеством слизи, прожилками крови. Мать ребенка здорова. Одновременно с ребенком в разных группах детского сада заболело еще несколько детей (высокая температура, головная боль, жидкий стул). Общий анализ крови: Hb –130 г/л, эр. – 3,5 1012 /л, Le10*109 /л, палоч. –10%, сегм. –55%, эоз. –4%,лимф. –28%, мон.-3%;СОЭ –22 мм/час. РНГА с сальмонеллезным диагностикумом – отриц. Вопросы: 1. Предварительный диагноз; 2. План обследования; 3. План лечения. Мальчик 12 лет заболел остро, появились резкие боли в эпигастральной области. Тошнота. Многократная рвота. Доставлен бригадой «Скорой помощи». В приемном отделении: состояние тяжелое, температура тела 38ºС, вялость, однократная рвота, принесшая облегчение. Кожные покровы бледные, слизистая полости рта сухая, язык густо 1.Дизентерия, острое течение, типичная форма, среднетяжелая. 2. Посев кала на бактериологическое исследование; РНГА с шигеллезными диагностикумами; билирубин и печеночные пробы 3. Диета –стол №4, оральная регидратация глюкозосолевыми растворами «Оралит», «Цитроглюкосолан»; антибактериальные препараты – фурозолидон или бисептол; ферментные препараты – мезим-форте, фестал; биопрепараты – бифидумбактерин, бификол. 127 3 1. Сальмонеллез, желудочнокишечная форма, средней степени тяжести. 2. Бактериоскопическое исследование фекалий, посев рвотных масс, крови. Исследование РА и РНГА 3. обложен белым налетом. Зев розовый чистый. Дыхание везикулярное, хрипов нет. ЧД 30 в мин. Тоны сердца приглушены. Пульс 100 в минуту, удовлетворительного наполнения. Живот слегка вздут, при пальпации болезненность в области пупка и эпигастрия. Печень и селезенка не увеличены. Сигмовидная кишка эластичная. Стул от начала заболевания был трехкратно, жидкий, обильный, зловонный, типа «болотной тины». Мочеиспускание не нарушено. Эпидемиологический анамнез – в семье 4 человека, здоровы. Мальчик употреблял в пищу пирожки с мясом, купленные во время экскурсии по городу с классом. Анализ крови общий: Hb –130 г/л, эр. – 3,6 1012 /л, Le12*109 /л, палоч. –10%, сегм. –60%, лимф. –28%, мон.2%;СОЭ –25 мм/час. Вопросы: 1.Предварительный диагноз; 2. Необходимые исследования; 3. Назначьте лечение. В приемный покой инфекционной больницы доставлен ребенок 10 месяцев. Жалобы на повышение температуры до 38,5ºС, появление частого водянистого стула, много кратную рвоту. Заболел 3 дня назад, симптомы развивались постепенно, ухудшение состояния 4 часа назад – ребенок стал вялым, отказывается от еды, воду не удерживает, стул без счета. При осмотре: состояние тяжелое, вялый. Воду пьет неохотно, рвота. Кожа бледная, с мраморным оттенком, акроцианоз, тургор кожи резко снижен, большой родничок запавший, слизистые оболочки сухие, яркорозового цвета. Тоны сердца приглушены, ЧСС 180 в мин. Живот увеличен в объеме, мягкий, при пальпации ребенок не беспокоится. Анус зияет, постоянное выделение водянистых желто-оранжевых каловых масс. Диурез снижен. Масса ребенка до заболевания 11 кг, в настоящее время 9800гр. Вопросы: 1. Предварительный диагноз; 2. План обследования; 3. Какое лечение необходимо назначить ребенку в первые сутки? с сальмонеллезным диагностикумом. 3. Водно-чайная пауза на 8 часов, затем диета –стол №4, оральная регидратация глюкозо-солевыми растворами «Оралит», «Цитроглюкосолан»; антибактериальные препараты – фурозазолидон или бисептол; ферментные препараты – мезим-форте, фестал; биопрепараты – бифидумбактерин, смекта. 1. Эшерихиозная инфекция, тяжелая форма. Токсикоз с эксикозом III степени. 2. Общий анализ крови, гематокрит, общий анализ мочи, анализ крови на КЩС, электролиты, бактериологические исследование фекалий, ЭКГ. 3. Лечение проводится в отделении интенсивной терапии. Внутривенно вводится жидкость из расчета 200 мл/кг, используют 10% глюкозу и "Лактосоль" в равных количествах. Назначается фуразолидон, мезим-форте, смекта, бифидумбактерин. Рекомендуемая литература: Основная: 1. Нисевич Н.И., Учайкин В.Ф. Инфекционные болезни у детей. - М.: "Медицина", 2008, -790 с. Дополнительная: 1. Инфекционные болезни у детей // Под редакцией В.В. Ивановой- М., Мед. Информационное агентство, 2002. 2. Инфекционные болезни у детей / Под редакцией профессора Э.Н. Симованьян Ростов на Дону: Феникс, 2007, - 766 с. – (Высшее образование). 128 3 Содержание Занятие № 1 - БРОНХИАЛЬНАЯ АСТМА 3 Занятие № 2 - ЛЕЙКОЗЫ 10 Занятие № 3 - РЕВМАТИЗМ. ПРИОБРЕТЕННЫЕ ПОРОКИ СЕРДЦА 18 Занятие № 4 - ЮВЕНИЛЬНЫЙ РЕВМАТОИДНЫЙ АРТРИТ 26 Занятие № 5 - НЕРЕВМАТИЧЕСКИЕ КАРДИТЫ 34 Занятие № 6 - ПИЕЛОНЕФРИТ 47 Занятие № 7 - ГЛОМЕРУЛОНЕФРИТ 54 Занятие № 8 - ЯЗВЕННАЯ БОЛЕЗНЬ 62 Занятие № 9 - ЗАБОЛЕВАНИЯ ЖЕЛЧЕВЫДЕЛИТЕЛЬНОЙ СИСТЕМЫ 70 Занятие № 10 - САХАРНЫЙ ДИАБЕТ 77 Занятие № 11 - ОРВИ. МЕНИНГОКОККОВАЯ ИНФЕКЦИЯ 87 Занятие № 12 - ВОЗДУШНО-КАПЕЛЬНЫЕ ИНФЕКЦИИ 95 Занятие № 13 - ДИФТЕРИЯ И СКАРЛАТИНА 104 Занятие № 14 - ОСТРЫЕ ВИРУСНЫЕ ГЕПАТИТЫ 114 Занятие № 15 - ОСТРЫЕ КИШЕЧНЫЕ ИНФЕКЦИИ 123 129 3