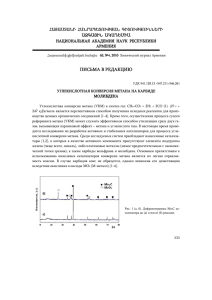
Катализаторы водяной конверсии метана в синтез-газ. Выполнила: Машина Ольга, ХТОВ-302 • Синтез-газ (смесь H2 и CO) служит исходным сырьем для производства многих химических и нефтехимических продуктов (метанол и другие оксигенаты, продукты синтеза Фишера-Тропша), а также используется для восстановления железной руды. Преобладающим сырьем для производства синтез-газа попрежнему остаются природный газ и легкие углеводороды (попутный газ или прямонный бензин) Основным методом переработки природного газа является паровая конверсия метана. После парциального окисления метана. кислородом и автотермического риформинга, который представляет собой комбинацию парциального окисления и паровой конверсии. Процесс паровой конверсии метана обычно описывается следующими равновесиями: Выражения для констант равновесия (1) и (2): Технологическая схема установки конверсии метана с водяным паром для получения CO + H2 (конфигурация с боковым обогревом) Установка для автотермического риформинга при низком соотношении пар-углерод Схема переработки углеводородного сырья с помощью автотермической риформинговой установки. Катализаторы паровой конверсии метана Для паровой конверсии метана, как правило, используется катализатор с высоким содержанием никеля (до 20% Ni в виде NiO), промотированный и нанесенный на α-оксид алюминия. Однако! В условиях, благоприятствующих получению синтез-газа с низким соотношением H2/CO, коксообразование более вероятно, поэтому катализатор паровой конверсии с высоким содержанием никеля не может быть использован. Одним из подходов к решению данной проблемы является проведение пассивированного серой процесса паровой конверсии и разработка нового катализатора для конверсии метана ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЙ В качестве активных компонентов для На основе данных приготовления катализатора были выбраны скрининговых металлы (включая Pt, Pd, Ir, Ni, Rh и Ph), экспериментов как самый которые комбинировали с носителями αAl2O3, TiO2 и ZrO2. перспективный был выбран При использовании некоторых носителей, в катализатор Pt/ZrO. частности ZrO2, в катализатор вводили платиновый катализатор, промоторы. нанесенный на диоксид Катализатор Pt/ZrO2 исследовали в условиях смешанной паровой/углекислотной циркония, в ходе работы конверсии. Процесс осуществляли в дезактивируется гораздо проточном реакторе, изготовленном из меньше, чем катализаторы специального сплава и помещенном в печь с трехзонным профилем температуры. Условия на основе никеля проведения реакции: 550ó850 °C, давление до 17 бар, объемные скорости от 1000 до 2000 чñ1, соотношение CO2/CH4 от 1,0 до 3,0, соотношение пар/метан от 0,25 до 1,6. Результаты типичных экспериментов при жестких условиях конверсии (соотношение пар/углерод равно нулю) подтверждают гораздо более высокую устойчивость Pt/ZrO2 по сравнению с Ni/Al2O3. Зависимость конверсии метана от температуры была исследована для ряда металлов VIII группы, нанесенных на диоксид циркония. Установлено, что активность изменяется в ряду: Rh, Pt > Ir, Pd > Ru. Сопоставление показателей работоспособности катализатора Pt/ZrO2 и различных промышленных никелевых катализаторов для паровой конверсии метана при повышенном давлении в жестких условиях риформинга показывает, что Pt/ZrO2 обладает наилучшими характеристиками. Модель реакции (схематически): Pt-катализатор на диоксиде циркония, вполне удовлетворяет требованиям по основным свойствам: механическим (прочность, истирание) физическим (удельная поверхность, пористость и состав) каталитическим (активность и стабильность). Химический состав катализатора неоднократно являлся предметом анализа в большом числе работ Наибольшее распространение в промышленности получили катализаторы, содержащие в качестве активного компонента металлический никель благодаря его доступности и относительно невысокой стоимости. Кроме того, активный компонент на основе металлического никеля отличается наименьшей склонностью к окислению, осернению и зауглероживанию. Помимо никельсодержащего активного компонента в их состав входят различные структурообразующие добавки (каолин, цемент, глина, графит, и др.). Катализаторы готовят различными методами: соосаждением соответствующих компонентов, смешением порошков или паст с последующими стадиями таблетирования или экструзионного формования; пропиткой носителя растворами соответствующих солей. При этом содержание никеля в катализаторах варьируется в пределах 10-60 мас.% Отличительными признаками катализаторов являются: 1. Состав активного компонента катализатора, включающий, мас.%: (3,7-16,0)NiO, (0,1-2,2)ZrO2, (0,1-4,1)Lа2О3. 2. Форма гранулы, представляющая собой трехлистник с тремя цилиндрическими отверстиями , позволяющая повысить степень использования активного компонента. Кроме того, позволяет добиться высокой турбулизации потока реакционного газа в промышленных трубчатых реакторах, обеспечивая минимальный перепад давления по высоте слоя при осуществлении турбулентного режима, а это в свою очередь способствует значительному увеличению теплоотдачи от стенки реактора к слою катализатора и наоборот. Эксперименты по испытанию эффективности работы катализаторов проводили на автоматизированной проточной каталитической установке (ПКУ -1) в лаборатории Казахского Национального университета им. аль-Фараби Республики Казахстан Оптимальные технологические параметры процесса: Т=750оС, W=1000 ч-1 и соотношение СН4:О2 = 2:1 При данных условиях конверсия метана составляет 91 %, концентрация водорода 71 об.% и монооксида углерода 72 об.%. NiLa/Al2O3 катализатор • Носитель - наибольшую активность проявляет γ — Al2O3 с удельной поверхностью равной 171 м2/г • Увеличение температуры прокалки с 300 до 1000оС влияет на величину удельной поверхности катализатора( снижение) от 172 до 118 м2/г. Также происходит уменьшения удельного объема пор от 0,084 до 0,059 см3/г, однако средний размер пор практический остается без изменений - спекание Таким образом, Катализатор в течении 30 часов не терял свою активность, соотношение Н2/СО также остается равна единице. После 16 часов проведения эксперимента концентрация водорода и СО повышаются до 72 и 73 об.%, соответственно. При этом конверсия метана составляет 91%, концентрация СО2 1,6 об.%.