Лекция 18 - Томский политехнический университет
реклама

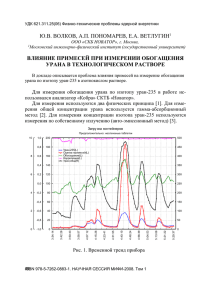
Министерство образования и науки РФ Государственное образовательное учреждение высшего профессионального образования Национальный исследовательский Томский политехнический университет Курс профессиональной переподготовки Технологии урановых добывающих и перерабатывающих предприятий Аффинаж солей урана к.т.н., доцент кафедры ХТРЭ Николай Степанович Тураев ОКСАЛАТНЫЙ АФФИНАЖ УРАНА Из солей щавелевой кислоты только оксалаты щелочных металлов и аммония растворимы в воде. Но многие оксалаты хорошо растворяются в минеральных кислотах. Так, оксалаты свинца, кадмия, висмута, меди, алюминия и трехвалентного железа легко растворяются в 0,1–0,5N растворах кислот. Оксалаты марганца, цинка, никеля, двухвалентного железа полностью растворяются в 1N азотной кислоте. Труднее растворяются в кислотах оксалаты тория, четырехвалентного урана, уранила и редкоземельных элементов. Например, в 2N азотной кислоте растворимость оксалатов тория, гадолиния и лантана составляет 0,6; 2,7 и 9,2 г/л соответственно. Следовательно, оксалатный аффинаж основан на осаждении оксалатов четырехвалентного урана и уранила в сильнокислой среде. Он может быть выполнен в двух вариантах. ОСАЖДЕНИЕ ОКСАЛАТА ЧЕТЫРЕХВАЛЕНТНОГО УРАНА Этот вариант обеспечивает более высокую степень осаждения урана (98%), так как растворимость оксалата урана (IV) меньше растворимости оксалата уранила. Растворение концентрата производится соляной кислотой, так как степень осаждения из соляно-кислой среды больше: U3O8 8HCl 2UO 2Cl 4 UCl 4 4H 2O В качестве восстановителя урана чаще используется дитионат натрия (не применяется цинк, так как он заражает продукт кадмием). Дитионат натрия берется в количестве 80% от веса концентрата, время восстановления 3–4часа, температура 80–90оС. Осаждение производится прибавлением насыщенного раствора щавелевой кислоты с избытком 30%. В качестве затравки (центров кристаллизации) вносится некоторое количество кристаллов оксалата урана. Температура процесса осаждения 80–90оС. UCl4 2H 2 C 2 O4 U (C 2 O4 ) 2 4HCl Данный процесс обеспечивает хорошую очистку от бериллия, бора, кадмия, ванадия и др. Плохо отделяется фосфор, торий, редкоземельные элементы. Для отделения редкоземельных элементов можно использовать образование комплексного раствора при действии на осадок оксалата урана растворами оксалата аммония: U(C 2O 4 ) 2 2( NH 4 ) 2 C 2O 4 ( NH 4 ) 4 [ U(C 2O 4 ) 4 ] После отделения осадка оксалатов редкоземельных элементов оксалатный комплекс разрушается кислотой: ( NH 4 ) 4[U(C2O4 ) 4 ] 4HCl U(C2O4 ) 2 2H 2C2O4 4NH 4Cl Технологическая схема проведения оксалатного аффинажа в этом варианте представлена на рис. Следующего слайда. Концентрат 30% HCl Столярный клей для коагуляции H2SiO3 Растворение | t=65oC, τ=2 часа, | Т:Ж=1:3 Фильтрация Раствор | СU=160-200 г/л | СHCl=5% Не растворенный остаток Na2S2O4 Восстановление урана На выщелачивание урана Декантация или фильтрация Осадок серы Насыщенный раствор H2C2O4 Раствор UCl4 Осаждение Фильтрация Раствор примесей Осадок U(C2O4)2 Осаждение урана Фильтрация Прокаливание при 500-600оС в инертной атмосфере Раствор UO2 NH4OH Осадок полиураната аммония Отвал Прокаливание на воздухе при 700-800оС На аффинаж U 3O 8 Технологическая схема осаждения оксалата четырехвалентного урана ОСАЖДЕНИЕ ОКСАЛАТА УРАНИЛА При действии щавелевой кислоты на раствор нитрата уранила осаждается тригидрат оксалата уранила: UO 2 ( NO3 ) 2 H 2C2O4 3H 2O UO 2C2O4 3H 2O 2HNO 3 Растворимость тригидрата повышении температуры резко увеличивается при Растворимость тригидрата оксалата уранила в воде Растворимость тригидрата увеличивается при повышении концентрации азотной кислоты и, особенно, щавелевой кислоты. Растворимость тригидрата оксалата уранила в азотной кислоте при 20оС Растворимость тригидрата оксалата уранила в щавелевой кислоте (20оС). Повышение растворимости тригидрата в щавелевой кислоте связывают с образованием растворимого комплекса: UO 2C2O 4 H 2C 2O 4 H 2 [ UO 2 (C2O 4 ) 2 ] Большая растворимость оксалата уранила по сравнению с оксалатом четырехвалентного урана снижает прямой выход урана в осадок до 95%. Концентрация азотной кислоты при осаждении берется в пределах, обеспечивающих растворение оксалатов примесей, щавелевая кислота при осаждении вносится в виде кристаллов с минимальным избытком. Осаждение проводится при комнатной температуре. Технологическая схема процесса приведена на рис. Следующего слайда. Концентрат HNO3 Растворение Фильтрация Не растворенный остаток Раствор | С(U)=200 г/л | С(HNO3)=100-150 г/л На извлечение урана Осаждение Кристаллы H2C2O4 порциями Фильтрация Кристаллы UO2C2O4 Раствор NH4OH Прокаливание при 400-500оС Прокаливание при 550-600 С в восстановительной атмосфере UO3 Прокаливание при 700-800оС Осаждение урана Фильтрация Осадок Раствор Аффинаж Сброс UO2 U 3O 8 Технологическая схема осаждения оксалата уранила Для получения диоксида урана недостаточна инертная атмосфера, так как при разложении оксалата уранила образуется только стехиометрическое количество восстановителя монооксида углерода: UO 2C 2O 4 UO 3 CO 2 CO UO3 CO UO 2 CO 2 В данном варианте отделяются те же примеси, что и при осаждении оксалата четырехвалентного урана. Для отделения редкоземельных элементов можно обработать осадок оксалата уранила раствором оксалата аммония с образованием комплексного раствора: UO 2C2O 4 2( NH 4 ) 2 C2O 4 ( NH 4 ) 4 [ UO 2 (C2O 4 )3 ] а затем после отделения примесей разрушить комплекс кислотой: Большим преимуществом второго варианта перед первым является меньшее количество стадий и меньший расход реагентов, что может компенсировать некоторое снижение степени осаждения. КАРБОНАТНЫЙ АФФИНАЖ УРАНА При взаимодействии растворов солей уранила и карбоната или бикарбоната аммония образуется комплексный раствор (NH4)2[UO2(CO3)3]. Растворимость аммоний-уранилтрикарбонатного комплекса (АУТК) в воде приведена в таблице. Растворимость АУТК в воде при различных температурах Следовательно, при 40оС мы можем получить комплексный раствор урана с концентрацией 40–45 г/л. При этом будут отделяться от урана элементы, образующие в карбонатной среде нерастворимые карбонаты и гидроксиды: щелочноземельные элементы, железо, алюминий, тяжелые металлы, редкоземельные элементы. Растворимость АУТК уменьшается с концентрации карбоната и бикарбоната аммония. увеличением Значит, при охлаждении раствора и насыщении его карбонатом или бикарбонатом можно снизить содержание урана в маточных растворах ниже 1 г/л, то есть обеспечить степень осаждения урана около 98 %. При этом те примеси, которые при образовании комплексного раствора урана находились вместе с ним в растворе, при высаливании АУТК останутся в растворе. На этой стадии уран отделяется от лития, бора, ванадия, фосфора, натрия. Большим достоинством карбонатного аффинажа является очистка от широкого круга элементов, как растворимых, так и нерастворимых в карбонатной среде. В зависимости от состава раствора используют или обе операции (образование комплексного раствора урана и высаливание АУТК) последовательно, или какую-либо одну из них. Иногда операцию высаливания АУТК проводят дважды. Это позволяет добиться ядерной чистоты. Часто карбонатный аффинаж комбинируется с другими аффинажными операциями, особенно с экстракцией, когда реэкстракция проводится растворами карбоната или бикарбоната аммония. Технологическая схема проведения карбонатного аффинажа приведена на следующем слайде. Концентрат HNO3 Растворение Фильтрация Раствор Не растворенный остаток SiO2 c~1% урана NH4HCO3 Перевод в t=40-50oC, t=2 часа карбонатный ост. конц. комплекс NH4HCO3=0,5% На выщелачивание Фильтрация Осадки гидроксидов и Комплексный раствор С(U)=40г/л карбонатов примесей NH4HCO3 Высаливание АУТК конц. 300 г/л охлаждение до 10оС Фильтрация Добавка свежего NH4HCO3 Кристаллы АУТК Фильтрат NH4HCO3 Промывка насыщенным Термическое разложение раствором NH4HCO3 при 100оС Кристаллы АУТК Прокаливание на воздухе при 750оС U3O8 Промывные воды Пары NH3, CO2, H2O Cуспензия Конденсация NH4OH Прокаливание в инертной атмосфере при 700оС UO2 Доосаждение урана Фильтрация Осадок Раствор На аффинаж Сброс Технологическая схема проведения карбонатного аффинажа При прокаливании АУТК в зависимости от условий можно получить UO3, U3O8, или UO2. ( NH 4 ) 4 [UO2 (CO3 ) 3 ] UO3 3CO2 4 NH 3 2 H 2 O 400o C Восстановление происходит за счет водорода, получающегося при разложении аммиака, оно происходит при температуре выше 600оС. практически оксид имеет кислородное отношение от 2,04 до 2,09.