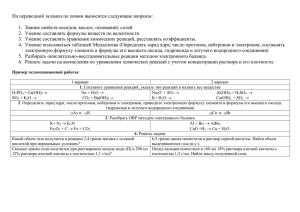
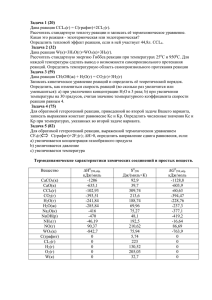
belorusova_prez
реклама

ГБОУ школа №501 Учитель химии Белорусова Марина Вадимовна Санкт-Петербург 2013 Содержание • • • • • • • • • Химическая реакция Признаки химических реакций Условия протекания химических реакций Реакции соединения Реакции разложения Реакции замещения Реакции обмена Закрепление материала Домашнее задание Химическая реакция • Явления, в результате которых из одних веществ образуются другие, называют химическими явлениями или химическими реакциями. Признаки химических реакций • ВЫПАДЕНИЕ ИЛИ РАСТВОРЕНИЕ ОСАДКА • ВЫДЕЛЕНИЕ ГАЗА • ИЗМЕНЕНИЕ ОКРАСКИ ВЕЩЕСТВА • ПОЯВЛЕНИЕ ЗАПАХА • ВЫДЕЛЕНИЕ ТЕПЛОТЫ ИЛИ СВЕТА Условия протекания реакций • Измельчение и смешивание веществ • Растворение веществ • Нагревание • Создание особых условий (электрический ток, свет, катализатор) Реакции соединения А+В→С • Реакция соединения – из двух ил и нескольких простых или сложных веществ образуется одно сложное вещество. Fe + S → FeS + = Расставьте коэффициенты в следующих уравнениях реакций: • • • • • N2 + O2 → NO SO2 + O2 → SO3 CaO + H2O → Ca(OH)2 Ca + O2 → CaO Al + Br2 → AlBr3 Что общего у всех записанных уравнений? Реакции разложения С → А + В + ... • Реакция разложения – из одного сложного вещества образуются два или несколько или сложных веществ. 2HgO → 2Hg + O2 Расставьте коэффициенты в следующих уравнениях реакций: • • • • • Fe(OH)3 → Fe2O3 + H2O KMnO4 → K2MnO4 + MnO2 + O2 HNO3 → H2O + NO2 + O2 CaCO3 → CaO + CO2 (NH4)2Cr2O7 → Cr2O3 + H2O + N2 Какими признаками сопровождается последняя реакция? Реакции замещения А + ВС → АС + В • Реакция замещения – атомы простого вещества замещают атомы одного из химических элементов в сложном веществе. Mg+ 2HCl → MgCl2 + H2 Реакции замещения • Fe + CuSO4 → Cu + FeSO4 • Zn + 2HCl → ZnCl2 + H2 Расставьте коэффициенты в следующих уравнениях реакций: • Al + CuO → Al2O3 + Cu • Zn + AgNO3 → Zn(NO3)2 + Ag • Fe2O3 + H2 → Fe + H2O • Al + HCl → AlCl3 + H2 Реакции обмена АВ + СД → АД + СВ • Реакции обмена - реакции между двумя сложными веществами, в результате которых они обмениваются своими составными частями. CuO + 2HCl → CuCl2 + H2O Условия протекания реакций обмена • Выпадение осадка CuSO4 + 2NaOH → Cu(OH)2 ↓ + Na2SO4 • Выделение газа Na2CO3 + H2SO4 → Na2SO4 + H2CO3 H2CO3 → H2O + CO2 ↑ • Образование воды NaOH + HCl NaCl + H2O Расставьте коэффициенты в следующих уравнениях реакций: • • • • • Na2SO4 + ВаСl2 → NaСl + ВаSO4 СuCI2 + KOH → Cu(OH)2 + KCI Mg(OH)2 + HCI → H2O + CuCI2 AgNO3+ KBr → AgBr +КNO3 CuO + H2SO4 → CuSO4 + H2O Закрепление материала Домашнее задание Напишите уравнения реакций по названиям исходных веществ и продуктов реакций. Определите типы реакций. 1. 2. 3. 4. 5. Сульфат магния + гидроксид натрия → гидроксид магния + сульфат натрия. Хлорид калия + нитрат серебра → нитрат калия + хлорид серебра. Железо + соляная кислота → хлорид железа (II) + водород. Оксид меди + оксид азота (Y) → нитрат меди. Железо + сера → сульфид железа (II).