Исследование водопроводной воды на содержание ионов
реклама

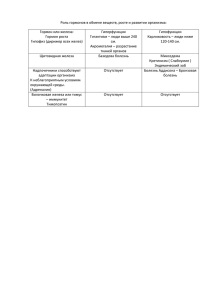
Исследование водопроводной воды на содержание ионов железа(III) Цель: оценить качество воды в МОУ лицее Шатурского муниципального района Московской области. Основными потребителями воды на нашей планете являются города Потребление воды жителем крупного города: 700 л Оптимальное потребление воды жителем крупного города: 250 л С помощью физических, химических, биологических исследований можно оценить качество воды и обозначить тенденции в его изменении. Эти исследования дают понять, какие воздействия на водоемы являются неблагоприятными и каким образом можно восстановить здоровье воды. Поверхностные воды Шатурского района обладают повышенной ожелезненностью, превышающей допустимую норму в несколько раз (в водных объектах содержание железа должно определяться ПДК, т.е. быть менее 0,3 мг/л, лишь в загрязненных водоемах концентрация ионов железа (III) возрастает до 8 мг/л!). Это – одна из природных особенностей нашей заболоченной и заторфованной территории. Для исследований в качестве объекта можно брать воду не только из природных источников (рек, озер, прудов, родников и т.д.), но и из водопровода, то есть питьевую. Особенно важно и актуально проводить данные исследования в детских учреждениях, где существует питьевой режим. МЕТОДИКА. В основе методики нашего исследования использованы методы аналитической химии. 1. Тест-метод определения ионов железа (III). В последние годы большое внимание уделяется использованию реактивных индикаторных бумаг для определения для определения ионов железа (II, III). Предложено большое количество реагентов, однако, представляет интерес рассмотреть тестметод с использованием 2-х реагентов: гексацианоферрата (II) калия и роданида аммония. Эти реагенты применяются при изучении химии в средней школе. Для определения ионов железа (III) (проведения тест-метода) были приготовлены стандартные растворы. Эталонный раствор с содержанием ионов железа (III) 1мг/мл готовили растворением точной навески – FeNH4 (SO4 )2 12H 2O Навеску массой 4,3036 г растворили в мерной колбе емкостью 500мл. Добавляли 2мл H 2 SO4 конц. и доводили объем колбы до метки. Перемешивали. H 2 SO4 добавляли для подавления гидролиза. Растворы меньшей концентрации готовили в день исследовани Десятикратным разбавлением эталонного раствора был получен раствор с концентрацией ионов железа (III) 100 мг/л. Раствор с концентрацией 50 мг/л готовили так: пипеткой собирали 25 мл эталонного раствора и помещали в мерную колбу на 500 мл. Доводили дистиллированной водой до метки. Раствор с концентрацией 10 мг/л получали десятикратным разбавлением раствора, содержащего 100 мг/л ионов железа. Десятикратным разбавлением раствора, в котором содержалось 10 мг/л ионов железа (III) готовили раствор, содержащий 1 мг/л ионов железа (III). Десятикратным разбавлением соответствующих растворов были получены растворы, содержащие 0,5 и 0,1 мг/л ионов железа (III). Таким образом, приготовленные растворы содержали от 0,1 до 10 мг/л ионов железа. Наиболее простая реактивная бумага может быть приготовлена путем пропитки фильтровальной бумаги в 10% растворе роданида аммония (РИБ-Р). Кроме того, можно приготовить реактивную индикаторную бумагу – РИБ – на основе гексацианоферрата (II) калия (РИБ ГЦФ (II)) Большой интерес представляют данные, полученные реактивной индикаторной бумагой на основе гексацианоферрата (II) калия. Реактивная индикаторная бумага РИБ-ГЦФ(II) светло-бурого цвета при погружении РИБ в раствор, содержащий ионы железа (III) в концентрациях более 10 мл/г бумага приобретает голубую окраску, но более яркое изменение окраски наблюдается в растворе. При возрастании концентрации интенсивность окрашивания увеличивается от голубого до интенсивно синего цвета (10 мг/л до 50 мг/л). 2. Приготовление РИБ на основе гексацианоферрата (II) калия. Нарезали полоски фильтровальной бумаги 2 5см 2 Пропитали раствором 2 3 сульфата меди (II) разной концентрации ( 10 и 10 моль/л), высушили тепловентилятором (электрическим феном). Высушенную бумагу обработали раствором гексацианоферрата (II) 3 2 1 калия различной концентрации ( 10 ,10 , 5 10 моль/л). В химические стаканы помещали по 50 мл каждого из стандартных растворов. Растворы подкисляли до pH=1, пользуясь универсальной индикаторной бумагой. В каждый раствор вносили тест-полоски размером 1*1 квадратный см. и наблюдали за изменениями в растворе и на бумаге. Обработка бумаги раствором сульфата меди проводилась с целью устранения мешающего влияния ионов меди (II) на определение ионов железа (III). Ионы меди с гексацианоферратом образуют осадок бурого цвета. Было установлено, что при обработке индикаторной бумаги раствором сульфата меди в концентрации 1 10 3 моль/л устраняется мешающее влияние ионов меди. При изменении концентрации гексацианоферрата (II) калия в широком диапазоне концентраций найдено, что наилучший видимый эффект наблюдается при обработке бумаги гексацианоферратом (II) калия в концентрации 0,5 моль/л. РИБ ГЦФ (II) логично обнаружить ионы железа (III) до концентрации 0,15 мг/л. Причем, изменение окраски бумаги практически не наблюдается, раствор становится голубым. В зависимости от концентрации ионов железа в растворе изменение окраски раствора происходит во времени: при концентрации 10 мг/л появляется синее окрашивание раствора сразу после погружения в раствор индикаторной бумаги, при концентрации 5 мг/л раствор становится голубым через 2 секунды, при концентрации ионов железа 1; 0,5; 0,25 мг/л изменение окраски наблюдается через 2, 3 и 5 минут соответственно. Во времени интенсивность окраски увеличивается. Таким образом, полуколичественное определение ионов железа (III) можно проводить тест-методом анализа с использованием реактивной индикаторной бумаги на основе гексацианоферрата (II) калия. Индикаторная бумага сохраняется длительное время (3 мес). Полученную реактивную бумагу необходимо хранить в герметичной упаковке. РЕЗУЛЬТАТЫ. Для исследования содержания ионов железа (III) в питьевой воде Шатурского лицея использовался тест-метод анализа при помощи реактивной индикаторной бумаги на основе гексацианоферрата (II) калия. При этом использовалась РИБ ГЦФ (II), обработанная раствором сульфата меди в концентрации 0,01 моль/л и гексацианоферратом (II) калия в концентрации 0,5 моль/л. Таблица 2. Содержание ионов железа (III) в пробах водопроводной воды Шатурского лицея и Мебельной компании «ШАТУРА» (ОАО МК «ШАТУРА» ) ОАО МК «ШАТУР А» Шатурский лицей водопроводный кран цеха ДСП водопроводн ый кран (I этаж) водопроводны й кран (II этаж) водопроводн ый кран (III этаж) Р-р синего цвета Р-р голубого цвета Р-р стал голубым и посинел через 1 мин. Р-р голубого цвета Контроль (Н2О дист.) Р-р бесцветный ВЫВОДЫ И РЕКОМЕНДАЦИИ. По изменению окраски (и ее интенсивности) проб воды во времени (таблица) можно сделать вывод о том, что содержание ионов железа (III) в водопроводной воде Шатурского лицея 1-5 мг/л, что превышает ПДК, как минимум, в 2 раза, и как максимум ,в 16 раз. Для решения данной проблемы мы решили использовать специальные фильтры («Барьер», «Аквафор» и др.), которыми были обеспечены все классы. При проведении тест-метода после фильтрации вода окрашивается в бледно-голубой цвет менее интенсивно и несколько позже. Считаем, что на первых этапах восстановления качества питьевой воды данное решение является приемлемым.