pril.1. atom
реклама
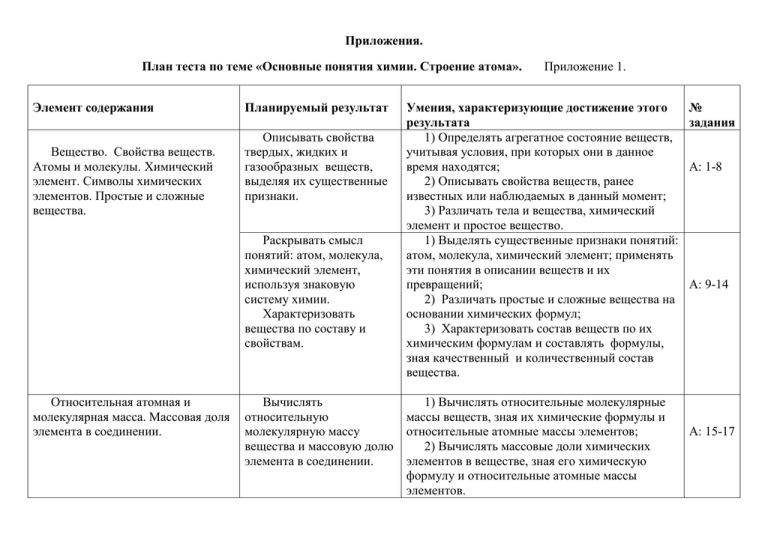
Приложения. План теста по теме «Основные понятия химии. Строение атома». Элемент содержания Вещество. Свойства веществ. Атомы и молекулы. Химический элемент. Символы химических элементов. Простые и сложные вещества. Планируемый результат Описывать свойства твердых, жидких и газообразных веществ, выделяя их существенные признаки. Раскрывать смысл понятий: атом, молекула, химический элемент, используя знаковую систему химии. Характеризовать вещества по составу и свойствам. Относительная атомная и молекулярная масса. Массовая доля элемента в соединении. Приложение 1. Умения, характеризующие достижение этого результата 1) Определять агрегатное состояние веществ, учитывая условия, при которых они в данное время находятся; 2) Описывать свойства веществ, ранее известных или наблюдаемых в данный момент; 3) Различать тела и вещества, химический элемент и простое вещество. 1) Выделять существенные признаки понятий: атом, молекула, химический элемент; применять эти понятия в описании веществ и их превращений; 2) Различать простые и сложные вещества на основании химических формул; 3) Характеризовать состав веществ по их химическим формулам и составлять формулы, зная качественный и количественный состав вещества. Вычислять 1) Вычислять относительные молекулярные относительную массы веществ, зная их химические формулы и молекулярную массу относительные атомные массы элементов; вещества и массовую долю 2) Вычислять массовые доли химических элемента в соединении. элементов в веществе, зная его химическую формулу и относительные атомные массы элементов. № задания А: 1-8 А: 9-14 А: 15-17 Строение атома. Ядро (протоны, нейтроны) и электроны. Изотопы. Строение электронных оболочек атомов элементов № 1-20 периодической системы химических элементов Д.И. Менделеева. Физический смысл порядкового номера химического элемента в периодической системе, номера периода и номера группы элементов. Описывать и характеризовать табличную форму периодической системы химических элементов. Характеризовать состав атомных ядер и распределение электронов по энергетическим уровням в атомах элементов малых периодов, а также калия и кальция. 1) Различать понятия: малый период, большой период, главная и побочная подгруппы (А-группа А: 18,19 и Б-группа соответственно). Закономерности изменения свойств химических элементов в связи с положением в периодической системе химических элементов. Объяснять закономерности в изменении характерных свойств химических элементов в пределах групп и малых периодов. Раскрывать смысл химических понятий: ион, катион, анион, валентность, электроотрицательность, степень окисления, используя знаковую систему химии. 1) Объяснять физический смысл порядкового номера элемента в периодической системе, номера периода и номера группы; А: 24-28 2) Объяснять закономерности в изменении характерных свойств химических элементов в пределах групп и малых периодов. 1) Выделять существенные признаки понятий: ион, катион, анион и применять эти понятия при описании веществ и их превращений А: 29-32 2) Определять степень окисления элемента В: 1, 2 по его положению в периодической системе; 3) Определять значение валентности и степени окисления химических элементов в бинарных соединениях; 4) Составлять формулы бинарных соединений Строение веществ. Ионы (катионы и анионы). Ионная химическая связь. Электроотрицательность. Ковалентная (полярная и неполярная) химическая связь. Валентность и степень окисления химических элементов в соединениях. Металлическая связь. 1) Определять число протонов ядре атома химического элемента по его положению в периодической системе; 2) Определять число электронов в атоме и А: 20-23 вычислять число нейтронов в ядре атома элемента; 3) Устанавливать порядок распределения электронов по энергетическим уровням в атоме на основании положения химического элемента в периоде и группе периодической системы. по валентности или степени окисления элементов; 5) Называть бинарные соединения по систематической номенклатуре. Количество вещества. Моль. Молярная масса. Постоянная Авогадро. Молярный объем газов. Определять виды химической связи в простых и сложных веществах. Раскрывать смысл понятий: количество вещества, моль, молярная масса вещества, молярный объем газов, постоянная Авогадро, нормальные условия. 1) Различать вещества, образованные ионной, ковалентной полярной, ковалентной неполярной и металлической связью. 1) Соотносить относительную молекулярную и молярную массу вещества; 2) Производить вычисления массы, объема, числа частиц или количества вещества по формулам, связывающим эти параметры. А: 33 А: 34 В: 3 Время выполнения теста – 40 мин. При выполнении заданий части А необходимо выбрать один правильный ответ из четырех предложенных. Каждое верно выполненное задание оценивается в 1 балл. Максимальная сумма баллов за задания части А – 34 балла. При выполнении заданий части В к каждому элементу первого столбца необходимо подобрать соответствующий элемент из второго столбца. Выбранные цифры записываются под соответствующими буквами в таблице ответов. Оцениваются задания части В так: все три ответа верны – 2 балла; один ответ ошибочен – 1 балл; два и более ответа ошибочны – 0 баллов. Максимальная сумма баллов за задания части В – 6 баллов. Итого максимальная сумма баллов за тест – 40 баллов. Оценка выставляется следующим образом: 36 – 40 баллов – «5», 30 – 36 баллов – «4», 26 – 30 баллов – «3», менее 26 баллов – «2».








