1 Содержание Задача №1 3 Задача №2 7 Задача №3. Расчёт
реклама

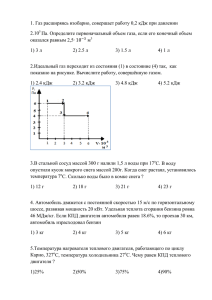
2 Содержание Задача №1 Задача №2 Задача №3. Расчёт параметров воздушной холодильной машины Список литературы Это полнотекстовый пример работы, выполненной специалистами www.MagazinZnaniy.ru 3 7 13 15 3 Задача №1 Газовая смесь состоящая из трех газов ( CO2 , N 2 и O2 ) в количестве m1 5,4 кг , m2 3,8 кг и m3 4,2 кг с начальными параметрами p1 220 кПа и t1 61 C , нагревается до t2 450 C при постоянном давлении p const . Определить: объемный состав смеси; ее начальный и конечный объемы V1 и V2 ; кажущуюся индивидуальную газовую постоянную смеси Rсм ; кажущуюся молекулярную массу смеси см ; теплоту Q12 , участвующую в процессе; среднюю теплоемкость смеси в данном процессе; работу расширения газовой смеси; изменение внутренней энергии, энтальпии и энтропии смеси в процессе. Решение: 1 Масса смеси газов равна: mсм m1 CO2 m2 N 2 m3 O2 , mсм 5,4 3,8 4,2 13,4 кг . Определяем массовую долю каждого газа в смеси: диоксида углерода CO2 : g1 CO2 m1 5,4 0,403 ; mсм 13,4 g 2 N 2 m2 3,8 0,284 ; mсм 13,4 g 3 O2 m3 4,2 0,313 . mсм 13,4 азота N 2 : кислорода O2 : Объемный состав смеси определяем по формуле: gi ri i 3 gi 1 i , где молекулярная масса равна: для CO2 – 1 44,01 ; для N 2 – 2 28,02 ; для O2 – 3 32,00 . Это полнотекстовый пример работы, выполненной специалистами www.MagazinZnaniy.ru 4 Тогда g1 0,403 1 44,01 r1 CO2 0,315 ; g1 g 2 g 3 0,403 0,284 0,313 1 2 3 44,01 28,02 32,00 g2 0,284 2 28,02 r2 N 2 0,349 ; g1 g 2 g 3 0,403 0,284 0,313 1 2 3 44,01 28,02 32,00 g3 0,313 3 32,00 r3 O2 0,336 . g1 g 2 g 3 0,403 0,284 0,313 1 2 3 44,01 28,02 32,00 2 Кажущуюся молекулярную массу смеси см находим по формуле через объемный состав: 3 см ri g i 0,315 44,01 0,349 28,02 0,336 32,00 8 1,8 18,2 34,4 . i 1 3 Кажущаяся индивидуальная газовая постоянная смеси Rсм равна: Rсм 8314 см 8314 Дж 241,7 . 34,4 кг К 4 Из уравнения pV MRT найдем начальный объем смеси V1 : p1V1 mRT1 V1 mRT1 , p1 13,4 241,7 61 273 1,92 м 3 . 3 220 10 Из соотношения для изобарного процесса p const найдем конечный V1 объем смеси V2 : V1 T1 V2 T2 V2 4,92 V2 V1 T2 , T1 450 273 40,65 м3 . 61 273 5 Найдем средние теплоемкости c pm . Средние молярные теплоемкости каждого газа (путем интерполяции для отсутствующих в таблице значений): диоксид углерода CO2 : 38,112 35,860 кДж 61 0 36,738 ; 100 0 моль град 44,573 43,25 кДж c pm1 CO2 0450 44,573 450 400 43,9115 ; 500 400 моль град c pm1 CO2 61 38,112 0 Это полнотекстовый пример работы, выполненной специалистами www.MagazinZnaniy.ru 5 450 c pm1 CO2 61 43,9115 450 36,738 61 кДж ; 45,036 450 61 моль град азот N 2 : 29,048 29,019 кДж ; 61 0 29,030 100 0 моль град 29,764 29,500 кДж ; c pm2 N 2 0450 29,764 450 400 29,632 500 400 моль град 29,632 450 29,030 61 кДж 450 . c pm2 N 2 61 29,726 450 61 моль град c pm2 N 2 61 29,048 0 кислород O2 : 29,538 29,274 кДж ; 61 0 29,377 100 0 моль град 31,334 30,878 кДж ; c pm3 O2 0450 31,334 450 400 31,106 500 400 моль град 31,106 450 29,377 61 кДж 450 . c pm3 O2 61 31,377 450 61 моль град c pm3 O2 61 29,538 0 Средняя молярная теплоемкость газовой смеси при постоянном объеме равна: 3 c pm см ri c pm 0,315 45,036 0,349 29,030 0,336 31,377 34,86 i 1 кДж . моль град Средние массовые теплоемкости: диоксид углерода CO2 : c pm1 CO2 c p1 45,036 кДж ; 1,023 44,01 кг град c pm2 N 2 c p 2 29,030 кДж ; 1,036 28,02 кг град c pm3 O2 c p3 31,377 кДж . 0,98 32,00 кг град азот N 2 : кислород O2 : Средняя массовая теплоемкость газовой смеси при постоянном объеме равна: 3 c pm см g i c pmi 0,403 1,023 0,284 1,036 0,313 0,98 1,013 1 кДж . кг град Средние объемные теплоемкости: диоксид углерода CO2 : Это полнотекстовый пример работы, выполненной специалистами www.MagazinZnaniy.ru 6 cpm1 CO2 азот N 2 : c p1 22,4 cpm2 N 2 c p 2 cpm3 O2 c p 3 кислород O2 : 22,4 22,4 45,036 кДж ; 2,01 22,4 кг град 29,030 кДж ; 1,296 22,4 кг град 31,377 кДж . 1,40 22,4 кг град Средняя массовая теплоемкость газовой смеси при постоянном объеме равна: 3 cpm см ri cpmi 0,315 2,01 0,349 1,296 0,336 1,40 1,556 1 кДж . м град 3 6 Количество тепла, получаемое газовой смесью при ее нагревании от t1 61 C до t2 450 C равно: Q M см q M см c pm см t 2 t1 ; Q 13,4 1,013 450 61 5280 кДж 5,28 МДж . 7 Работа расширения газовой смеси равна: L Rсм T2 T1 M см 241,7 723 334 13,4 1260 кДж 1,26 МДж ; L 241,7 723 334 13,4 1260 кДж 1,26 МДж . 8 Учитывая, что Q U L (первый закон термодинамики), найдем изменение внутренней энергии: U Q L ; U 5,28 1,26 4,02 МДж . 9 Изменение энтальпии газовой смеси в изобарном процессе равно: i c pm см t 2 t1 M см Q ; i Q 5,28 МДж . 10 Изменение энтропии газовой смеси в процессе равно: T кДж 723 . S c pm см ln 2 M см 1,013 ln 13,4 10,5 К 334 T1 Ответ: – r1 CO2 0,315 ; r2 N2 0,349 ; r3 O2 0,336 ; – V1 1,92 м3 ; V2 40,65 м3 ; – Rсм 241,7 Дж ; кг К – см 34,4 ; – Q 5,28 МДж ; – c pm см 34,86 кДж кДж кДж ; c pm см 1,013 ; cpm см 1,556 3 ; моль град кг град м град – L 1,26 МДж ; – U 4,02 МДж ; i 5,28 МДж ; S 10,5 кДж К . Это полнотекстовый пример работы, выполненной специалистами www.MagazinZnaniy.ru 7 Задача №2 Трехступенчатый компрессор сжимает газ. Определить: удельные объемы газа после сжатия в I , II и III ступенях; изменение энтальпии в ходе сжатия в I , II и III ступенях; изменение энтальпии газа при прохождении через межступенчатые (и концевой) холодильники; кажущуюся индивидуальную газовую постоянную смеси Rсм ; кажущуюся молекулярную массу смеси см ; теплоту, отводимую в межступенчатых и концевом холодильниках; среднюю теплоемкость смеси в данном процессе; удельную работу сжатия газа. Построить диаграммы циклов в координатах p v t1 и t s . Дано : pa 100000 Па 0,1 МПа Ta 301 К p1 502000 Па 0,502 МПа p2 3450000 Па 3,45 МПа p3 19500000 Па 19,5 МПа n 1,2625 Азот, 28 Решение: Принцип работы трехступенчатого компрессора: Через клапан первой ступени происходит всасывание азота с давлением pa 0,1 МПа и температурой Ta 301 К . После сжатия азот через охладитель направляется во вторую ступень компрессора. Всасывание газа во второй ступени происходит при давлении сжатия в первой ступени. Всасывание газа в третьей ступени выполняется через промежуточный охладитель при давлении сжатия во второй ступени. Через нагнетательный клапан третьей ступени осуществляется нагнетание азота в резервуар (концевой холодильник). 1 Степень сжатия азота в первой ступени компрессора равна: x1 p1 0,502 5,02 . pa 0,1 Это полнотекстовый пример работы, выполненной специалистами www.MagazinZnaniy.ru 8 Температура воздуха после сжатия в первой ступени равна: p T1 Ta 1 pa n 1 n 1, 26251 0,502 1, 2625 301 421 К . 0,1 Удельный объем азота после сжатия в первой ступени компрессора равен: vI RT1 296,8 421 0,25 м 3 кг . 6 p1 0,502 10 Массовая теплоемкость, молярная масса и газовая постоянная азота равны: кДж ; кг К N2 14 2 28 ; Дж R 296,8 ; кг К c p 1,04 cv c p R 1,04 0,2968 0,7432 кДж . кг К Тогда изменение энтальпии газа в ходе сжатия в первой ступени равно: i1 c p T1 Ta 1,04 421 301 124,8 кДж кг . Количество теплоты, отводимое от азота при политропном сжатии в первой ступени, равно: q1 cv nk 1,2625 1,4 T1 Ta 0,7432 421 301 46,7 кДж кг . n 1 1,2625 1 Средняя теплоемкость охлаждении равна: c pm1 азота при промежуточном изобарном 1,0418 421 1,040 301 кДж 1,046 . 421 301 кг К Так как в межступенчатых и концевом холодильниках азот изобарно охлаждается до начальной температуры Ta 301 К , то изменение энтальпии в межступенчатом холодильнике между первой и второй ступенью компрессора равно: i1 c pm1 T1 Ta 1,046 421 301 125,52 кДж кг Количество теплоты, отводимое от азота при изобарном охлаждении, равно: промежуточном q1 c pm1 Ta T1 1,046 301 421 125,52 кДж кг . Это полнотекстовый пример работы, выполненной специалистами www.MagazinZnaniy.ru 9 Работа равна: n 1 p1 n n l1 R Ta 1 ; n 1 pa 1, 26251 1,2625 0,502 1, 2625 l1 296,8 301 1 171,26 кДж кг . 1,2625 1 0,1 2 Степень сжатия азота во второй ступени компрессора равна: x2 p2 3,45 6,87 . p1 0,502 Температура воздуха после сжатия во второй ступени равна: p T2 Ta 2 p1 n1 n 1, 26251 3,45 1, 2625 301 449,4 К . 0,502 Удельный объем азота после сжатия во второй ступени компрессора равен: vII RT2 296,8 449,4 0,04 м 3 кг . p2 3,45 106 Изменение энтальпии газа в ходе сжатия во второй ступени равно: i2 c p T2 Ta 1,04 449,4 301 154,34 кДж кг . Количество теплоты, отводимое от азота при политропном сжатии во второй ступени, равно: q2 cv nk 1,2625 1,4 T2 Ta 0,7432 449,4 301 57,8 кДж кг . n 1 1,2625 1 Средняя теплоемкость охлаждении равна: c pm2 азота при промежуточном изобарном 1,0427 449,4 1,040 301 кДж . 1,048 449,4 301 кг К Так как в межступенчатых и концевом холодильниках азот изобарно охлаждается до начальной температуры Ta 301 К , то изменение энтальпии в межступенчатом холодильнике между второй и третьей ступенью компрессора равно: i2 c pm2 T2 Ta 1,048 449,4 301 155,52 кДж кг Это полнотекстовый пример работы, выполненной специалистами www.MagazinZnaniy.ru 10 Количество теплоты, отводимое от азота при промежуточном изобарном охлаждении, равно: q2 c pm2 Ta T2 1,048 301 449,4 155,52 кДж кг Работа равна: n 1 p2 n n l2 R Ta 1 ; n 1 p1 1, 26251 1,2625 3,45 1, 2625 l2 296,8 301 1 211,82 кДж кг . 1,2625 1 0,502 3 Степень сжатия азота в третьей ступени компрессора равна: x3 p3 19,5 5,65 . p2 3,45 Температура воздуха после сжатия в третьей ступени равна: p T3 Ta 3 p2 n 1 n 1, 26251 19,5 1, 2625 301 431,5 К . 3,45 Удельный объем азота после сжатия в третьей ступени компрессора равен: vIII RT3 296,8 431,5 0,0066 м 3 кг . 6 p3 19,5 10 Изменение энтальпии газа в ходе сжатия в третьей ступени равно: i2 c p T3 Ta 1,04 431,5 301 135,72 кДж кг . Количество теплоты, отводимое от азота при политропном сжатии в третьей ступени, равно: q3 cv nk 1,2625 1,4 T3 Ta 0,7432 431,5 301 50,8 кДж кг . n 1 1,2625 1 Средняя теплоемкость азота при изобарном охлаждении в концевом холодильнике равна: c pm3 1,042 431,5 1,040 301 кДж 1,0466 . 431,5 301 кг К Это полнотекстовый пример работы, выполненной специалистами www.MagazinZnaniy.ru 11 Так как в межступенчатых и концевом холодильниках азот изобарно охлаждается до начальной температуры Ta 301 К , то изменение энтальпии в концевом холодильнике равно: i3 c pm3 T3 Ta 1,0466 431,5 301 136,58 кДж кг Количество теплоты, отводимое от азота при промежуточном изобарном охлаждении, равно: q3 c pm3 Ta T1 1,0466 301 431,5 136,58 кДж кг Работа равна: n 1 p3 n n l3 R Ta 1 ; n 1 p2 1, 26251 1,2625 19,5 1, 2625 l3 296,8 301 1 186,27 кДж кг . 1,2625 1 3,45 4 Работы компрессора равна сумме работ: 3 lк li l1 l2 l3 , 1 lк 171,26 211,82 186,27 569,35 кДж кг . 5 Диаграммы циклов компрессора. Рисунок 1 Индикаторная диаграмма трехступенчатого компрессора в координатах p v t1 Это полнотекстовый пример работы, выполненной специалистами www.MagazinZnaniy.ru 12 В первой ступени компрессора газ сжимается от давления pI pa до давления pII p1 (сжатие идет по политропе 1 a ). Затем, выйдя из цилиндра первой ступени, газ по изобаре pII const охлаждается в холодильнике I (между первой и второй ступенью) до исходной температуры Ta (точка b , так же как и точка 1 , лежит на изотерме 1 b d e , соответствующей температуре Ta const ). После этого газ поступает в цилиндр второй ступени, где по политропе b c сжимается до давления pIII p2 . Далее следует охлаждение по изобаре pIII const в холодильнике II (между второй и третьей ступенью) до температуры Ta . Затем газ с параметрами pIII p2 и Ta поступает в цилиндр третьей ступени, где по политропе d 2 сжимается до нужного давления p p3 . Рисунок 2 Процесс сжатия в трехступенчатом компрессоре в координатах t s Это полнотекстовый пример работы, выполненной специалистами www.MagazinZnaniy.ru 13 Задача №3 Расчёт параметров воздушной холодильной машины Воздушная холодильная установка производит лед при температуре t Л 4 C из воды с температурой t В 8 C . Всасываемый в компрессор воздух имеет температуру t1 13 C , давление p1 96 кПа и сжимается до давления p2 420 кПа . Затем воздух поступает в холодильник и там охлаждается до t3 . Расход воздуха V 650 м 3 час при нормальных условиях. Принять: теплоемкость воды c p 4,187 кДж кг ; теплоту плавления льда q2 330,7 кДж кг ; теплоемкость льда cЛ 2,09 кДж кг . Определить: холодильный коэффициент установки ; мощность привода компрессора установки N ; количество получаемого установкой в час льда m . Дано : t Л 4 C t В 8 C t1 13 C p1 96 кПа p2 420 кПа V 650 м 3 ч c p 4,187 кДж кг q2 330,7 кДж кг cЛ 2,09 кДж кг Найти : ? N ? m? Решение: 1 Определяем температуру воздуха после сжатия в компрессоре (сжатие адиабатное): p T2 T1 2 p1 k 1 k 1, 41 420 103 1, 4 13 273 396,4 К . 3 96 10 Температура воздуха T4 после расширения в цилиндре детандера (расширительного цилиндра) равна: Это полнотекстовый пример работы, выполненной специалистами www.MagazinZnaniy.ru 14 T T4 T3 1 . T2 Так как температура t3 не задана, то принимаем ее равной t3 20 или T3 20 273 293 К . Тогда температура воздуха T4 равна: 13 237 T4 293 192,2 К . 396,4 2 Для того чтобы 1 кг воды с температурой t В 8 C превратить в лед с температурой t Л 4 C необходимо отнять от нее некоторое количество теплоты равное qВ q1 q2 q3 , где q1 cВ t В t0 4,187 8 0 33,496 кДж кг – теплота, идущая на охлаждение воды от 8 C до 0 C ; q2 330,7 кДж кг – теплота плавления льда; q3 cЛ t0 t Л 2,09 0 4 8,36 кДж кг – теплота отнимаемая для того, чтобы понизить температуру льда от 0 C до 4 C . Тогда общее количество теплоты, которое необходимо отнять у воды, равно: qВ 33,496 330,7 8,36 372,56 кДж кг . 3 Холодопроизводительность воздуха равна: Q0 V cp T1 T4 650 1,297 260 192,2 57159 кДж ч 57 МДж ч , где cp 1,297 кДж – объемная теплоемкость воздуха. м3 К Количество получаемого установкой льда в час равно: m Q0 57159 153,4 кг ч . q В 372,56 Холодильный коэффициент установки равен: 13 273 1,9 . T1 T2 T1 396,4 13 273 Работа цикла холодильной установки равна: L Q0 57 30 МДж ч . 1,9 Мощность привода компрессора установки равна: N Ответ: L 30 103 8,33 кВт . 3600 3600 1,9 ; Это полнотекстовый пример работы, выполненной специалистами www.MagazinZnaniy.ru 15 N 8,33 кВт ; m 153,4 кг ч . Список литературы 1 Кудинов В.А., Карташов Э.М. Техническая термодинамика. Учеб. пособие для вузов. М.: Высш. шк., 2000. – 261 с., ил. 2 Панкратов Г.П. Сборник задач по теплотехнике: Учеб. пособие для неэнергетич. спец. Вузов. – 2-е изд., перераб. и доп. – М.: Высш. шк. 1986. – 248 с., ил. 3 Рабинович О.М. Сборник задач по технической термодинамике. М.: «Машиностроение», 1973. – 344 с. Это полнотекстовый пример работы, выполненной специалистами www.MagazinZnaniy.ru