ПАТОГЕНЕТИчЕСкИЕ МЕхАНИзМЫ УчАСТИЯ
реклама

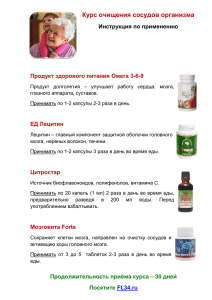
Погляд на проблему Е.В. Лекомцева Институт неврологии, психиатрии и наркологии, Харьков Ключевые слова: гиппокампальная формация, стриарный комплекс, порог электросудорожной готовности, электроэнцефалография, эстрогены, прогестерон. Патогенетические механизмы участия гиппокампальной формации и стриарного комплекса при нарушениях центральной нейроэндокринной регуляции Резюме. В работе представлено теоретическое обобщение клинико-экспериментальных данных относительно функционального состояния головного мозга в зависимости от гормонального профиля системы гипофиз — гонады, молекулярно-клеточных механизмов действия половых стероидных гормонов, взаимосвязи динамики гормонального спектра и биоэлектрической активности мозга (преимущественно у больных с катамениальной эпилепсией). Изложены данные о механизмах участия гиппокампа, миндалевидного тела, стриарного комплекса в центральной регуляции нейроэндокринной функции и модуляции биоэлектрической активности головного мозга в норме и при патологии. ВВЕДЕНИЕ Интерес к изучению нейроэндокринных рас­ стройств обусловлен высокой частотой поражения эндокринной системы и негативным влиянием гормональных нарушений на течение любой невро­ логической патологии. По сложности функциональной организации и многообразию функций эндокринную систему сравнивают с нервной, а патологию центральной нервной и эндокринной систем большинство ис­ следователей рассматривает как патологию единой функциональной нейроэндокринной системы, отражающей различные сигналы внешней и внут­ ренней среды. Наибольший интерес представляет изучение электроэнцефалографических особенностей функ­ ционального состояния головного мозга в зависи­ мости от гормонального профиля, так как изучение взаимосвязи гормонального спектра и биоэлектри­ ческой активности мозга позволяет выйти на новый уровень патогенетической коррекции пароксиз­ мальной активности и определить ведущие клини­ ко-патогенетические механизмы участия нейро­ стриатума, гиппокампальной формации и лимбикоретикулярного комплекса в центральной регуляции нейроэндокринной функции. Анализ литературных данных зарубежных и отечественных авторов (������� Herzog� ����� A���� .��� G��. ��� et� ����� al��� ., ������ 1982; ��� Bi­ lo� ��� L�� ���. ��� et� ����� al��� ., ������ 1988; ������ Мухин ������ К.Ю., ������ 1989; ������������� Rosciszewska� ���� D��� ., 1994; ��������� Cummings� ����� L���� .��� N��. ��� et� ����� al��� ., ������ 1995; ��������������� Волошин П.В. и соавт., 1996; �������� Morrell� ������ M����� .���� J��� ., ������ 1999) ������������������ и результаты собс­ твенного исследования (Григорова И.А. и соавт., 2003), которое было проведено на базе кафедры нервных болезней Харьковского государственного медицинского университета (2001–2005 гг.), позво­ лили выявить, что у больных ������������������������� ����������������� неврологического профиля нарушение функционального состояния системы гипофиз — гонады является одним из наи­ более частых сопутствующих параневрологических нейроэндокринных осложнений. Цель работы — обобщить результаты исследований особенностей биоэлектрической активности мозга в зависимости от разного гормонального профиля половых стеро­ идных гормонов, а также данные о молекулярноклеточных механизмах действия овариальных сте­ роидов и их влиянии на неспецифические структу­ ры мозга — гипоталамус, гиппокамп, мин­далевидное тело (амигдалу), нейростриатум, лимбико-ретику­ лярный комплекс. ГОРМОНАЛЬНЫЙ СТАТУС И ПАТОЛОГИЯ НЕРВНОЙ СИСТЕМЫ Механизмы участия стриатума, лимбико-рети­ кулярного комплекса, таламуса, гипоталамуса, эпифиза, гиппокампа, ретикулярной формации среднего мозга в центральной регуляции нейроэн­ докринной функции половых желез привлекали и привлекают многих исследователей. При ряде за­ болеваний (катамениальная (менструальная) эпи­ лепсия, катамениальная мигренозная цефалгия; український м е д и ч н и й ч асо п и с – № 2 ( 5 2 ) – I І I / I V 2 0 0 6 57 п о гл я д н а п роблему альгоменорея и вторичная аменорея центрального генеза; пароксизмальные болевые состояния, вклю­ чающие тригеминальную невралгию; вегетативнососудистые пароксизмы) возникновение и/или частота и тяжесть клинических проявлений четко приурочены к овариальному циклу. Деятельность половых желез регулируется выс­ шими структурами головного мозга — медиобазаль­ ными отделами височных и лобных долей, амигда­ лой и гиппокампом через лимбическую систему и ретикулярную формацию ствола мозга. Возникно­ вение аномальной активности в ней­рональной де­ ятельности (преимущественно эпилептиформного генеза — 78,5% случаев) сопро­вождается наруше­ нием интегративных связей, обеспечивающих нормальное функционирование нейроэндокринной системы. Формируются новые, отсутствующие в норме отношения, что ведет к нарушению регуля­ ции мозгом деятельности гонад. Изменение гормо­ нальной активности последних играет, в свою очередь, определенную роль в поломке механизмов, обеспечивающих нормальный гомеостаз мозга и оптимальный уровень реактивности нервной сис­ темы (�������� Hopkins� ���� A��� ., ������ 1987; ������� Карлов В.А., ������ ������������� Власов П.Н., 1997; Рыбникова Е.А. и соавт., 1999; Темин П.А., Никанорова М.Ю., 1999). В неврологии одним из самых ярких примеров зависимости возникновения заболевания от перио­ дичности колебания гормонального статуса явля­ ется катамениальная эпилепсия у женщин. Боль­ шинство ученых рассматривают катамениальную эпилепсию как эпилепсию, связанную с различны­ ми фазами овариального цикла, и выделяют три пика повышения частоты эпилептических парок­ сизмов согласно колебаниям уровней овариальных стероидов — эстрогенов и прогестерона (Кар­ лов В.А., Власов П.Н., 1997; Herzog� ������� A���� ����� .��� G��. ��� et� ����� al��� ., ������ 1997; Бадалян Л.О. и соавт., 1998; �������� Morrell� ������ M����� .���� J��� ., ������ 1999) ���� (ри­ сунок). Данное определение катамениальных эпи­ лептических приступов подразумевает возможность выделения припадков, возникающих за 1–2 дня до menses��������������������������������������� , припадков, возникающих исключительно в этот период и припадков, учащающихся в середи­ не овариального цикла. Данные проведенных со­ временных эпидемиологических исследований демонстрируют три достоверных пика повышения частоты катамениальных пароксизмов: первый и второй соответственно в начале и во время цикла, третий — в середине эстрогенового цикла (в пре­ овуляторном периоде). Отсутствие менструаций более шести месяцев называют аменореей. Синдром функциональной гипоталамической аменореи является примером вызванного стрессом нарушения нейроэндокринной функции гонад и служит моделью предполагаемой активации лимбической системы мозга и ее воздейс­ твия на репродукцию и эндокринную среду.� Понятие катамениальной мигренозной це­ фалгии как синдрома включает дебют мигрени в период менархе, обострение болезни (учащение мигренозных пароксизмов) в менструальный пери­ од, лучшую диагностическую эффективность об­ зорной электроэнцефалографии (ЭЭГ) для выявле­ ния составляющих феноменов пароксизмального характера и спектрально-когерентного анализа в период ����������������������������������������� menses����������������������������������� , относительно низкий уровень акти­ вации коры (Лейкок Д.Ф., Вайс П.Г., 2000). В зави­ симости от фаз овариального цикла изменяется спектр мощности ритмов ЭЭГ у этих пациентов. Общая динамика фоновой активности в группе данных пациентов характеризуется уменьшением суммарной мощности ритмов от 1–7 дней фолли­ кулярной фазы цикла к 21-му дню лютеиновой фазы овариального цикла (������������ Silberstein� S���� ����� .��� D��. et� ��� al��� ����� ., 2001). ������� Патогенез гормональнозависимых приступов до конца не изучен. Существует несколько точек зре­ ния на нейропатофизиологию катамениальных пароксизмов. Установлено, что физиологические колебания эндокринной секреции гонад в течение овариального цикла (см. рисунок) влияют на при­ падки — их частота самая низкая в лютеиновой фазе и наиболее высокая в фолликулярной фазе цикла. Прогестерон Эстрадиол Рисунок. Колебания уровней половых стероидных гормонов плазмы крови у здоровых женщин (������ n����� =20, ���������������� средний возраст �� — ��������� 23,5±2,1 ������ года) ����������������������� в течение овариального цикла: первые 4–6 дней соответствуют menses�� ��������; 6–14-й ������������������������� дни соответствуют фолликулярной �������������� фазе ������������ цикла, 14–15-й ������������ дни — �� овуляции, ���������� 16–28/30-й ��������������� дни — �� лютеиновой ����������� фазе овариального цикла женщины (данные von Egiluis� ���� �������� L���� ����� .��� H��. Spierings�� �����������, 2002) ������ 58 у к ра ї н с ь к и й м е д и ч н и й ч асо п и с – № 2 ( 5 2 ) – I І I / I V 2 0 0 6 Погляд на проблему Первая (фолликулярная) фаза соответствует быст­ рому снижению концентрации в крови прогестеро­ на (в перименструальный период и/или непосред­ ственно перед ���������������������������������� menses���������������������������� ), который обладает антикон­ вульсогенным действием (десинхронизирующим влиянием на биоэлектрическую активность мозга), и повышению концентрации в крови эстрадиола (до овуляции), обладающего проконвульсивным (синхронизирующим) действием. В овуляцию час­ тота пароксизмов статистически значимо кор­ релирует с эстрадиол/прогестероновым коэффици­ ентом. Эстрадиол/прогестероновое отношение наиболее высокое до овуляции и также в перименс­ труальный период и наиболее низкое в раннюю и среднюю лютеиновые фазы; однако недостаточ­ ность лютеиновой фазы с низкой секрецией про­ гестерона приводит к повышению эстрадиол/про­ гестеронового коэффициента сыворотки крови и появлению и/или учащению пароксизмов даже в лютеиновой фазе (���������� Backstrom� ���� T��� ., ����������� Zetterlund� ���� B��� ., ������ 1982; Herzog� A���� ����� .��� G��. et� ��� al��� ����� ., ������ 1982; ������ Klein� P��� ���� ., Herzog� ������� A����� ������ .���� G��� ., 1998; ������ Bonuccelli� ��� U��. ��� et� ����� al��� ., ������������������������������ 1989). В других работах такой четкой зависимости частоты приступов от эстради­ ол/прогестеронового коэффициента проследить не удалость. Например, при изучении динамики трех фракций эстрогенов и метаболизма прогестерона у больных с катамениальной эпилепсией была отмечена связь припадков только с уровнем прогестерона. Анализу были подвергнуты как катамениальные, так и нека­ тамениальные приступы. Клинические наблюдения отметили снижение частоты припадков на 22-й день, соответствующий максимальной концентрации прогестерона сыворотки крови. Минимальное число припадков на этот день было отмечено как при ка­ тамениальной, так и при некатамениальной эпилеп­ сии (������������� Rosciszewska� ���� D��� ., ������������������������������ 1994). С другой стороны, изме­ нение частоты катамениальных эпилептических припадков возможно за счет снижения в сыворотке крови содержания противоэпилептических препа­ ратов, которые, как и половые стероиды, метаболи­ зируются той же микросомальной системой печени. Перименструальное снижение секреции половых гормонов позволяет увеличивать метаболизм анти­ конвульсантов, следствием чего является снижение их концентрации в крови (������� Herzog� ����� A���� .��� G��. ��� et� ����� ����� al��� ., ������ 1984; Hopkins� A��� ���� ., 1987; ������ Зенков ������������� Л.Р., 2002). ������� Изменение функциональной активности нейро­ эндокринной системы может возникнуть под воз­ действием различных стрессорных факторов (Кры­ жановский Г.Н., Глебов Р.Н., 1984): как нарушение центральной регуляции вегетативных функций лим­ бико-ретикулярного комплекса при вовлечении в патологический процесс лимбической системы моз­ га (Темин П.А., Никанорова М.Ю., 1999; Григоро­ва И.А. и соавт., 2003��) ����������������������� и в результате длитель­ но проводимой медикаментозной терапии (������� Herzog� ����� A���� .��� G��. ��� et� ����� al��� ., ������ 1984; �������� Hopkins� ���� ���� A��� ., ������ 1987; ����� Bilo� ��� ��� L��. et� al��� ����� ., 1988; ������ Cummings� ��������� L���� ����� .��� N��. et� ��� ����� al��� ����� ., 1995; ������ Зенков Л.Р., ������������� 2002��� ). Показано наличие большого количества рецеп­ торов половых гормонов в головном мозгу, и это позволяет предположить, что мозг является одним из органов-мишеней половых стероидов. Много­ численными экспериментальными исследованиями показано, что специфические внутриклеточные цитозольные рецепторы для эстрадиола находятся в гипофизе, гипоталамусе, гиппокампе, коре голов­ ного мозга и в подкорковых лимбических структу­ рах (�������� Weiland� N����� ������ .���� G��� ., ������ 1992; ������� Murphy� D���� ����� .��� D��. ��� et� ����� al��� ., ������ 1998; Дудкин А.О., Сбитнев В.И., 2000; Сельянов А.В., Годухин О.В., 2001; ������� McEwen� ���� B��� ., ������������������� 2002). Регионарное распределение и аккумуляция рецепторов прогес­ терона следующие: средний мозг, амигдала, а затем по убывающей — гипоталамус, кора и гиппокамп. Получены результаты, выявившие принципиально два разных вида прогестерон-рецептивных сис­ тем — в среднем мозгу и коре количество прогесте­ роновых рецепторов всегда постоянно, а в преоп­ тическом поле гипоталамуса и гипофизе количест­ во рецепторов может изменяться, особенно после системного назначения эстрадиола (�������� Weiland� ������ N����� .���� G��� ., 1992; Wang� ����� Q��� ���� ., 2000). ������� Используя хронически имплантированные элек­ троды, ��� S��. ����������� ����������� Grahnstedt��� �� и ��� B��. ����������������� ����������������� Ellertsen�������� (1984) ��������� показали циклически меняющуюся возбудимость определен­ ных областей мозга половозрелых крыс, обуслов­ ленную изменением гормонального фона и корре­ лирующую со стадией эстрального цикла. Так, порог возбудимости дорсальной части гиппокампа снижался в период проэструса и частично эструса. Активность гиппокампальной коры в 1-й фоллику­ лярной фазе (соответствующей гиперэстрогенемии) овариального цикла была представлена появлением «спайкового сложения» в виде острых колебаний на вершинах суммарных постсинаптических потен­ циалов, которые обусловлены гиперактивной реак­ цией нейрональной системы гиппокампа, поддер­ живаемой гуморальными агентами. При частоте 10 Гц «спайковое сложение» переходило в самопод­ держивающийся эпилептический послеразряд. Порог возбудимости дорсальной части гиппокампа повышался во время диэструса с последующим повторением цикла. Сходный паттерн активности проявляла медиальная часть амигдалы: порог воз­ будимости снижался также во время преобладания концентрации эстрогенов и повышался в период наиболее низкого уровня эстрогенов. В латеральной части амигдалы электрическая активность была противоположной. Таким образом, между латераль­ ной частью амигдалы, с одной стороны, и дорсаль­ ной частью гиппокампа, медиальной частью амигдалы — с другой существуют реципрокные отношения, обусловленные изменением концент­ рации женских половых гормонов. Таким образом, цикличность секреции половых стероидов соответс­ твует цикличности биоэлектрической активности гиппокампа и амигдалы, что также связано с сексу­ альным поведением. український м е д и ч н и й ч асо п и с – № 2 ( 5 2 ) – I І I / I V 2 0 0 6 59 п о гл я д н а п роблему Действие стероидных женских половых гормо­ нов исследовалось в различных модификациях опытов: при местном применении, при системном назначении, на различных биологических моделях. Однако патогенетические механизмы влияния по­ ловых стероидных гормонов на биоэлектрическую и судорожную активность головного мозга изучены недостаточно. Установлено, что половые стероидные гор­ моны — эстрогены (главным образом эстрадиол, эстрон, эстриол), прогестерон, тестостерон — поразному влияют на порог электросудорожной го­ товности головного мозга (Крыжановский Г.Н., Глебов Р.Н. 1984; ����� Wang� Q��� ���� ., ������������������������ 2000). Они могут влиять на судорожную активность головного мозга путем нарушения ионной проницаемости мембран ней­ ронов с последующим изменением их биоэлектри­ ческой активности и изменяя внутриклеточный нейрональный метаболизм. По данным экспериментальных исследований показано, что эстрадиол ингибирует гамма-амино­ масляную кислоту (ГАМК) и потенцирует глута­ матергическую трансмиссию, повышает нейрональ­ ный метаболизм и скорость деполяризации; эстра­ диол многократно повышает частоту синаптических связей в СА1-регионе гиппокампа у взрослых крыс; способствует созданию новых эпилептических фо­ кусов при аппликации на кору (�������� Weiland� N����� ������ .���� G��� ., ������ 1992; Murphy� ����� D���� .��� D��. ��� et� ����� al��� ., ������ 1998; ����� Wang� ���� ���� Q��� ., ������ 2000; ������� Rudick� ������ C����� .���� N��� ., Woolley� ������ C����� .���� S��� ., 2001; ������ ������� McEwen� ���� B��� ., ������������������� 2002). Прогестерон уменьшает нейрональный метаболизм и скорость деполяризации: в период диэструса, когда отмеча­ ется самый низкий уровень эстрогенов, порог электрошоковых судорог повышается. Прогестерон увеличивает порог электросудорожной готовности, подавляет возникно­вение эпилептической актив­ ности, вызванной киндлингом, фокальным повреж­ дением, вызывает седативный и анестетический эффекты у крыс (������������� Gra­hn­stedt� S��� ���� ., Ellertsen� ���������� ���� B��� ., ������ 1984; Fountain� N���� ����� .��� B��. et� ��� al��� ����� ., 1998; ������ Wang� ����� Q��� ���� ., 2000). ������ Конвульсогенный эффект эстрадиола был про­ демонстрирован в ряде экспериментальных иссле­ дований (������������� Rosciszewska� ��� D��. ������ 1994, ����� Zahn� ����� C���� .��� A��. ��� et� ����� al��� ., 1998). Согласно этим исследованиям повышение биоэлектрической активности головного мозга крыс происходит в полдень дня проэструса, что коррелирует с пиком выброса лютеинизирующего гормона и повышением уровня эстрадиола. Анало­ гичные результаты получили T�� ���. ������������ Backstrom��� ������������ и ��� B��. ���� ���� Zet­ terlund��������� (1982). В настоящее время также выполнено значитель­ ное количество экспериментальных исследований, в которых показан антиконвульсивный эффект прогестерона. Было обнаружено, что дозы прогес­ терона, превышающие его физиологический уро­ вень, предохраняют экспериментальных животных от развития судорог, вызванных электротоком (�������� Hopkins� A��� ���� ., 1987). ������� Другие исследователи провели эксперименталь­ ное исследование, где эпилепсия была смоделиро­ 60 вана посредством корковой аппликации пеницил­ лина. Задачей исследования являлось определение влияния прогестерона на судорожную готовность головного мозга животных и определение измене­ ний уровня гонадотропина и лютеинизирующего гормона в межприступный период. Ни у одного из неполовозрелых особей не наблюдалось тяжелых генерализованных судорожных приступов с паде­ нием. У половозрелых особей антиконвульсивный эффект был менее выражен (Шаляпина В.Г. и со­ авт., 1999). Дискутируются возможные механизмы проти­ восудорожного действия прогестерона. Было пред­ ложено несколько возможных механизмов его влияния на судорожную активность: а) блокирова­ ние восходящей ретикулярной формации ствола головного мозга; б) изменение внутринейронного метаболизма; в) дисбаланс нейротрансмиттеров (��������� Fountain� ����� N���� .��� B��. ��� et� ����� al��� ., ������ 1998; ����� Wang� ���� Q��� ., �������������� 2000). По мне­ нию других авторов одним из возможных механиз­ мов изменения порога судорожной готовности го­ ловного мозга при назначении половых стероидов может быть влияние на уровень глюкозы в мозгу (Крыжановский Г.Н., Глебов Р.Н., 1984; Кар­ лов В.А., Власов П.Н., 1997). Некоторые исследователи показали успешность применения прогестероновой терапии. Наиболее протестирован метапрогестеронацетат (�������������� Mattson������� ������ R����� .���� H��� ., Cramer� ������ J����� .���� A��� ., ������ 1985; ����� Bilo� ��� L��. ��� et� ����� al��� ., ������ 1988; ������������� Лейкок Д.Ф., Вайс П.Г., 2000). Считается, что прогестерон может снижать частоту припадков за счет подавления выработки гонадотропинов, тем самым снижая уровень эстрогенов. Показано, что дериваты про­ гестерона, не имеющие гормональной активности, такие как аллопрегнанолон (������������������ allopregnanolone��, 3�������������������������������������������������� alpha��������������������������������������������� ,5������������������������������������������� alpha�������������������������������������� -������������������������������������� Tetrahydroprogesterone��������������� ), оказывают в десятки раз более выраженное противосудорожное действие (������� Rhodes� M���� ����� .��� E��. et� ��� al��� ����� ., 2004). ������� Корковые аппликации препарата конъюгиро­ ванных эстрогенов в разных концентрациях приво­ дили к появлению пик-волновой активности с частотой 2,5–4,0 Гц или вызывали полипиковую активность на ЭЭГ. В настоящее время такая ап­ пликация является одной из распространенных моделей эпилепсии и используется для изучения эффективности и тестирования различных групп противоэпилептических препаратов (��������� Nissinen� ��� J��. et� ������ al���� ������ ., 2000; ������ Rudick� ������� C����� ������ .���� N��� ., Woolley� �������� C����� ������ .���� S��� ., 2001). ������� Функциональное состояние головного мозга в зависимости от гормонального профиля Электроэнцефалографическое исследование до настоящего времени остается наиболее специфич­ ным и адекватным методом выявления эпилепти­ ческой активности и нейрофизиологических пара­ метров деятельности головного мозга. На сегодняшний день существует значительное количество исследований, свидетельствующих о различиях биоэлектрической активности головно­ у к ра ї н с ь к и й м е д и ч н и й ч асо п и с – № 2 ( 5 2 ) – I І I / I V 2 0 0 6 Погляд на проблему го мозга у мужчин и женщин. Косвенным доказа­ тельством различного влияния мужских и женских половых гормонов на судорожную активность го­ ловного мозга являются четкие различия ЭЭГ у мужчин и женщин. Показано, что у женщин наблю­ дается более высокая представленность бета(β)активности по сравнению с мужчинами во всех возрастных группах. У женщин на ЭЭГ наблюдает­ ся бóльшая амплитуда и количество β-волн меньше, чем у мужчин, представительство альфа(α)- и тета(θ)-волн, большая тенденция к десинхрониза­ ции ритма (������������� Rosciszewska� D��� ���� ., ������ 1994; ������� Карлов ������ В.А., Власов П.Н., 1997; Зенков Л.Р., 2002; Tettenborn� ����������� B�� ���. et� al��� ����� ., 2002; ������ Григорова ������������������������� И.А. и соавт., 2003). ������� Неоднозначны результаты авторов по ЭЭГ-ис­ следованиям влияния фаз овариального цикла на их параметры. Одни авторы описывали повышение частоты α-ритма в лютеиновой фазе овариального цикла и снижение частоты доминирующего α-рит­ ма во время овуляции (������� Herzog� A���� ����� .��� G��. et� ��� al��� ����� ., ������ 1997; ��� Ба­ далян Л.О. и соавт., 1998; �������� Morrell� ������ M����� .���� J��� ., ����������� 1999), дру­ гими исследователями циклически медленный фон в овуляторный период подтвержден не был (���� Hop­ kins� ���� A��� ���� ., 1987; ������ Tettenborn� ����������� B�� ���. et� ��� al��� ����� ., 2002). ������� Наиболее четкие различия выявлены при ана­ лизе амплитуды основных корковых ритмов: боль­ шинство исследователей отмечают редукцию амп­ литуды α-ритма в предменструальные дни и менс­ труальный период. У здоровых женщин на 21-й день овариального цикла выявляется повышение мощ­ ности α-ритма, уменьшение межполушарной асим­ метрии, снижение мощности низкочастотных со­ ставляющих спектра и минимального прироста мощности при гипервентиляции по всем частотным диапазонам, что свидетельствует о стабильной ней­ родинамике (�������� Morrell� M����� ������ .���� J��� ., 1999). ������� Исследования, основанные на большом количес­ тве наблюдений, убедительно свидетельствуют о наличии половых различий ЭЭГ у больных эпилеп­ сией. Возможно, одной из причин более частых па­ тологических изменений ЭЭГ у женщин является высокое содержание в их организме эстрогенов. Влияние экзогенного введения женских половых гормонов на судорожную активность головного мозга исследовано достаточно давно. Так, J�� ���. ����� Logo­ ����� thetis��������������������� и соавторами (1959) было ��������������������� установлено кон­ вульсогенное действие препарата конъюгированных эстрогенов (���������� Premarin��) ���������������������������� и предложено его применение для выявления скрытой эпилептической активнос­ ти в стационарных условиях (цит. по: Мухин К.Ю., 1989). Также изучали влияние эстроген/прогестинсодержащих препаратов на параметры ЭЭГ у здо­ ровых людей. При их применении на ЭЭГ регист­ рируются: медленноволновая активность амплиту­ дой около 100 мВ, чаще во фронтальной и париетальной областях; пароксизмальная актив­ ность в височной области; повышение частоты пиков α-ритма; медленный θ-ритм и δ-активность (Мухин К.Ю., 1989). Антиконвульсивный эффект прогестерона был продемонстрирован T�� ���. ����������������������� Backstrom�������������� ����������������������� и соавторами (1984), которые назначали прогестерон внутривен­ но капельно женщинам с парциальной эпилепсией. На фоне введения прогестерона у 4 из 7 больных частота эпилептических комплексов значительно редуцировалась. Протективные свойства прогестерона в отноше­ нии судорог показаны и в экспериментальных ис­ следованиях. Прогестерон хорошо проникает через гемато-энцефалический барьер и обнаруживается через несколько минут в тканях мозга после внут­ ривенного введения, быстро и значительно по­ вышая порог электрошоковых судорог. После внутривенного введения прогестерон подавлял интериктальную спайковую активность корковопенициллинового очага на 50% по сравнению с контролем (���������� Backstrom� ���� T��� ., ����������� Zetterlund� ���� B��� ., ������ 1982; Klein� ���� P��� ���� ., Herzog� ������� A����� ������ .���� G��� ., 1998; ������ Bauer� ������ J�� ���. 2001). ������� Другие исследования влияния фаз овариального цикла на параметры ЭЭГ у здоровых женщин отме­ тили только легкое повышение частоты α-ритма в лютеиновой фазе (Крыжановский Г.Н., Глебов Р.Н., 1984; ����� Zahn� ����� C���� .��� A��. ��� et� ����� al��� ., ������������������������� 1998). При сопоставлении данных ЭЭГ с концентрацией прогестерона в плаз­ ме крови был выявлен определенный параллелизм между повышением концентрации гестагенов и учащением α-ритма; частота же β-ритма на протя­ жении всего овариального цикла оставалась ста­ бильной. Исследование, включавшее наблюдения молодых женщин (средний возраст — 24,3±4,6 лет), отметило преобладающую частоту α-ритма в пред­ менструальные дни (за 3 дня до наступления men­ ���� ses��) — �� 11 ����������������������������������������� Гц, а в овуляторный период регистриро­ вался α-ритм с преимущественной частотой 9–10 Гц. Также в предменструальные дни и период menses������������������������������������������� была отмечена редукция амплитуды α-ритма. Кроме того, в предменструальный период была более выраженная θ-активность и появление па­ роксизмальной активности, значительно усиливаю­ щейся на фотостимуляцию (Карлов В.А., Вла­ сов П.Н., 1997). Исследование влияния фаз овариального цикла на параметры ЭЭГ у женщин с эпилепсией выяви­ ло, что наиболее выраженная степень эпилептичес­ кой активности наблюдалась на протяжении фол­ ликулярной фазы овариального цикла, а наличие выраженных амплитудно-частотных изменений пароксизмальной активности в фолликулярной фазе овариального цикла дают возможность реко­ мендовать проведение электроэнцефалографичес­ кого обследования для диагностики эпилепсии у женщин в фолликулярной фазе цикла, что соответс­ твует 7–8-му дню овариального цикла (Григоро­ ва И.А. и соавт., 2003). У больных с вторичной олиго-, аменореей цен­ трального генеза выявлены следующие особеннос­ ти изменения биоэлектрической активности голов­ ного мозга. На ЭЭГ нередко фиксировались изме­ нения эпилептиформного характера. Признаки український м е д и ч н и й ч асо п и с – № 2 ( 5 2 ) – I І I / I V 2 0 0 6 61 п о гл я д н а п роблему повышения активности глубоких структур мозга в виде генерализации α-активности и стертости зо­ нальных различий, доминирование α-ритма в те­ менной области, вспышек билатеральных синхро­ низированных биопотенциалов, чаще в передних отделах, пароксизмальной генерализованной ак­ тивности. Данные частотного анализа относитель­ но большей синхронизации α-ритма справа свиде­ тельствуют о доминирующей роли правого полуша­ рия в реализации таламокортикальных влияний (�������� Hopkins� ���� A��� ., ������ 1987; Лейкок ������������� Д.Ф., Вайс ����������� П.Г., 2000; ������ McEwen� B��� ���� ., 2002). ������ Доминирование правого полушария у больных с нарушениями овариальной функции центрально­ го генеза не случайно, так как имеется предполо­ жение о значении межполушарной асимметрии мозга в генезе нейроэндокринных расстройств и роли правого полушария в специфической нейро­ секреции (Бадалян Л.О. и соавт., 1998). Широкое распространение в связи с развитием компьютерной техники и внедрением методов кор­ реляционного анализа в современных нейрофи­зио­ логических и нейропсихологических работах по­ лучило измерение статистической связи между колебаниями биопотенциалов, протекающих в раз­ личных отделах головного мозга, с помощью вы­ числения когерентности ЭЭГ. На сегодняшний день анализ пространственной организации потенциа­ лов мозга является стандартом диагностики при дифференциации различных патологических со­ стояний головного мозга. Нарастание мощности — это прямое следствие синхронизации работы ней­ ронов мозга, и является генетически детерминиро­ ванной фенотипической предосновой развития заболевания по эпилептическому типу. На ЭЭГ синхронизация проявляется высокоамплитудной, низкочастотной ритмичной билатерально-синхрон­ ной активностью. Такая синхронизированная ак­ тивность соответствует меньшей информационной содержательности процессов мозга, характерной для сна без сновидений, наркоза или глубокой комы. Снижение уровня функциональной актив­ ности сопровождается сокращением афферентного притока и большей зависимостью организации нейронной активности мозга от эндогенных меха­ низмов (Зенков Л.Р., 2002). В стволе, диэнцефальной и лимбической сис­ темах имеются ядра, активация которых приводит к изменению функциональной активности практи­ чески всего мозга. Среди этих систем выделяют так называемые восходящие, активирующие системы, расположенные на уровне ретикулярной формации среднего и преоптических ядрах переднего мозга, или тормозящие, сомногенные системы, располо­ женные главным образом в неспецифических та­ ламических ядрах, в нижних отделах моста и про­ долговатом мозгу. Возбуждение активирующих ретикуло-кортикальных систем приводит к десин­ хронизации, которая на ЭЭГ проявляется высоко­ частотной и низкоамплитудной активностью (Ба­ 62 далян Л.О. и соавт., 1998; Дудкин А.О., Сбит­ нев В.И., 2000). Описанные выше межнейрональные взаимо­ действия непосредственно реализуются синапти­ ческими нейротрансмиттерными системами. Осо­ бое значение придается ГАМК-эргическим тормоз­ ным системам, которые рассматриваются как один из основных механизмов препятствия переходу мозга на эпилептический режим работы. Важней­ шая роль здесь принадлежит неспецифическим лимбико-ретикулярным структурам, содержащим на всех уровнях ядра с активными тормозными механизмами и ГАМК-чувствительными рецепто­ рами. Эстрадиол оказывает непосредственное влияние на процессы возбуждения мембраны ГАМК-рецептора типа ������� A������ (ГАМКА). Когда эстради­ ол связывается с распознавательным сайтом ГАМКА-рецептора, он нарушает его хлоридную проводимость, вследствие чего ГАМК-потенциро­ ванное ингибирование рецептора становится менее эффективным. Прогестерон оказывает противопо­ ложное действие на ГАМКА-рецептор (�������� Morrell� M����� ������ .���� J��� ., 1999). Другим фактором, определяющим преимущес­ твенность того или иного реагирования различных отделов мозга на воздействие эпилептогенного фактора, является их разная эпилептическая готов­ ность. В экспериментальной нейрофизиологии используется понятие порога судорожной готовнос­ ти. Так, мозжечок имеет наиболее высокий порог судорожной готовности, так же, как и стриарный комплекс, в то время как ������������������������ у сенсомоторной коры он относительно более низкий. Самый низкий порог судорожной готовности имеют образования гиппо­ кампальной формации, активность которой пере­ дается через таламические и септальные ядра и оттуда обратно в гиппокамп; при этом в процесс возбуждения вовлекаются гиппокамп и лимбичес­ кие образования противоположной стороны (Зен­ ков Л.Р., 2002). В гиппокамп проецируется вся медиальная кора, височная конвекситальная кора, обонятельные системы, включая миндалевидное тело, интраламинарные и ростральные ядра тала­ муса, боковое коленчатое тело, ядра шва моста и среднего мозга. В свою очередь гиппокамп проеци­ руется в преоптическую кору, гипоталамические неспецифические ядра, продольный пучок средне­ го мозга, лобную кору, ядра перегородки. ЗАКЛЮЧЕНИЕ На основе изложенных выше клинико-экспе­ риментальных данных возможна разработка моде­ ли возникновения катамениальнозависимых паро­ ксизмов. Группа больных с катамениальной эпи­ лепсией, катамениальной мигренью, аменореей, вегетативно-сосудистой дистонией нозологически неспецифична, однако имеет определенные кли­ нико-нейрофизиологические характери­стики. Доказано альтернативное ��������������������������������� влияние и высокое сродство половых стероидов — эстрадиола и про­ у к ра ї н с ь к и й м е д и ч н и й ч асо п и с – № 2 ( 5 2 ) – I І I / I V 2 0 0 6 Погляд на проблему гестерона — к коре головного мозга, эпилептичес­ кому очагу, потенциально эпилептогенным облас­ тям мозга (гиппокампу и амигдале), а также неспе­ цифическим структурам мозга. Предположение об активирующем влиянии эстрадиола на неспецифи­ ческие системы основано на экспериментальных данных, свидетельствующих о большом количестве цитозольных гормональных рецепторов в стволовых структурах, а также об учащении доминирующего α-ритма в лютеиновой фазе овариального цикла. Влияние половых стероидов на активирующие системы также предполагается на том основании, что в эту систему входят стволовые и гипоталами­ ческие структуры, такие как каудальное ретикуляр­ ное ядро моста и латеральное ядро гипоталамуса. Припадок реализуется в результате взаимодействия сомногенных, восходящих ретикуло-кортикальных систем и неспецифических систем мозга, на кото­ рые половые стероидные гормоны оказывают мо­ дулирующие влияние. Возможно, что становление катамениальных пароксизмов формируется на ос­ нове высокой наследственной отягощенности, а циклические проявления заболевания возникают в связи с функционированием системы гипо­та­ла­ мус — гипофиз — гонады. Введение в клиническую практику радиоимму­ нологических, биохимических, гистологических методов исследования позволило детально изучить метаболизм гормонов, определить интимные меха­ низмы, лежащие в основе нейроэндокринных рас­ стройств. Эстрогены и прогестерон играют важную роль в деятельности и функциональной активности головного мозга, влияют на нейрональную актив­ ность его отдельных областей и участвуют в слож­ ных и многообразных отношениях преимуществен­ но лимбико-гипоталамической системы и гиппо­ кампа, амигдалы. Несмотря на многочисленные эксперименталь­ ные и клинические исследования, посвященные изучению функционального состояния гипофи­ зарно-гонадной системы, причины и механизм развития выявленных нарушений, характер эндо­ кринной дисфункции, ее взаимосвязь с течением неврологического заболевания окончательно не установлены. До настоящего времени не решен принципиаль­ но важный вопрос: возникают ли данные наруше­ ния нейроэндокринной функции первично, спо­ собствуя снижению порога судорожной готовности головного мозга, или они проявляются вторично, являясь следствием основного текущего патологи­ ческого процесса в центральной нервной системе. ЛИТЕРАТУРА Бадалян Л.О., Темин П.А., Аметов А.С., Мухин К. Ю. (1988) Дискуссионные вопросы проблемы менструальной эпилеп­ сии. Журн. невропатологии и психиатрии им. С.С. Корса­ кова, 88(6): 120–123. Волошин П.В., Мерцалов В.С., Волошина Н.П. (1996) Диагностика, лечение и реабилитация больных эпилепсией. Харьковский медицинский журнал, 3: 5–8. Григорова И.А., Дубенко Е.Г., Лекомцева Е.В. (2003) Особенности функционального состояния головного мозга в зависимости от гормонального профиля у больных эпи­ лепсией. Врачебная практика, 5: 80–85. Дудкин А.О., Сбитнев В.И. (2000) Спонтанные синхронные разряды в срезах гиппокампа. Биофизика, 45(1): 119–124. Зенков Л.Р. (2002) Клиническая эпилептология (с эле­ ментами нейрофизиологии). МИА, Москва, 416 с. Карлов В.А., Власов П.Н. (1997) Клинические, электро­ энцефалографические, гормональные особенности и терапия катамениальных эпилептических припадков. Неврологичес­ кий журнал, 4: 19–23. Крыжановский Г.Н., Глебов Р.Н. (1984) Гормоны и эпи­ лептическая активность. Журн. невропатологии и психиат­ рии им. С.С. Корсакова, 84(6): 930–937. Лейкок Д.Ф., Вайс П.Г. (2000) Основы эндокриноло­ гии (Пер. с англ.). Медицина, Москва, 501 с. Мухин К.Ю. (1989) Изменение функционального состоя­ ния гипофизарно-тестикулярной системы при эпилепсии. Дис. … канд. мед. наук: 14.00.13. М., 159 с. Рыбникова Е.А., Ракицкая В.В., Шаляпина В.Г. (1999) Учас­ тие стриатума в центральной регуляции гормональной функции гонад. Российский физиологический журнал, 85(4): 594–597. Сельянов А.В., Годухин О.В. (2001) Клеточно-молекуляр­ ные механизмы фокального эпилептогенеза. Успехи физио­ логических наук, 32(1): 60–78. Темин П.А., Никанорова М.Ю. (ред.) (1999) Эпилепсии и судорожные синдромы у детей. Руководство для врачей. Медицина, Москва, 656 с. Шаляпина В.Г., Вайдо А.И., Лопатина Н.Г. (1999) Изме­ нение секреции половых стероидных гормонов при стрессе у крыс с разной возбудимостью головного мозга. Российский� физиологический��������� журнал�� ��������, 85(1): ������� 1428–1433. ����������� Backstrom T., Zetterlund B. (1982) Pulsate secretion of LH, FSG, prolactin, estrogen and progesterone during the human menstrual cycle. Clinical Endocrinology, 18(1): 29–42. Backstrom T., Zetterlund B., Blom S., Romano M. (1984) Effects of intravenous progesterone infusions on the epileptic discharge frequency in women with partial epilepsy. Acta Neurol. Scand., 69(4): 240–248. Bauer J. (2001) Interactions between hormones and epilepsy in female patients. Epilepsia, 42 (Suppl. 3): 20–22. Bilo L., Meo R., Nappi C., Annunziato L., Striano S., Colao A.M., Merola B., Buscaino G.A. (1988) Reproductive en­ docrine disorders in women with primary generalized epilepsy. Epilepsia, 29(5): 612–619. Bonuccelli U., Melis G.B., Paoletti A.M., Fioretti P., Murri L., Muratorio A. (1989) Unbalanced progesterone and estradiol secre­ tion in catamenial epilepsy. Epilepsia, 3(2): 100–106. Cummings L.N., Guidice L., Morell M.J. (1995) Ovulatory function in epilepsy. Epilepsia, 36(4): 355–359. Fountain N.B., Bear J., Bertram E.H. 3rd, Lothman E.W. (1998) Responses of deep entorhinal cortex are epileptiform in an elec­ trogenic rat model of chronic temporal lobe epilepsy. J. Neuro­ physiol., 80(1): 230–240. Grahnstedt S., Ellertsen B. (1984) Brain state and kindled seizures. Exp. Neurol., 84(3): 596–605. Herzog A.G., Klein P., Ransil B.J. (1997) Three patterns of catamenial epilepsy. Epilepsia, 38(10): 1082–1088. Herzog A.G., Russell V., Vaitukaitis J.L., Geschwind N. (1982) Neuroendocrine dysfunction in temporal lobe epilepsy. Arch. Neurol., 39(3): 133–135. Herzog A.G., Seibel M.M., Schomer D., Vaitukaitis J., Geschwind N. (1984) Temporal lobe epilepsy: an extrahypothalamic pathogenesis for polycystic ovary syndrome? Neurology, 34(10): 1389–1393. Hopkins A. (1987) Epilepsy. Chapman and Hall, London, 585 p. Klein P., Herzog A.G. (1998) Hormonal effects on epilepsy in women. Epilepsia, 39(Suppl. 8): S9– S16. український м е д и ч н и й ч асо п и с – № 2 ( 5 2 ) – I І I / I V 2 0 0 6 63 п о гл я д н а п роблему Logothetis J., Harner R., Morrell F., Torres F. (1959) The role of estrogens in catamenial exacerbation of epilepsy. Neurology, 9(5): 352–360. Mattson R.H., Cramer J.A. (1985) Epilepsy, sex hormones, and antiepileptic drugs. Epilepsia, 26(Suppl. 1): S40–S51. McEwen B. (2002) Estrogen actions throughout the brain. Recent. Prog. Horm. Res., 57: 357–384. Morrell M.J. (1999) Epilepsy in women: the science of why it is special. Neurology, 53(4 Suppl. 1): S42–S48. Murphy D.D., Cole N.B., Greenberger V., Segal M. (1998) Estradiol increases dendritic spine density by reducing GABA neurotransmission in hippocampal neurons. J. Neurosci., 18(7): 2550–2559. Nissinen J., Halonen T., Koivisto E., Pitkanen A. (2000) A new model of chronic temporal lobe epilepsy induced by electrical stimu­ lation of the amygdala in rat. Epilepsy Res., 38(2–3): 177–205. Rhodes M.E., Harney J.P., Frye C.A. (2004) Gonadal, adre­ nal, and neuroactive steroids’ role in ictal activity. Brain Res., 1000(1–2): 8–18. Rosciszewska D. (1994) Epilepsy and the menstrual cycle. Pol. Tyg. Lek., 49(4–5): 99–101. Rudick C.N., Woolley C.S. (2001) Estrogen regulates func­ tional inhibition of hippocampal CA1 pyramidal cells in the adult female rat. J. Neurosci., 21(17): 6532–6543. Silberstein S.D., Lipton R.B., Dalessio D.J. (Eds.) (2001) Wolff’s headache and other head pain. Oxford University Press, 648 p. Tettenborn B., Genton P., Polson D. (2002) Epilepsy and wo­ men’s issues: an update. Epileptic Disord., 4(Suppl. 2): S23–S31. von Egiluis L.H. Spierings (2002) Migraine: questions and answers. Merit Publishing International, 124 p. Wang Q. (2000) The roles of estrogen and progestin in epilep­ togenesis and their mechanisms of action. Sheng Li Ke Xue Jin Zhan, 31(3): 231–233. Weiland N.G. (1992) Estradiol selectively regulates agonist bin­ ding sites on the N-methyl-D-aspartate receptor complex in the CA1 region of the hippocampus. Endocrinology, 131: 662–668. Zahn C.A., Morrell M.J., Collins S.D., Labiner D.M., Yerby M.S. (1998) Management issues for women with epilepsy: a review of the literature. Neurology, 51(4): 949–956. ПАТОГЕНЕТИЧНІ МЕХАНІЗМИ УЧАСТІ ГІПОКАМПАЛЬНОЇ ФОРМАЦІЇ ТА СТРІАРНОГО КОМПЛЕКСУ ПРИ ПОРУШЕННЯХ ЦЕНТРАЛЬНОЇ НЕЙРОЕНДОКРИННОЇ РЕГУЛЯЦІЇ Є.В. Лекомцева Резюме. У роботі представлено теоретичне узагальнення клініко-експериментальних даних щодо функціонального стану головного мозку залежно від гормонального профілю системи гіпофіз — гонади, молекулярно-клітинних механізмів дії статевих стероїдних гормонів, взаємозв’язку динаміки гормонального спектра та біоелектричної активності мозку (переважно у хворих із катаменіальною епілепсією). Наведено дані щодо механізмів участі гіпокампа, мигдалевидного тіла, стріарного комплексу у центральній регуляції нейроендокринної функції та модулюванні біоелектричної активності головного мозку в нормі та при патології. Ключові слова: гіпокампальна формація, стріар­ ний комплекс, поріг електросудомної готовності, електроенцефалографія, естрогени, прогесте­ рон. PATHOGENETIC MECHANISMS OF THE HIPPOCAMPAL FORMATION AND STRIATAL COMPLEX PARTICIPATION IN DISORDERS OF THE CENTRAL NEUROENDOCRINE REGULATION Ye.V. Lekomtseva Resume. Article represents theoretical generalization of clinical-experimental data on brain functional state depending on the hypophysis-gonadal system profile, as well as molecular-cellular mechanisms of the steroid sex hormones effect and interactions between the hormonal spectrum dynamics and bioelectric brain activi­ty (mainly in women with catamenial epilepsy). Data are also given on the mechanisms of the hippocampus, amygdala and striatal complex participation in the central neuroendocrine regulation and bioelectric brain activity modulation, both in normal and pathological conditions. Key words: hippocampus formation, striatum com­ plex, electroconvulsive threshold, electroencepha­ lography, estrogens, progesterone. Адрес для переписки: Лекомцева Евгения Владимировна 61064, Харьков, ул. Пермская, 9, кв. 53 E-mail: lekomtseva1@yandex.ru Реферативна інформація Ацетил-L-карнитин Acetyl-L-carnitine. Altern. Med. Rev., 1999, 4(6): 438–441 (http://www.thorne.com/altmedrev/ fulltext/4/6/438.pdf). Ацетил-L-карнитин — эфир триметилирован­ ной аминокислоты, L-карнитина —синтезируется в головном мозге, печени и почках человека при участии фермента ацетил-L-карнитин-трансфе­ разы. Ацетил-L-карнитин способствует поглощению ацетил-коА митохондриями в процессе окисления 64 жирных кислот, усиливает продукцию ацетилхо­ лина, а также стимулирует синтез протеинов и мембранных фосфолипидов. Ацетил-L-карнитин сходен по строению с ацетилхолином и также об­ ладает холиномиметическим эффектом. В иссле­ дованиях установлены терапевтические эффекты ацетил-L-карнитина при деменции альцгеймеров­ ского типа, депрессии в пожилом возрасте, ВИЧ-ин­фекции, диабетических нейропатиях, ишемии и реперфузии головного мозга, когнитив­ ных нарушениях при алкоголизме. у к ра ї н с ь к и й м е д и ч н и й ч асо п и с – № 2 ( 5 2 ) – I І I / I V 2 0 0 6