десорбция водных растворов солей на горизонтальной
Реклама

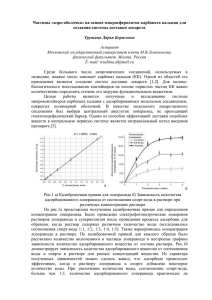
2. Скрипов В.П., СкриповА.В. Спинодальный распад (Фазовый переход с участием неустойчивых состояний) // УФН. – 1979. – Т. 128. – С. 193–231. 3. Хавкин А.Я. Перспективы создания газогидратной промышленности // Вестник российской академии естественных наук. – 2010. – Т. 1. – С. 42–45. 4. Groenveld Р. Взрывное парообразование // Труды американского общества инженеров-механиков (Русский перевод. Издательство Мир). – 1972. – №2. – С. 122–124. 5. Rausch А.Н. and Levine A.D. Rapid phase transformations caused by thermodynamic instability in cryogens // Cryogenics. – 1973. – Vol. 13. – № 4. – Р. 224–229. УДК 621.577 ДЕСОРБЦИЯ ВОДНЫХ РАСТВОРОВ СОЛЕЙ НА ГОРИЗОНТАЛЬНОЙ ПОВЕРХНОСТИ НАГРЕВА Накоряков В.Е., академик РАН, Елистратов С.Л., д.т.н., Мисюра С.Я. Институт теплофизики СО РАН, г. Новосибирск E-mail: nakve@itp.nsc.ru; elistratov@itp.nsc.ru; misura@itp.nsc.ru Ранее наибольшее внимание при усовершенствовании абсорбционных тепловых насосов уделялось процессам абсорбции. Однако, не менее важно точно рассчитывать десорбцию растворов сложного состава в десорбере. При развитии вертикальной плёнки в технических аппаратах часто происходят разрывы плёнок и образование струй, капель. Поэтому представляет интерес исследование десорбции струй и капель. Общие положения разработанной и успешно применяемой сегодня теории неизотермической абсорбции [1] могут использоваться и для задач десорбции. В отличие от процессов квазистационарной абсорбции – десорбция существенно нестационарна. При десорбции значительно изменяется концентрация соли, равновесная температура и равновесное парциальное давление на поверхности раздела фаз. Таким образом, для корректного теоретического описания существенно нестационарной и неизотермической десорбции требуется проведение дополнительных экспериментальных исследований в широком диапазоне определяющих параметров. При испарении однокомпонентных и многокомпонентных жидкостей, когда испаряются все компоненты, имеется три характерных режима испарения: 1) полное испарение без отрыва жидкости от твёрдой стенки, 2) перемежающийся отрыв (чередование пузырькового и плёночного кипения), 3) устойчивое плёночное кипение при температуре Лейденфроста. При десорбции высококонцентрированных водных солевых растворов третий режим (устойчивоё плёночное кипение) не наблюдается. Происходит вырождение кризиса теплообмена [2]. При использовании растворов солей имеет место образование третей твёрдой фазы – кристаллогидратной плёнки, что существенно влияет на интенсивность десорбции и требует учёта при теоретическом описании. 54 Для изучения физической картины процессов тепломассообмена в такого рода системах нами были выполнены экспериментальные исследования по нестационарному испарению капель водных растворов солей CaCl2 и LiBr с различной начальной весовой концентрацией СО для в широкого диапазона температур TСТ при атмосферном давлении окружающей среды. Для регистрации текущих параметров неизотермической десорбции дозированных объемов водно-солевых растворов (капель) на горизонтальной поверхности нагрева была разработана экспериментальная методика для проведения прямых измерений веса испаряющейся капли. Рабочий участок был установлен на лабораторные электронные весы. Использование при этом видео и тепловизионной съемки позволило определить качественные и количественные характеристики процесса неизотермической десорбции капель для закона теплообмена TСТ const . Были выявлены следующие закономерности неизотермической десорбции водно-солевых растворов. В диапазоне температур TСТ TКИП (температура стенки меньше температуры кипения) с увеличением начальной массовой концентрации соли CО наблюдалось (см. рис. 1) существенное снижение интенсивности десорбции. Такая закономерность определяется снижением давления насыщенных паров растворителя (воды) над межфазной поверхностью раствора (жидкость–газ) с увеличением концентрации соли [3–6]. Рис. 1. Зависимости для испарения капель дистиллированной воды и водных растворов солей (Vo = 300 мкл; TСТ = 80 °С) 55 При приближении концентрации раствора к линии кристаллизации, на поверхности капли образуется кристаллогидратная плёнка, которая первоначально образуется на краях капли и затем перемещается к центру, полностью покрывая всю поверхность. Дальнейшее испарение воды происходит с поверхности при наличие трёх фаз: жидкая под плёнкой, твёрдая плёнка и водяной пар над поверхностью раздела фаз. Для данного случая необходимо учитывать процесс диффузии воды через твёрдую плёнку. При наличие кристаллогидратной плёнки скорость десорбции уменьшается в десятки раз по сравнению с чистой водой. Таким образом, для описания физической картины десорбции капель растворов солей не могут быть в полной мере использованы теоретические модели квазистационарной абсорбции. Существенное изменение концентрации соли и равновесного парциального давления пара приводит к зависимости диффузии от вышеуказанных параметров. Для корректного теоретического описания важно знать зависимость скорости десорбции от концентрации и температуры, а также учитывать влияние кристаллогидратной плёнки. Исследование физической картины неизотермической десорбции капель, тонких пленок сложного состава имеет междисциплинарный характер. Работа выполнена при финансовой поддержке гранта № 11.G34.31.0003 (ведущий учёный Т.И. Сигфуссон, ТПУ) и № 11.G34.31.0046 (ведущий учёный К. Ханъялич, НГУ) Список литературы: 1. Накоряков В.Е., Григорьева Н.И. Неизотермическая абсорбция в термотрансформаторах. – Новосибирск: Наука, 2010. – 113 с. 2. Nakoryakov V.E. Experimental investigation of the nonstationary desorption of watersalt solutions in the spheroidal state / V.E. Nakoryakov and S. L. Elistratov. Journal of Engineering Thermophysics. – 2009. – V. 18. – № 2. – Р. 87–92. 3. Lower H. Thermodynamishe und Physikalische Eigenschaften der wassrigen LifhumBromid Losung: Dissertation. – Karlsruhe, 1960. – 113 s. 4. Boryta D.A. Solubility of lithium bromide in water between 50 and 100 °С. (45 to 70 % lithium bromide). // Journal on Chemical and Engineering Data. – 1970. – V. 15. – № 1. – P. 142–144. 5. Верба О.И., Груздев В.А., Захаренко Л.Г., Псахис Б.И. Термодинамические свойства и диаграммы водных растворов бромистого лития. // Холодильная техника. – 1986. – № 3. 6. Груздев В.А., Верба О.И. Давление насыщенных паров водных растворов бромистого лития. Исследование теплофизических свойств жидких растворов и сплавов: Сб. научных трудов. – Новосибирск, 1977. – C. 5–19. 56