У С. Ю. Юрова, , А.Н. Черный
реклама

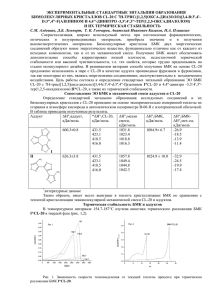
Успехи в химии и химической технологии. ТОМ XXIX. 2015. № 8 УДК 621.039.75, 544.344.015.3 С. Ю. Юрова,1 В. П. Синдицкий1, А.Н. Черный1, А.А. Васильева,2 Д.В. Дашко,2 А.А. Астратьев2 1 Российский химико-технологический университет им. Д.И. Менделеева, Москва, Россия, 125480, Москва, ул. Героев Панфиловцев, д. 20, корп. 1 ФГУП «СКТБ «Технолог», Санкт-Петербург ГОРЕНИЕ БИМОЛЕКУЛЯРНЫХ КРИСТАЛЛОВ CL-20 С ЛИНЕЙНЫМИ НИТРАМИНАМИ Исследованы закономерности горения и разложения бимолекулярных кристаллов (БМК) гексанитрогексаазаизовюрцитана (CL-20) с линейными нитраминами 2,4-динитро-2,4-диазопентаном (DNP) и 2,4динитро-2,4-диазагептаном (DNG). Показано, что в составе БМК линейные нитрамины плавятся при более высоких температурах, а распад CL-20 протекает при более низких температурах в сравнении с индивидуальными компонентами. Молекулярное разбавление CL-20 термостойкими и летучими DNP и DNG приводит к падению скорости горения БМК, определяемой кинетикой тепловыделения CL-20 в конденсированной фазе. Ключевые слова: бимолекулярные кристаллы, гексанитрогексаазаизовюрцитан, 2,4-динитро-2,4-диазопентан, 2,4динитро-2,4-диазагептан, горение. На протяжении последних лет интерес к гексанитрогексаазоизовюрцитану (CL-20) со стороны исследователей не ослабевает. Это обусловлено высокими энергетическими возможностями этого соединения [1-2]. Однако CL-20 является более чувствительным к механическим воздействиям, чем широко применяемый на данный момент октоген. В настоящее время одним из направлений по модификации CL-20 с целью снижения его чувствительности является получение бимолекулярных кристаллов (БМК) с другими соединениями. Однако при этом наблюдается заметное снижение энергетических характеристик по сравнению с индивидуальным CL-20. Тем не менее, идея совмещения в одной кристаллической решетке CL-20 с различными энергоемкими соединениями чрезвычайно заманчива, поскольку позволяет во многом влиять на другие недостатки самого CL-20, такие как повышенная растворимость в полярных растворителях (нитроэфиры, ацетаты, нитросоединения и другие) и, как следствие, неконтролируемое изменение конформационного состояния. На сегодняшний день известны БМК CL-20 с триацетатом глицерина [3], диметилформамидом [4]. Уже получены и исследованы кристаллические структуры бимолекулярных кристаллов CL-20 с тринитротолуолом (ТНТ) [5], октогеном (HMX) [6], БТФ (бензотрифуроксаном) [7], 2,4-динитро-2,4диазопентаном (DNP) и 2,4-динитро-2,4диазагептаном (DNG) [8]. Очевидным преимуществом бимолекулярных кристаллов по сравнению с механической смесью является распределение компонентов на молекулярном уровне, что может сказаться в случае протекания каких-либо химических реакций между компонентов. Кроме того, комплексообразование серьезно изменяет как температуру плавления компонентов, так и параметры термического распада по сравнению с индивидуальными составляющими этого БМК [9]. Это в свою очередь может серьезно повлиять на закономерности горения. В этой связи целью данной работы явилось изучения закономерностей горения бимолекулярных кристаллов CL-20. В качестве объектов исследования выбраны БМК CL-20 с 2,4-динитро-2,4диазапентаном DNP (СLD) в соотношении 2:1 (рисунок 1) и БМК CL-20 с 2,4-динитро-2,4диазагептаном DNG (далее в тексте СLD-2) в соотношении 1:1 (рисунок 2). Рисунок 1 - Состав СLD Рисунок 2 - Состав СLD-2 Выбор этих объектов продиктован тем обстоятельством, что их содержание в комплексе будет заметно меньше, чем для большинства других энергоемких субстратов и, следовательно, энергетические характеристики будут в меньшей степени отличаться от взрывчатых характеристик CL20. Действительно, согласно расчетам, для чистого CL-20 адиабатическая температура горения (Тf) при давлении 10 МПа составляет 3365°С. Для БМК CLD она всего на 100°С ниже, а для CLD-2 это падение температуры более ощутимо и составляет 700°С. Бимолекулярные кристаллы для исследований были получены по методике, описанной в работе [8]. Дифференциальносканирующую калориметрию (ДСК) и термогравиметрию проводили в диапазоне температур 25—300°С с помощью термического анализатора DSC 822e Mettler Toledo при скорости 35 Успехи в химии и химической технологии. ТОМ XXIX. 2015. № 8 нагрева 10°С/мин в токе азота и массе навесок 1—3 мг. Образцы для исследования горения готовились прессованием измельченного вещества в плексигласовые трубки внутренним диаметром 4 мм при давлении прессования 200 МПа. Эксперименты по измерению скорости горения проводили в бомбе постоянного давления БПД-360 объемом 1.5 литра в интервале давлений 0.1-15 МПа. Давление создавалось азотом. Помещенный в бомбу заряд воспламенялся витой спиралью. Температурные профили в волне горения получены с помощью плоских вольфрам-рениевых микротермопар с толщиной термоспая 5-7 мкм. Термодинамические расчеты проводились с помощью программы REAL [10]. Согласно данным термогравиметрического анализа [11] оба линейных нитрамина DNP и DNG испаряются в интервале температур 70-170qС без видимых признаков разложения. В тоже время по данным термопарных исследований [12] CL-20 является нелетучим веществом с высокой температурой испарения. Следовательно, можно ожидать, что линейные нитрамины в волне горения БМК будут испаряться первыми. Согласно данным ТГА бимолекулярных кристаллов CLD и CLD-2 в области температур 150185 и 110-170qС потеря массы составляет 16.8 и 34.8%, соответственно, что очень хорошо согласуется с содержанием в БМК линейных нитраминов (15.7 и 30.5%). Потеря массы на второй стадии для обоих БМК протекает в близком температурном интервале 210-250qС и составляет 75 и 64%, соответственно. На термограммах ДСК наблюдается слабый эндотермический сигнал для CLD в области 111114qС и для CLD-2 в области 139-145qС в зависимости от скорости нагрева. Это значительно выше температур плавления линейных нитраминов DNP и DNG (54 и 76qС [8], соответственно). Максимально измеренные тепловые эффекты на этой стадии составляют 15.9 и 57.2 Дж/г, что в пересчете на содержание линейных нитраминов составляет 101.2 и 187.5 Дж/г. Для DNP полученная величина практически совпадает с теплотой плавления чистого DNP 102.3 Дж/г [13], что свидетельствует о том, что плавлению подвергается только линейный нитромин, CL-20 остается в твердом виде. Испарение нитрамина DNP на ДСК термограммах фиксируются в виде эндотермического пика в области 185°С, частично закрываемого экзотермическим пиком разложение CL-20 в области 214-223°С в зависимости от скорости нагрева. Величина эндоэффекта 27-29 Дж/г или 173185 Дж на грамм DNP соответствует лишь 33-35% от теплоты испарения DNP [14], остальная часть DNP испаряется совместно с разложением CL-20. Максимально измеренный тепловой эффект разложения CLD составляет 2852 Дж/г, что с учетом доли CL-20 и тепловых потерь на испарение DNP дает величину теплоты разложения CL-20 в бимолекулярном кристалле в 3440 Дж/г. На ДСК термограммах CLD-2 отдельного пика испарения DNG не наблюдается, экзоэффект разложения CL-20 составляет 2269 Дж/г. Пересчет теплового эффекта на чистый CL-20 дает величину в 3420 Дж/г, то есть линейные нитрамины не влияют на химизм разложения CL-20. Однако стабильность CL20 в бимолекулярных кристаллах стало заметно меньше. Скорее всего, это связано с тем, что после испарения линейных нитраминов CL-20 находится в аморфном виде и влияние кристаллической решетки на распад отсутствует. 100 50 30 CLD CLD2 Скорость горения, мм/с 20 10 TC CL-20 5 DNP 3 2 1 0.5 0.3 0.2 0.1 0.1 0.2 0.3 0.5 1 2 3 5 Давление, MPa 10 20 Рисунок 3 – Сравнение зависимости скорости горения CLD-1 и CLD-2 с CL-20, DNP и тройной смеси ТС [17]. 800 700 CL-20 CLD-2 Температура, oC 600 500 TS 400 300 200 Tm 100 0 -1 -0.5 0 0.5 Расстояние, мм 1 1.5 2 Рисунок 4 – Сравнение температурных профилей в волне горения CLD-2 и CL-20 при атмосферном давлении. TS и Tm –температуры поверхности и плавления. Согласно опубликованным кинетическим данным по разложению алифатических нитраминов [15] и CL20 [16] термическая стабильность первых в несколько раз превосходит стабильность CL-20. Это означает, что в волне горения области тепловыделения CL-20 и линейных нитраминов будут пространственно 36 Успехи в химии и химической технологии. ТОМ XXIX. 2015. № 8 разделены, DNP и DNG будут выступать в качестве инертных разбавителей. Действительно, оба БМК горят со скоростями меньшими, чем скорость горения CL-20 (Рисунок 3). Как и для CL-20 зависимость U(P) БМК состоит из двух участков. Первый при низких давлениях характеризуется более низким значением показателя степени в законе горения ν, а после излома в области 1-2 МПа наблюдается более резкое увеличение скорости горения. Сравнение термопарных профилей CLD-2 и CL20, записанных при атмосферном давлении, показывает, что на профилях CLD-2 температура поверхности расположена при более низкой температуре, обусловленной испарением DNG (Рисунок 4). В работе [12] было показано, что скорость горения CL-20 определяется ведущей реакцией в конденсированной фазе (к-фазе). Исследований механизма горения индивидуальных линейных нитраминов не проводилось, однако в работе [17] исследовался механизм горения тройной смеси, содержащей наряду с DNP еще два близких по строению нитрамина. Оказалось, что горение тройной смеси также определяется ведущей реакцией в к-фазе. Отметим, что, поскольку скорость горения БМК выше, чем скорость горения линейных нитроаминов, их глубина разложения в к-фазе БМК будет ниже изза меньшего времени пребывания там. Как видно из сравнения закономерностей горения исследованных БМК добавление алифатических нитраминов к CL-20 приводит к падению скорости горения непропорционально по сравнению с количеством добавки. Так, в области 2-10 МПа скорость горения CLD очень слабо отличается от скорости горения CL-20, в то время как для CLD-2 падение скорости достигает 3 раз. При низких давлениях падение скорости горения пропорционально введенным добавкам, что подчеркивает ведущую роль CL-20 в горении БМК. Юрова Серафима Юрьевна студент V курса кафедры химии и технологии органических соединений азота РХТУ им. Д. И. Менделеева, Москва, Россия Синдицкий Валерий Петрович д.х.н., декан ИХТ факультета, профессор кафедры химии и технологии органических соединений азота РХТУ им. Д.И. Менделеева, Москва, Россия Черный Антон Николаевич ведущий инженер кафедры химии и технологии органических соединений азота РХТУ им. Д. И. Менделеева, Москва, Россия Васильева Анна Анатольевна инженер технолог ФГУП «СКТБ «Технолог», Санкт-Петербург Россия Дашко Дмитрий Владимирович к.х.н., начальник отдела, ФГУП «СКТБ «Технолог», СанктПетербург, Россия Астратьев Александр Александрович, д.х.н., зам. директора по научной работе ФГУП «СКТБ «Технолог», Санкт-Петербург, Россия Литература 1. Nielsen A.T. Caged polynitramine compounds, US Pat., 5693794, publ. Dec. 2, 1997. 2. Simpson R.L., Urtiew P.A., Ornellas D.L., Moody G. L., Scribner K. J., Hoffman D.M. CLǦ20 performance exceeds that of HMX and its sensitivity is moderate. Propellants, Explosives, Pyrotechnics, 1997, 22(5), 249-255. 3. Алдошин С.М., Алиев З.Г., Гончаров Т.К., Корчагин Д.В., Милёхин Ю.М., Шишов Н.И. // Известия АН. Сер. хим. – 2011- № 7 – с. 1372. 4. Yu-Xiang Ou, Hui-Ping Jia, Bo-Ren Chen, Yong-Jiang Xu, Jiang-Tao Chen, Rui-Xing Xu // Chin.J.Org.Chem. – 1999 – № 19 - P. 500. 5. Bolton O., Matzger A. J. // Angew. Chem. Int. Ed. – 2011 – Vol. 50. – P. 8960. 6. Bolton O., Simke L. R., Pagoria P. F., Matzger A. J. // Cryst. Growth Des. – 2012 – Vol. 12. – P. 4311. 7. Zongwei Yang, Hongzhen Li, Xioqing Zhou, Chaoyng Zhang, Hui Huang, Jinshan Li and Fude Nie // Cryst. Growth Des. – 2012. – Vol. 12. - № 11. P. 5155. 8. Гончаров Т. К., Алиев З. Г., Алдошин С. М., Дашко Д. В., Васильева А. А., Шишов Н. И., Милехин Ю. М. Получение, структура и основные свойства бимолекулярных кристаллов CL-20—DNP и CL-20—DNG // Известия АН. Сер. хим. – 2015- № 2 – с. 366. 9. Gao B., Wang D., Zhang,J. et al. Facile, continuous and large-scale synthesis of CL-20/HMX nano co-crystals with high-performance by ultrasonic spray-assisted electrostatic adsorption method // J. Mat. Chem. A, 2014, Vol.2(47), pp.19969-19974. 10. Belov G.B. Thermodynamic Analysis of Combustion Products at High Temperature and Pressure // Propellants, Explosives, Pyrotechnics. – 1998. – Vol.23. – P. 86 – 89. 11. Vijayalakshmi R., Naik N. H., Gore G. M., Sikder A.K. Linear Nitramine (DNDA-57): Synthesis, Scale-Up, Characterization, and Quantitative Estimation by GC/MS // J. Ener. Mat. – 2015. – Т. 33. – №. 1. – С. 1-16. 37 Успехи в химии и химической технологии. ТОМ XXIX. 2015. № 8 12. Синдицкий В.П., Егоршев В.Ю., Березин М.В., Серушкин В.В., Милехин Ю.М., Гусев С.А., Матвеев А.А. Закономерности и механизм горения высокоэнергетического каркасного нитрамина гексанитрогексаазаизовюрцитана // Ж. химической физики - 2003 - T.22(7)-C. 69-74 13. Spitzer D., Braun S., Schäfer M.R., Ciszek F. Comparative Crystallization Study of Several Linear Dinitramines in NitrocelluloseǦBased Gels //Prop., Explos., Pyrot. – 2003. – Т. 28. – No 2. – C. 58-64. 14. Miroshnichenko E.A., Kon’kova T.S., Matyushin Y.N., Inozemtsev Y.O. Bond dissociation energies in nitramines //Russ. Chem. Bull. – 2009. – Т. 58. – №. 10. – С. 2015-2019. 15. Манелис Г.Б., Назин Г.М., Рубцов Ю.И., Струнин В.А. Термическое разложение и горение взрывчатых веществ и порохов. – М.; Наука, 1996, 233с. 16. Корсунский Б.Л., Неделько В.В., Чуканов Н.В., Ларикова Т.С., Фольк Ф. Кинетика термического разложения гексанитрогексаазаизо-вюрцитана // Изв. АН, Сер.хим., 2000, No. 5, С.815-821. 17. Ermakov A.S., Petrov E.Y., Vinogradov D.B., Van Toai F., Denisyuk A.P., Rusin D.L. New plasticizers for energetic materials //Theoretical Foundations of Chemical Engineering. – 2007. – Т. 41. – №. 5. – С. 660-667. Yurova Seraphima Yurevna, Sinditskii Valery Petrovich, Chernyi Anton Nikolaevich, Vasilyeva Anna Anatol’evna, Dashko Dmitry Vladimirovich, Astratev Alexander Alexandrovich. D.I. Mendeleev University of Chemical Technology of Russia, Moscow, Russia. COMBUSTION OF BIMOLECULAR CRYSTAL OF CL-20 WITH A LINEAR NITRAMINES Abstract Combustion and decomposition behaviors of biomolecular crystals (BMC) hexanitrohexaazaisowurtzitane (CL-20) with linear nitramines 2,4-dinitro-2,4-diazopentane (DNP) and 2,4-dinitro-2,4-diazaheptane (DNG) have been studied. It is shown that linear nitramines melt in the composition of BMP at higher temperatures, and CL-20 decomposition proceeds at lower temperatures in comparison with the individual components. Molecular dilution of CL-20 by termostable and volatile DNP and DNG leads to a drop in the burning rates of BMC, which are determined by kinetics of CL-20 heat release in the condensed phase. Key words: bimolecular crystals, hexanitrohexaazaisowurtzitane, 2,4-dinitro-2,4-diazopentane, 2,4-dinitro-2,4-diazaheptane, combustion. 38