Двойные – состоят из кислотного остатка, связанного с атомами
реклама
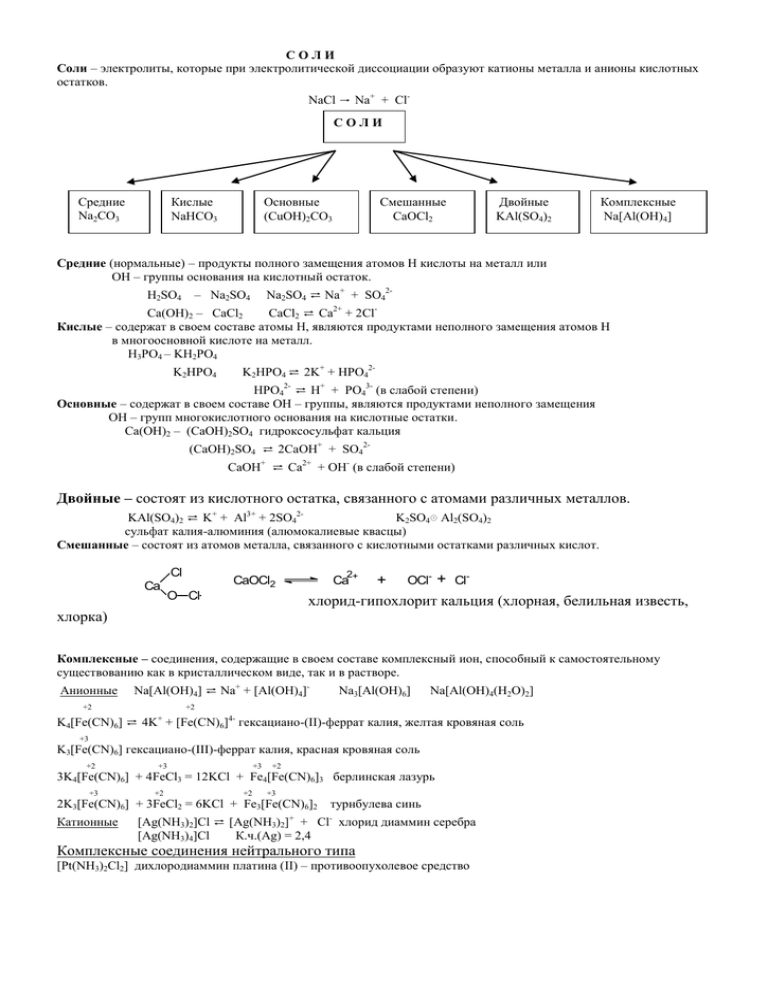
СОЛИ Соли – электролиты, которые при электролитической диссоциации образуют катионы металла и анионы кислотных остатков. NaCl → Na+ + ClСОЛИ Кислые NaHCO3 Cредние Na2CO3 Основные (CuOH)2CO3 Смешанные СаOCl2 Двойные KAl(SO4)2 Комплексные Na[Al(OH)4] Средние (нормальные) – продукты полного замещения атомов Н кислоты на металл или ОН – группы основания на кислотный остаток. H2SO4 Na2SO4 ⇄ Na+ + SO42- – Na2SO4 Ca(OH)2 – CaCl2 CaCl2 ⇄ Ca2+ + 2ClКислые – содержат в своем составе атомы Н, являются продуктами неполного замещения атомов Н в многоосновной кислоте на металл. H3PO4 – KH2PO4 K2HPO4 K2HPO4 ⇄ 2K+ + HPO42- HPO42- ⇄ H+ + PO43- (в слабой степени) Основные – содержат в своем составе ОН – группы, являются продуктами неполного замещения ОН – групп многокислотного основания на кислотные остатки. Ca(OH)2 – (CaOH)2SO4 гидроксосульфат кальция (CaOH)2SO4 ⇄ 2CaOH+ + SO42CaOH+ ⇄ Ca2+ + OH- (в слабой степени) Двойные – состоят из кислотного остатка, связанного с атомами различных металлов. KAl(SO4)2 ⇄ K+ + Al3+ + 2SO42K2SO4ּ Al2(SO4)2 сульфат калия-алюминия (алюмокалиевые квасцы) Смешанные – состоят из атомов металла, связанного с кислотными остатками различных кислот. Cl Ca CaOCl2 O Cl 2 Ca + + OCl- + Clхлорид-гипохлорит кальция (хлорная, белильная известь, хлорка) Комплексные – соединения, содержащие в своем составе комплексный ион, способный к самостоятельному существованию как в кристаллическом виде, так и в растворе. Анионные Na[Al(OH)4] ⇄ Na+ + [Al(OH)4]- +2 Na3[Al(OH)6] Na[Al(OH)4(H2O)2] +2 K4[Fe(CN)6] ⇄ 4K+ + [Fe(CN)6]4- гексациано-(II)-феррат калия, желтая кровяная соль +3 K3[Fe(CN)6] гексациано-(III)-феррат калия, красная кровяная соль +2 +3 +3 +2 3K4[Fe(CN)6] + 4FeCl3 = 12KCl + Fe4[Fe(CN)6]3 берлинская лазурь +3 +2 +2 +3 2K3[Fe(CN)6] + 3FeCl2 = 6KCl + Fe3[Fe(CN)6]2 Катионные турнбулева синь [Ag(NH3)2]Cl ⇄ [Ag(NH3)2]+ + Cl- хлорид диаммин серебра [Ag(NH3)4]Cl К.ч.(Ag) = 2,4 Комплексные соединения нейтрального типа [Pt(NH3)2Cl2] дихлородиаммин платина (II) – противоопухолевое средство