2.2. Контроль транскрипции с помощью РНК и ДНК
реклама

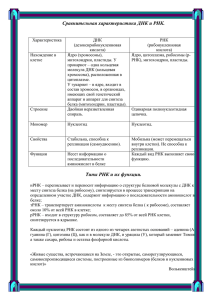
2.2. Контроль транскрипции и трансляции и с помощью РНК и ДНК, посттрансляционный контроль. Контроль транскрипции (Энхансеры, Сайленсеры, Аттенуаторы, РНКпереключатели). Посттрансляционный контроль: аллостерическая регуляция, ковалентная модификация и компартментация. Контроль транскрипции и трансляции с помощью РНК и ДНК, посттрансляционный контроль. Регуляция транскрипции может проходить с помощью белковых регуляторов и специфических последовательностей ДНК и РНК. Для некоторых регуляторных белков не существует эффекторов, либо белок выполняет двойную роль, действуя как активатор на один промотор и как репрессор на другой. В некоторых случаях белок-репрессор может становиться активатором после взаимодействия с молекулой эффектора. Если оперон представляет собой часть модулона (группы оперонов с разными функциями, но объединенных общей задачей), его транскрипция регулируется специфическим регулятором оперона и общим регулятором модулона. Важную роль в инициации транскрипции выполняет РНК-полимераза, её δсубъединица распознает промотор. В регуляции участвуют также удаленные сайты (энхансеры и сайленсеры). В некоторых случаях инициация транскрипции зависит от структуры ДНК, измененине суперспирализации ДНК может стимулировать или подавлять активность промоторов. Процессы элонгации и терминации транскрипции также подвержены регуляции, перемещение РНК-полимеразы происходит неравномерно и может прерываться паузами или преждевременной терминацией. В контроле экспрессии генов иакже участвуют процессы рекомбинации ДНК и метаболизм РНК. Контроль транскрипции (Энхансеры, Сайленсеры, Аттенуаторы, РНК- переключатели). Энхансеры и удаленные сайты. Сайты активации расположенные на большом удалении от промотора – Энхансеры, они обнаружены у эукариот, но встречаются и у бактерий. Белки, связывающиеся с энхансерами, активируют транскрипцию, взаимодействуя c HYR1 полимеразой. Часто происходит изгибание петли ДНК, при этом энхансер и промотор сближаются. Известны также мобильные м энхансеры бактериофагов. РНК НК-полимераза содержит кодируемый фагом фактор σ55. 55. Репликация активируется при узнавании одноцепочечных разрывов ДНК. Репликационная вилка служит их источником. Аттенуация на примере оперона синтеза триптофана. После начала транскрипции лидерного региона региона процесс может быть остановлен – аттенуация. Последовательность РНК (аттенуатор) формирует 4 региона, комплиментарных друг другу (1-2, (1 2-3, 3-4). Соединение петель 11-2 и 3-4 приводит к образованию вилки препятствующей продвижению РНК-полимеразы РНК полимеразы далее за ллидерный регион. Соединение петель 2-3 2 3 формирует антитерминаторную петлю и транскрипция продолжается. Причина – содержание 2 кодонов Trp в области 1, если тРНК тРНК-Trp мало – рибосома задерживается связывая петлю 1, петли 2 и 3 соединяются и не препятствуют транскрипции. Высокий уровень триптофана обеспечит беспрепятственную трансляцию 1 и 2 участков. При этом 3 и 4 образуют вилку, и рибосома будет вынуждена диссоциировать от иРНК. 2 РНК-переключатели переключатели (riboswitch). ( Особая форма аттеннуации в ходе трансляции транс без участия рибосом. Лидерный регион иРНК (РНК-переключатель) переключатель) формирует различные конформации включая и выключая трансляцию. Смена конформаций происходит в ответ на связывание молекул эффекторов (метаболитов), что считалось функцией исключительно белков. Пример: Синтез рибофлавина у Bacillus subtilis.. Флавинмононуклеотид (ФМН) – продукт рибофлавина, связывается связывается с лидерным регионом м мРНК, останавливая трансляцию. В отсутствие метаболита (лиганда), комплиментарные последовательности на лидерной РНК связаны, ны, рибосома имеет доступ к Шайн-Дельгарно Шайн Дельгарно последовательности. Лиганд блокирует одну из комплиментарных последовательностей, вторая связывается с участком инициации. Трансляции нет. 3 Регуляция путем рекомбинации ДНК. Сайт-специфическая реципрокная рекомбинация с перестройкой структуры генов может многократно включать и отключать гены, обеспечивая адаптацию. Пример: Синтез 2 типов белка жгутиков – флагеллина у бактерий. Продукт варианта В экспрессируется совместно с белком, который служит репрессором экспрессии белка варианта А. Также совместно с белком экспрессируется фактор hin, катализирующий инверсию путем рекомбинации. Инвертированный промотор варианта В не запускает синтеза белка В и репрессора, Транскрипция варианта А идет беспрепятственно. Регуляция и метаболизм РНК. Обычно, РНК у прокариот транслируется в том же виде что синтезируется. Исключение составляют некоторые бактериофаги и некоторые полицистронные РНК бактерий. Пример: оперон rrn, РНК которого содержит 23S-, 16S-, 5S- рРНК и несколько тРНК последовательностей. Для предотвращения бесполезной трансляции, РНК подвергается деградации. Малые РНК. Известно множество молекул РНК не относящихся к тРНК, мРНК или рРНК – малые РНК. У E.coli известно более 40 мРНК от 40 до 400 нуклеотидов. Предполагается, что у эукариот насчитывается сотни и тысячи мРНК. У E.coli мРНК регулируют трансляцию, комплиментарно соединяясь с лидерными последовательностями иРНК – антисмысловая РНК. Трансляция гена ompF (белка порина) регулируется антисмысловой РНК MicF – продукта гена micF. 4 Посттрансляционный контроль: аллостерическая регуляция, ковалентная модификация и компартментация. Наряду с регуляцией экспрессии генов, которая может занимать до нескольких периодов генерации, клеткам требуется более оперативный и гибкий путь координации метаболической активности. Микроорганизмы должны регулировать метаболизм для сохранения материалов и энергии в условиях постоянно меняющейся окружающей среды. Если E.сoli выращивается на среде с единственным источником углерода – глюкозой, все пути функционируют, если добавить триптофан, угнетается путь его синтеза. Если перенести бактерию на среду с лактозой – запускается путь ее метаболизма. Регуляция синтеза у прокариот. Пути регулирования метаболических путей: Компартментация. Аллостерическая регуляция. Ковалентная модификация. 5 Компартментация. Обеспечивает быстрое регулирование схожих метаболических путей. Пути координируются движением метаболитов и коферментов между частями клетки. Отсутствие мембранных органоидов у прокариот значительно усложняет регуляцию катаболических и анаболических процессов. Все они протекают в гомогенной цитоплазме. Цитоплазма – достаточно плотная и вязкая среда, молекулы затрачивают некоторое время на диффузию. В клетке может формироваться разность концентраций метаболитов. Отсутствие мембранных органоидов у прокариот значительно усложняет регуляцию катаболических и анаболических процессов. Все они протекают в гомогенной цитоплазме. Основные механизмы разделения метаболических реакций: Кинетическая (различия в сродстве компонентов и констант равновесия). Временная (поочередный синтез). Использование разных ферментов. Физическая компартментация. Компартменты прокариотической клетки: Цитоплазма; Плазматическая мембрана; Периплазматическое пространство; Наружная мембрана; Наружная поверхность и примыкающее внеклеточное пространство. Катаболические и анаболические пути, имеющие общие промежуточные продукты, должны регулироваться очень точно, во избежание «холостых циклов», когда продукт одной реакции, может разлагаться следующим ферментом. Пример – реакции, катализируемые ферментом фосфофруктокиназой и фруктозо-1,6,-бифосфатазой. В таких случаях компартментация осуществляется при помощи регуляции экспрессии генов, аллостерической регуляции катаболических и анаболических ферментов. Принципы регуляции ферментов. Ферменты катализируют химические реакции, обладая большой специфичностью. Структура фермента: апоэнзим + кофактор формируют холоэнзим. Кофактор: простетическая группа или коэнзим. Ферменты увеличивают скорость реакции, не сдвигая 6 равновесия. Присоединение субстрата происходит к каталитическому сайту, увеличивая число молекул имеющих достаточную энергию активации и число промежуточных молекул. Ферменты ускоряют реакции до 10 млрд. раз. Скорость оборота от 1 до 10 000 в с., ДНК полимераза I – 15, лактатдегидрогеназа – 1000. Ферменты чувствительны к температуре, концентрации субстрата, кислотности среды, денатурирующим химическим агентам. У микроорганизмов обнаружены также рибозимы, выполняюшие функции сплайсинга РНК. Регуляция активности ферментов осуществляется по нескольким механизмам: Конкурентное ингибирование ферментов – блокирование активного сайта. Может использоваться в антибактериальной терапии (сульфаниламид блокирует синтез фолиевой кислоты). Неконкурентное – связывание с другими участками (аллостерический) с изменением конфигурации (тяжелые металлы, ртуть). Аллостерическая регуляция – за счет конформационных изменений молекулы фермента в результате связывания с определенным (не активным) центром. Ковалентная модификация осуществляется путем фосфорилирования, протеолиза, метилирования, ацетилирования, аденилирования, уридинилирования или ацилирования жирными кислотами. Аллостерическая регуляция. Аллостерические ферменты имеют 2 активных сайта – каталитический и аллостерический. Связывание молекулы-регулятора с аллостерическим сайтом вызывает изменение конформации фермента, каталитический сайт получает или теряет способность связывать молекулу субстрата. Аллостерические ферменты состоят из нескольких субъединиц (2, 4 и более), кроме субстрат-связывающего сайта эти ферменты содержат один или несколько сайтов для связывания молекул эффекторов. Эффекторы либо снижают (обычно конечные продукты реакций) либо повышают (обычно промежуточные продукты) активность фермента. 7 Рисунок 1. Конкурентное/неконкурентное ингибирование [[Joanne M. Willey et al. 2008]. Ингибирование по типу обратной связи (конечным продуктом). Характерный механизм для анаболических анаболических реакций. Конечный продукт в некоторых случаях может связываться с аллостерическим сайтом первого специфического фермента пути. Накопление продукта – сигнал о прекращении его синтеза, что позволяет избежать накопления промежуточных продуктов. У E. сoli,, треонин – изолейцин, продукт – ингибирует первую реакцию, когда он истощается, реакция запускается. Обратная связь. Рисунок 1. Ингибирование синтеза триптофана по механизму «обратной связи» [Joanne M. Willey et al.. 2008]. 2008] 8 Ковалентная модификация белков. Как правило, происходят обратимые изменения ферментов. Фосфорилирование белков – наиболее распространенный механизм модификации. В нем участвуют протеинкиназы, фосфопротеинфосфатазы, которые переносят фосфат на гистидин, цистеин, тирозин, аспартат, треонин и серин. Другой распространенный механизм модификации ферментов -- аденилирование (Белок + АТФ = ФФ + Белок-АМФ). Адаптация бактерий. В отличие от растений и животных, большинство бактерии живут в постоянно изменяющихся условиях среды. Они способны реагировать на изменения, корректируя структурные протеины, транспортные белки, токсины, ферменты. Например E.сoli не продуцирует фимбрии, когда свободно живет в толще воды. Vibrio cholerae не продуцирует холерный токсин, вне ЖКТ. Bacillus subtilis не синтезирует фермент для синтеза триптофана если в среде есть его предшественники. Neisseria gonorrhoeae развивает сложную систему поглощения и транспорта железа, если его не хватает в среде. 9