ЛИПИДЫ (Обмен. Регуляция. Патология)
реклама

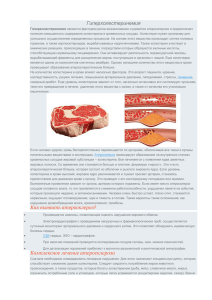
ЛИПИДЫ (Обмен. Регуляция. Патология) Синтез триацилглицеролов и фосфоглицеролипидов. Биосинтез холестерина. Ацетоновые тела. Связь между обменом жиров и углеводов. Биоэффекторная роль различных представителей класса липидов. Регуляция и патология липидного обмена. СИНТЕЗ ТРИАЦИЛГЛИЦЕРОЛОВ И ФОСФОГЛИЦЕРОЛИПИДОВ А. 1. Глицерофосфатный (почки, кишечник, печень) Б. 3. 2-Моноацил глицератный (кишечник) ОН АТФ HO 2. Диоксиацетонфосфатный (жировая ткань, мышцы, печень) ОН АДФ НАД НАДН/Н+ HO Глицерол-3-фосфат Глицерин ОН O О - PO3H2 ОН ДАФ-ДГ ОН ДАФ ОН R ОН МАГ R-C~SKoA O Трансфераза HSKoA Фн R2 ДАГ R1 Трансфераза R1 ОН R-C~SKoA ФФн О - PO3H2 Фосфатидат Фосфатаза R2 ЦТФ R1 H2 O R1 R2 HSKoA ТАГ R2 R3 ЦДФ ЦДФ-ДАГ Инозит ЦМФ ФФн O ЦДФ-ЭА ЦДФ-холин ЦМФ ЦДФ R2 R1 R1 ЦДФ R2 О-РО3-Глицерин Р Метилирование S АГц Р холин х3 Фосфатидилхолины SАМ R1 R2 Трансфераза ИН Фосфатидилинозитолы ЦМФ R1 R2 R1 О- Р Р -О О Серин СО2 Этаноламин R1 R2 R3 Р Серин Фосфатидилсерины Серин Обменное замещение ЦДФ R4 НО Обменное замещение R2 О Р ЭА Фосфатидилэтаноламины Дифосфатидилглицерины (кардиолипины) Триглицериды конкурирут с фосфолипидами за ДАГ. Метионин способствует синтезу фосфолипидов, обеспечивая процесс метилирования фосфатидилэтаноламинов. В итоге происходит переключение с синтеза ТАГ на синтез фосфолипидов. Это спасает организм от ожирения. ЦДФ – это специфические нуклеотиды для обмена липидов. Фосфотидилинозитолы. (схема активации протеинкиназы С). Сигнальная молекула ПК (акт.) Фосфолипаза С Рецепторный домен мембранный домен мембрана неакт. цитоплазма PIP2 акт. ГТФ ГТФ GP ДАГ Са+ ДАГ IP3 ГДФ ГДФ белок (факторы клет. роста) Са2+ прерывание сигнала ЭПР Са2+ Са2+- АТФ + 1 + 3 Са2+-кальмодулиновый комплекс прерывание клеточный ответ кальмодулин (вторич. ПК С посредник) неакт. Са2+ АДФ АТФ-аза факторы роста бел.- Р фосфопротеины АТФ АДФ сигнала Фосфодиэстераза ц-АМФ (блокирование циклазных систем) + 2 клет. ответ АДФ киназы (ПК) фосфопротеин АТФ белок (легкие цепи миозина) Энергия поступает из липидов, блокировка мобилизации углеводов Синтез вторичных мессенджеров: ДАГ и Инозит-1,4,5-трифосфата R R 1 O O 2 ЖК Фосфатидная кислота O ЖК HO O O P P O OH 5 OH OH O 1 HO OH 4 O HO P O OH Фосфатидилинозит-4,5-дифосфат (PIP2) Н2О OH ДАГ + Фосфолипаза С HO P O O O O 5 P OH OH OH 1 HO OH4 O HO P OH Инозит-1,4,5-трифосфат (IP3) O Фосфолипиды Липопротеины низкой (ЛПНП) и высокой плотности (ЛПВП) состоят на 11-17% и 24-40% из фосфолипидов, основную часть которых составляют фосфатидилхолины. От их количества зависит содержание ЛПНП и ЛПВП в крови. Повышение уровня ЛПНП наблюдается при: гиперлипопротеинемии III типа первичной семейной гиперхолестеринемии гиперкортицизме сахарном диабете гипотиреозе Понижение – при: синдроме мальабсорбции муковисцидозе тяжелом голодании Количество ЛПВП повышается при хроническом алкоголизме и снижается при: обтурационной желтухе лимфогранулематозе парентеральном питании Фосфатидилхолины служат основными компонентами биомембран. Особенно много их Функционирование в мозге, нервной ткани, сердце и печени. этих тканей и органов зависит от обмена фосфоглицеридов. Так, снижение его интенсивности в мозге происходит при инсулиновой коме, наркозе и возбуждении. Недостаток холина или метионина нарушает синтез фосфатидилхолинов в печени. Это приводит к жировой инфильтрации печени. СИНТЕЗ СФИНГОЛИПИДОВ (Болезни накопления. В мозге у детей) Серин Пальмитоил-КоА НАДФН/Н НАДФ Сфинганин Кетосфинганин АцилHS-KoA КоА Болезнь Нимана-Пика (у детей) Сфингомиелины (депо церамида) ФАД ФАДН2 Сфингенин (сфингозин) Церамиды Сфингомиелиназа Болезнь Гоше Регуляция клеточной дифференцировки Цереброзиды 1) Глюкоцереброзидаза Ганглиозиды (стимулируют рост клеток) Углеводные цепочки Болезнь Краббе 2) Галактоцереброзидаза ацетилгексозаминидаза Болезнь Тея-Сакса "пенистые клетки" "Болезни накопления" - врожденное отсутствие соответствующих ферментов в лизосомах клеток Болезни накопления (синоним: тезаурисмозы, накопительные ретикулезы) — общее название большой группы заболеваний, характеризующихся врожденными или приобретенными нарушениями метаболизма и патологическим накоплением в крови и (или) в клетках различных органов продуктов обмена веществ. Накапливающиеся вещества по своей химической природе могут быть белками (при амилоидозе), липидами (при лейкодистрофиях, гистиоцитозах X, болезнях Гоше, Ниманна — Пика), углеводами (Гликогенозы, Мукополисахаридозы), продуктами минерального обмена (Гемохроматоз, Гепатоцеребральная дистрофия), порфиринами (Порфирии), пуринами (Подагра). В значительной части случаев болезни накопления связаны с наследственными энзимопатиями (Ферментопатии). Могут быть поражены ц.н.с., система кроветворения, сердце, печень, селезенка, почки, поджелудочная железа, кишечник и другие органы и ткани. Для диагностики болезни накопления определяют содержание продуктов метаболизма в крови (например, мочевой кислоты при подагре, железа — при гемохроматозе), проводят цитологическое и цитохимическое исследование биоптатов органов (при амилоидозе, болезни Гоше), энзимологические исследования. КЕТОГЕНЕЗ 2 х СН3-С~SKoA O конденсация СН3-С-СН2-С~SKoA трансфераза синтаза АМФ+ ФФн Н2О HSKoA СН3-С~SKoA ГМГ-КоАлиаза АТФ O ЦТК OН O гидроксиметилглуарил-КоА O ацетил-КоА HSKoA сукцинил-КоА НООС-СН2- С-СН2-С~SKoA O O ацетоацетил-КоА ацетил-КоА НООС-СН2-СН2-С~SKoA СН3 1 2 Н3С-С-СН2-СООН О ацетоацетат Синтез холестерина НООС-СН2-СН2-СООН сукцинат НАДН/Н+ Другие гкани Печень НАД+ Н3С-СН-СН2-СООН кровоток СО2 (при кетозе ) Н3С-СН-СН3 ОН гидроксибутират Другие ткани спонтанно О ацетон Печень Гидроксиметилглутарил-КоА – последний общий продукт двух процессов: 1 – синтез кетоновых тел 2 – синтез холестерина Норма: концентрация в крови равна 2 мг/дл ЖК – основной источник энергии при: 1. Длительной мышечной работе 2. Голодании 3. Диабете Если синтез кетоновых тел превышает возможности тканей использовать их, то развивается кетоацидоз (кетоз): 1. Концентрация кетоновых тел превышает 20 ммоль/л 2. Диурез: норма равна 40 мг/сут Патология: 50 г/сут и более СИНТЕЗ ХОЛЕСТЕРИНА (Цитозоль: печень, кишечник, кожа) 2НАДФ 2НАДФН/Н 3 х Ацетил-КоА СН3 HS-KoA НООС-СН2-С-СН2-СН2-ОН ГМГ-КоАОН редуктаза Мевалонат -холестерин 3 АТФ -глюкагон -кетостероиды +инсулин +тироксин 3АДФ ГМГ-КоА Хлорофилл ПолимериСН3 СН3 СО2 зация Н2С = СН2-С-СН2-СН2- О- Р -О- Р НООС-СН2-С-СН2-СН2-О- Р -О- Р Фитол АДФ Изопентилпирофосфат АТФ (20 С) О- Р Полимери3-фосфо-5-пирофосфомевалонат зация Камфора Токоферолы (Вит. Е) Геранил (10 С) Монотерпены (10 С) Филлохиноны (Вит. К) Геранилгеранил (20 С) Каротиноиды (Вит. А) Фарнезил (15 С) Сквален (30 С) О2 Убихиноны (КоQ) 7-Дегидрохолесте рин (27 С) (Вит. D3) Кортикоиды (21 С) H2O (без О2 нет циклизации - нет стеринов) Ланостерин (30 С) Холестерин (27 С) Прогестерон (21 С) Желчные кислоты Андрогены (19 С) Минералокортикоиды Глюкокортикоиды (21 С) (21 С) Эстрон Тестостерон Андростендион Эстрогены (18 С) Андростерон Эстрадиол Стероиды - циклические производные полиизопреноидов Терпены - это полиизопреноидные цепочки Эстриол Холестерин Холестерин – высший, полициклический, ненасыщенный, вторичный спирт. Большая часть холестерина в крови находится в виде холестеридов. Холестериды - это сложные эфиры холестерина с высшими жирными кислотами: пальмитиновой, стеариновой или олеиновой. Холестерин и его эфиры нерастворимы в воде и образуют комплексные соединения со специфическими белками – липопротеинами (ЛП). Они – обязательные компоненты липопротеинов крови и клеточных мембран: влияют на физико-химические свойства плазматической мембраны регулируют: проницаемость мембран активность ферментов, интегрированных в нее. Из холестерина образуются вещества с высокой физиологической активностью: желчные кислоты, стероидные гормоны и провитамины группы D фитостероиды Холестерин поступает в организм с пищей и синтезируется из ацетилКоА в печени, мозге и, частично, в кишечнике. Из печени в ткани он попадает в составе липопротеинов низкой плотности (ЛПНП). Избыток холестерина из тканей удаляется липопротеинами высокой плотности (ЛПВП) в печень. Холестерин – это основной компонент ЛПНП и минорный ЛНОНП и ЛПВП. На уровень холестерина влияет: наследственность питание состояние эндокринных желез состояние внутренних органов (печень, почки) 1. Нарушение соотношения содержания холестерина и фосфолипидов в биомембранах приводит к злокачественному перерождению клетки. 2. Атеросклероз сопровождается гиперхолестеринемией и высоким содержанием в плазме крови ЛПНП при низком содержании ЛПВП. Образуются обильные отложения холестерина и его эфиров на внутренней поверхности кровеносных сосудов. Ограничение кровотока путем сужения просвета сосудов мозга и сердца при атеросклерозе может приводить к инсульту или инфаркту миокарда. Существует корреляционная зависимость между высокой концентрацией холестерина в крови и вероятностью развития атеросклероза. Степень риска кардиососудистых заболеваний обратнопропорциональна концентрации холестерина во фракции ЛПВП. Определение общего холестерина и холестерина в ЛПВП представляет интерес для оценки риска кардиососудистых и ряда других заболеваний. Общий холестерин – это весь холестерин, содержащийся в ЛП. (таблица Классы липопротеинов крови). 3.Повышение уровня холестерина наблюдается также при: семейной гиперхолестеринемии (ксантоматозе) гипотиреозе декомпенсированном сахарном диабете нефротическом синдроме хроническом гепатите билиардном циррозе механической желтухе гипопротеинемии (идиопатической, на фоне нефроза или хронического гепатита) липидемии (идиопатической, семейной) 4.Понижение концентрации холестерина характерно при: остром гепатите болезни Гоше гипертиреозе острых инфекциях кахексии анемии остром панкреатите недоедании дефиците аполипопротеинов 5. Исследуется роль холестерина в процессах синаптической пластичности, нейродегенерации и развитии болезни Альцгеймера. 6. Фитостероиды ашвагандхи: оптимизируют обменные процессы в предстательной и семенных железах нормализуют функциональное состояние сперматозоидов, коллоидное равновесие и рН спермы. препятствуют переходу тестостерона в дегидротестостерон (у пожилых мужчин) предотвращают развитие аденомы и аденокарциномы предстательной железы Классы липопротеинов крови Название Размер, НМ Свойства Состав, % Место синтеза ФЛ Хол. Белок 7 4 слизистая 2 оболочка кишечника (энтероциты) 18 15 1. слизистая 10 (+7) оболочка (энтероциты) 2. печень (гепатоциты) 21 47 1. плазма крови 25 2. гепатоциты 25 25 1. плазма крови 45 2. гепатоциты 1. Хиломикроны 120 – 300 ТАГ 85 2. ЛПОНП (пре–β–ЛП) 30 – 80 50 3. ЛПНП (β–ЛП) 4. ЛПВП (β - ЛП) 20 7 5 – 30 5 5. ЛПОВП 5› жирные кислоты алибумин плазма крови 6. Аполипопротеины (апобелки или апо) коллоидный раствор - 100 гепатоциты Функции транспорт ТАГ транспорт ТАГ транспорт Хол. внутрь клеток (атерогенные) транспорт Хол. из клеток (антиатерогенные) перенос ЖК по кровотоку образование ЛП, перенос липидов по кровотоку, лиганды к рецепторам (структурная, транспортная) Классификация ЛП основаны на различиях в их свойствах: 1. гидратированной плотности 2. скорости флотации в гравитационном поле 3. электрофоретической подвижности 4. апопротеиновом составе К (атерогенность) = Х общ – Х ВП Х ВП N = > от 2 до 4 У человека в организме всего 140 г. холестерина. С пищей получает 2-3 г/сут экзогенного холестерина. Он ингибирует синтез эндогенного холестерина. Эйкозаноиды Эйкозаноиды – это липиды: производные полиеновых жирных кислот с 20 атомами углерода («эйкоза» по-гречески 20) с коротким периодом полужизни (секунды) синтезируются почти всеми типами клеток (кроме эритроцитов) модулируют внутриклеточное действие гормонов через ц-АМФ, цГМФ и Са+2 как гормоны местного действия вызывают эффект по аутокринному (местно) или паракринному (на соседние клетки) механизму через специфические рецепторы. Эйкозаноиды делят на три основные группы по названию клеток, в которых они были впервые обнаружены: 1) Эйлер предполагал, что простагландины (включая простациклины) являются секретом предстательной железы – простаты. 2) тромбоксаны были найдены в тромбоцитах 3) лейкотриены – в лейкоцитах Исходными субстратами для синтеза эйкозаноидов служат полиеновые жирные кислоты с 20 атомами углерода: арахидоновая (20:4 ω-6) эйкозапентаеновая (20:5 ω-3). Они поступают с пищей или синтезируются из незаменимых жирных кислот с 18 атомами С, которые также поступают с пищей. Схема синтеза 20-ти углеродных полиеновых жирных кислот: ω-6 кислоты: линолевая – 18:2 (9,12) → 20:3 (8,11,14) → 20:4 (5,8,11,14) – арахидоновая. ω-3 кислоты: линоленовая – 18:3 (9,12,15) →→ 20:5 (5,8,11,14,17) – эйкозапентаеновая. В процессе ресинтеза такие полиеновые жирные кислоты с 20 атомами С и с 3-5 двойными связями оказываются во 2-м положении в структуре фосфоглицеридов, которые в составе липопротеинов с кровотоком разносятся к тканям организма и с помощью рецепторов встраиваются в клеточные мембраны. Арахидоновая кислота преобладает среди этих кислот. Полиеновые кислоты из фосфолипидных мембран освобождаются под действием фосфолипазы А2, после ее активации. Далее, циклооксигеназа образует за счет двух двойных связей циклопентановое кольцо с участием 8-го и 12-го атомов С и присоединяет 2 молекулы кислорода. Образуется нестабильный, первичный простагландин PGG2. Пероксидаза быстро восстанавливает его до PGH2. Донором водорода служит глутатион. Каждый из этих ферментов представляет каталитический центр фермента простагландинсинтазы, состоящий из 2 субъединиц. Последующие превращения PGH2 зависят от типа тканей. Например, тромбоксаны в основном синтезируются в тромбоцитах, простациклины – в клетках эндотелия сосудов. Липоксигеназа образует соединения с тремя сопряженными двойными связями («лейкотриены» А, В, С, D, E). В отличие от простаноидов они: не содержат циклической структуры, содержат 4 двойных связи могут образовывать с глутатионом комплексы. Так, например, лейкотриен А превращается в лейкотриен С, который после отщепления глутамильного остатка, становится лейкотриеном D. Далее, после потери остатка глицина, образуется лейкотриен Е. Схема синтеза эйкозаноидов. Эссенциальные жирные кислоты→→ЛП сыворотки крови→→фосфолипиды мембран ресинтез кровоток O OH CH3 Арахидоновая кислота Липооксигеназа O 6 -Аспирин (необратимо) -Индометацин (обратимо) 9 8 O -Витамин Е O 5 Циклооксигеназа O 5 O - O 7 9 11 O CH3 14 Лейкотриен LTA4 Гидролаза CH3 11 12 15 - (R7) (R8) O OH Простагландин PGG4 (нестабильный) Глутатион 2 Глутатион-SH LTB4 LTC4 Пероксидаза R-Глу Глу-S-S-Глу Гли LTE4 9 LTD4 O R7 8 O CH2 9 5 8 O O 11 O 12 O R8 Тромбоксан TXA2 11 OH PGE2 12 (R8) OH R7 9 R8 11 8 R7 9 11 12 R8 R4 O OH HO 8 15 (R7) Простагландин PGI2 O 9 CH3 11 12 - 8 R7 9 11 12 O OH PGD2 PGF2 R8 7 8 12 R8 OH Простациклин PGI2 Инактивируются простаноиды путем окисления до соответствующих 15-кетопроизводных. Каждая из групп эйкозаноидов отличается по числу двойных связей в боковых цепях. Число двойных связей обозначается цифровым индексом, например PGE2. Оно зависит от полиеновой кислоты – предшественника. Две двойные связи используются при образовании цикла, а оставшиеся в радикалах двойные связи определяют серию простагландина: 1, 2, 3 и 4. А. 20:3 (8, 11, 14) PGE1 Б. PGF1 20:4 (5,8, 11, 14) PGI1 PGE1 В. PGF1 20:5 (5,8, 11, 14,17) TXA3 PGE1 TXA3 PGI1 Поскольку арахидоновая кислота содержится в составе фосфолипидов в большом количестве даже при обычном рационе, то преобладают простагландины серии 2. Однако, при рационе, обогащенном рыбьим жиром с высокой концентрацией 20:5 жирной кислоты, синтез эйкозаноидов серии 3 увеличивается. В разных тканях образуются различные эйкозаноиды. Обычно в каждом типе клеток синтезируется преимущественно один тип эйкозаноидов. Они выходят из клетки и действуют на рецепторы соседних клеток. Время такого действия ограничивается несколькими минутами, однако этого оказывается достаточно, чтобы вызвать существенные изменения метаболизма в тех тканях, где они образовались. Существует много типов рецепторов и для каждого эйкозаноида есть несколько типов рецепторов. Они располагаются в мембране клеток рядом с аденилатциклазой. Некоторые взаимодействуют с G-белками аденилатциклазного комплекса. Таким образом, они могут модулировать активность аденилатциклазы. Например, PGE1 увеличивает количество ц-АМФ в некоторых клетках, а PGE2 уменьшает. Ответ клетки на действие эйкозаноида определяется ее типом. По сумме признаков эйкозаноиды определяют как гормоны местного действия: 1. они образуются не в эндокринных железах, а во всех органах и тканях 2. быстро инактивируются путем окисления до менее активных соединений 3. за один круг кровообращения в печени и легких инактивируется около 80% этих соединений 4. низкая концентрация в крови не позволяет им вызывать ответ в клетках-мишенях. Только при некоторых патологических состояниях, в результате резкого увеличения концентрации в крови, эйкозаноиды могут оказывать системное действие на гладкую мускулатуру. Сбалансированность мощного фармакологического действия эйкозаноидов из разных групп можно считать очень важной особенностью их обмена. Примером могут служить простациклины и тромбоксаны. Регуляция тонуса стенок сосудов и агрегации тромбоцитов эйкозаноидами. Показатель 1. Место синтеза 2.Агрегация тромбоцитов 3. Сосуды 4. Эффект Простациклины Эндотелий сосудов Ингибируют Расширяют Жидкая кровь Тромбоксаны Тромбоциты Активируют Сокращают Тромб, инфаркт При патологии или при действии фармакологических средств равновесия между свертывающей и противосвертывающей системами крови может смещаться в любую сторону. При разрушении клеток эндотелия, например, в результате образования атеросклеротических бляшек, синтез простациклинов снижается. Тромбоциты при этом активируются в месте контакта с поврежденной стенкой сосуда. Секретируются тромбоксаны. Это стимулирует образование тромба в области повреждения эндотелия сосудов. Повышается степень риска развития инфаркта. Напротив, риск развития инфаркта миокарда резко снижается у людей, в диете которых присутствует большое количество рыбьего жира. У них реже образуются тромбы в сосудах сердца. Это связано с тем, что в рыбьем жире содержится большое количество эйкозапентаеновой кислоты (20:5 ω-3), из которой образуются простаноиды третьей серии. Тромбоксаны этой серии слабо стимулируют, а простациклины сильно ингибируют агрегацию тромбоцитов. Это препятствует тромбообразованию. В общем, при определенных условиях эйкозаноиды стимулируют: 1. сокращение гладкой мускулатуры (сосуды, бронхи, матка) 2. биосинтез стероидных гормонов 3. секрецию желудочного сока и синтез мукоидов, защищающих стенки желудка 4. гормонозависимые липазы 5. болевые реакции 6. воспалительные реакции 7. агрегацию тромбоцитов Аспирин снимает эти эффекты. Ацетильный остаток переносится с молекулы аспирина на ОН-группу циклооксигеназы (ацелирование) и необратимо инактивирует ее. Индометацин обратимо ингибирует этот фермент и также, как аспирин проявляет противовоспалительное действие. Глюкокортикоиды действуют как противовоспалительный препараты, индуцируя синтез липокортинов, которые ингибируют фосфолипазу А2. Адреналин + Глицерофосфолипиды мембран (Рецептор) Кортикостероиды (противовоспалительное действие) Фосфолипаза (А2, С) _ Аспирин (необратимо), индометацин (обратимо) _ ингибируют 8 5 + Липопротеины сыворотки крови 1 O OH CH3 (20) 11 14 15 Арахидоновая кислота Простагландинсинтаза (циклооксигеназа) Липоксигеназа (лейкоциты, тромбоциты, макрофаги) Простагландины Н2 (ПГН2) ПГ F2 альфа Родостимулятор, обезболивающее действие Тромбоксан А2 число двойных связей ПГ I2 Лейкотриены A, B, C, D, E Способствуют хемотаксису и развитию аллергических реакций Простациклин I2 Тх В2 Способствует агрегации тромбоцитов, тромбообразование Антитромбообразующие свойства Стимулируют: Аспирин снимает эти эффекты (аспирин как антитромботическое средство) 1) Сокращение гладкой мускулатуры (сосуды, бронхи, матка) 2) Биосинтез стероидных гормонов 3) Секреция желудочного сока и синтез мукоидов, защищающих стенку желудка 4) Гормонзависимые липазы 5) Болевые реакции 6) Воспалительные реакции 7) Агрегацию тромбоцитов Прооксиданты 1.Молекулярны кислород 2.Металлы переменной валентности 3.Пестициды 4.Раионуклиды 5.Полициклические, ароматические углеводороды 6.Нитрозамины 7.Продукты метаболизма некоторых (антибиотики тетрациклинового ряда) лекарственных препаратов 8.Любые свободно-радикальные частицы, образующиеся под влиянием УФоблучения, йонизирующей радиации, озонирования, гипербарической оксигенации и др. 9.Функционирование оксидаз 10. Аутоокисление тетрагидроптеринов гидрохинонов, флавинов, тиолов, катехоламнов, 11.Стресс Антиоксиданты Неферментативная защита Ферментативна защита 1.Аскорбат, цитрат 8.Глуттион 2.Витамины Е, К 9.Липоевая кислота 2.Супероксиддисмутаза (Cu, (восстановленная) Zn, Mn-содержащий 3.Убихинон (KoQ) 4.Витамин каротин А, β- 10.Карнозин 11.Цистеин, метионин 1.Цитохром Р-450 металлофермент) 3.Каталаза 5.Zn, Se 12.Ансерин 4.Глутатионпероксидаза 6.Биофлавоноиды 13.Полиамины (Se-зависимая) 7.Фосфолипиды биомембран 5.Длутатионредуктаза (НАДФН) 6.Церулоплазмин (Си+2содержащий АФК (активные формы кислорода) через сигнальные клетки запускают апоптоз, в том числе клеток опухоли. Антиоксиданты могут тормозить этот процесс, препятствуя уничтожению раковых клеток. Схема расщепления олефинов синглетным кислородом с образованием двух молекул альдегидов R H R + О2 R1 H Олефин R1 H O Н R O H + R O 1 Н O Альдегиды Перекись олефина Схема участия молекулярного кислорода в окислительных превращениях субстратов (S) в клетке Sвосст. оксидазный путь : О2 1/2 О2 Sокисл. H2O SH монооксигеназный 1/2 О 2 путь: диоксигензный путь: S-OH + H2O SH О2 S-OОH Малоновый диальдегид (МДА) – конечный продукт свободнорадикального окисления полиненасыщенных высших жирных кислот (ВЖК) из фосфолипидов биологических мембран. Свободными радикалами (R) называют атомы, молекулы или структурные фрагменты молекул, имеющие на внешних орбиталях неспаренные электроны. Радикал может быть нейтральным или иметь положительный либо отрицательный заряд. В силу исключительно высокой реакционной способности радикалы могут взаимодействовать с различными молекулами, вызывая их повреждение. До настоящего времени описано около 8000 свободных радикалов. В организме они выполняют защитные функции (окисление ксенобиотиков, бактерицидное действие), регулируют проницаемость мембран, деление и рост клеток, иммунные реакции и интенсивность обмена веществ. Активация перекисных и свободно-радикальных процессов (синдром пероксидации) – это фактор патогенеза: атеросклероза ИБС инфаркта инсульта язвенной и ожоговой болезни онкологических, воспалительных, инфекционных заболеваний синдрома адаптационного перенапряжения хронической усталости диабета Синдром пероксидации проявляется также при: снижении потребления биоантиоксидантов стрессе любого происхождения действии синтетических лекарств ксенобиотиков и наркотиков пониженных температур гиподинамии старении организма избыточном потреблении в пищу жиров и углеводов гипоксических состояниях воздействии вибрации электромагнитных полей, радиоактивного ультрафиолетового и др. излучений Универсальный характер синдрома пероксидации превращает его в неспецифический фактор патогенеза большинства заболеваний и состояний организма, объединяемых понятиями «оксидативный стресс» и «свободно-радикальная патология». Основным источником образования ОН в большинстве живых организмов являются реакции: Fe2++H2O2 Fe3+ + ОН + ОН (1) Fe2++HOCl Fe3+ + ОН + Cl (2) HOCl+О2 ОН + Cl + O2 (3) Реакция (1) известна как реакция Фентона. Она протекает с участием свободных ионов металлов переменной валентности, например Fe или Cu, а также их хелатных комплексов с органическими кислотами, фосфатами, АДФ, ЭДТА, цитратом, гистидином и др. Источники образования АКМ в организме млекопитающих АКМ Источник образования О2 Одновалентное восстановление О2 ксантиноксидазой, НАДФН-оксидазой фагоцитов, оксидазами Супероксидный анион-радикал аминокислот; образование в цепи транспорта электронов митохондрий и микросом; при автоокислении оксигемоглобина в метгемоглобин и адреналина в адренохром HO2 Присоединение Н+ к О2 в кислой среде (рК=4,8); Пергидроксильный реакция Н2О2 с R; промежуточный продукт в реакциях радикал Н2О2 восстановленных флавинов с О2 Двухэлектронное восстановление О2 ксантиноксидазой и Пероксид водорода флавиновыми оксидазами; реакция дисмутации О2 с участием или без участия супероксиддисмутазы NO Оксид азота 1 О2 Синглетный Окисление L-аргинина конституциональными индуцибельными NO-синтетазами и Сопутствующий продукт в реакциях с пероксидазами, при спонтанной дисмутации О2, при взаимодействии кислород Н2О2 с NO; фотоиндуцированные реакции HOCl/OCl Реакция Н2О2 с миелопероксидазой нейтрофилов, макрофагов и моноцитов, а также с пероксидазой эозинофилов Хлорноватистая кислота/ гипохлорит-анион ОН Гидроксильный радикал Разложение Н2О2 ионами металлов переменной валентности; при радиолизе воды; при микросомальном окислении; при взаимодействии HOCl/OCl с О2 и Fe2+ RO2 Пероксильный Взаимодействие О2 с R; реакция О2, ОН, 1О2, RO с ненасыщенными липидами и жирными кислотами радикал RO Алкоксильный радикал Разложение органических перекисей ионами металлов переменной валентности Антиоксиданты плазмы крови Антиоксидант Гаптоглобин/ гемопексин Церулоплазмин Способ действия Связывают свободный Hb/гем. Относятся к белкам “острой фазы” Окисляет ионы Fe2+ в Fe3+ (ферроксидазная активность). Взаимодействует с О2 и HOCl/OCl. Относится к белкам “острой фазы” Трансферрин, Связывают ионы Fe3+. Препятствуют их участию в лактоферрин индуцированиии реакций свободнорадикального окисления Альбумин Связывает ионы Cu2+. Является эффективным перехватчиком HOCl/OCl-. Транспортирует билирубин ЭЦ-СОД SH-группы белков Перехватывает О2 Взаимодействуют со свободными радикалами (О 2, ОН, NO, RO2), 1O2 и HOCl/OCl Аскорбиновая См. табл. 4 кислота Мочевая кислота Перехватывает RO2, RO, ОН, связывает ионы железа и меди. Взаимодействует с HOCl/OCl Глюкоза Перехватывает ОН (константа скорости реакции 2,2х109 М1с1 [133]) Билирубин Транспортируется альбумином. Защищает связанные с альбумином жирные кислоты от процесса пероксидации -Токоферол Жирорастворимый цепь-обрывающий антиоксидант плазмы крови. Перехватывает RO2, RO. Является тушителем 1О2 -Каротин, ликопин Перехватывают RO2, RO. Являются тушителями 1О2 Антиоксидантные свойства аскорбиновой кислоты № Свойства 1 Перехватывает О2 и HO2 (константа скорости реакции 2,7х105 М1с1 при рН 7,4) 2 Тушит 1О2 3 Перехватывает ОН (константа скорости реакции 1,2х1010 М1с1 при рН 7 [133]) 4 Перехватывает HOCl/OCl 5 Взаимодействует с водорастворимыми RO2, ферилл радикалами Hb и миоглобина, а также тиил и сульфенил радикалами 6 Восстанавливает феноксильные радикалы -токоферола в токоферол 7 Восстанавливает радикалы мочевой кислоты, образующиеся после ее взаимодействия с ОН и другими прооксидантами 8 Защищает липопротеины низкой плотности плазмы крови от окислительной модификации, индуцированной ионами Cu2+ 9 Защищает от оксидантов, присутствующих в сигаретном дыме Окислительному действию АФК подвержены любые органические субстраты: липиды, аминокислоты, белки, углеводы, ДНК и РНК. Однако молекулы липидов, имеющие в своем составе легкоокисляющиеся ненасыщенные жирные кислоты, чаще всего становятся мишенью для АФК, поэтому процесс ПОЛ является одним из наиболее распространенных свободнорадикальных процессов в организме. В процессе ПОЛ выделяют стадии зарождения цепи, продолжения цепи, разветвления цепи и обрыва цепи: зарождение цепи RH + Х R + ХН (4) продолжение цепи R + O2 RO2 (5) RO2 + RH ROOH + R (6) разветвление цепи обрыв цепи ROOH + Fe2+ RO + OH + Fe3+ (7) RO + RH ROH + R (8) R + R RR (9) RO2 + R ROOR (10) RO2 + RO2 P* P + h (11) В настоящее время постоянно пополняется обширный перечень патологических состояний организма человека, сопровождающихся развитием оксидантного стресса. Так, установлено, что активация реакций свободнорадикального окисления и, в частности, ПОЛ наблюдается при ишемических и реоксигеннационных эндокринопатиях, повреждениях, воспалительных стрессах, токсикозах, заболеваниях различной этиологии, иммунных нарушениях, злокачественном росте, а также дегенеративных болезнях или заболеваниях пожилого возраста, включая атеросклероз, диабет, гипертонию, катаракту, артриты и др. Антиоксиданты АКМ Липиды Пероксидное окисление липидов Белки Поперечные сшивки ДНК Разрывы, поперечные сшивки Повреждение клетки Антиоксиданты Последствия взаимодействия АКМ (активных кислородных молекул) с биологически важными молекулами и участие антиоксидантов в регуляции этого процесса Значительные количества АФК продуцируют фагоцитирующие клетки (нейтрофилы, моноциты, эозинофилы, базофилы периферической крови, тканевые макрофаги и т.д.) при взаимодействии с возбудителями инфекции, иммунными комплексами или пылевыми частицами. АФК, образуемые фагоцитами, являются важным элементом защиты организма от чужеродных антибактериальными, объектов, антипаразитарными, так как обладают противоопухолевыми свойствами Номенклатура АФК (активные формы кислорода) Species O− O2 • − O3 O3 − HO• HO2• Systematic IUPAC Name oxide(1-) dioxide(1-) trioxygen trioxide(1-) hydroxyl hydrogen dioxide Alternative/Comments hydroxyl radical without proton superoxide ozone ozonide not hydroxy, hydroxide is OH− hydrodioxyl, or hydroperoxyl, but perhydroxyl does not make sense HO2− hydrogen dioxide(1-) hydrogenperoxide(1-) H2O2 hydrogen peroxide RO• alkoxyl not alkoxy ROO• alkyldioxyl alkylperoxyl not peroxy ROOH alkyl hydroperoxide ONOO− oxoperoxonitrate (1-) peroxynitrite ONOOH hydrogen oxoperoxonitrate peroxynitrous acid NO• monoxide nitric nitric oxide