О радиоизотопной датировке
реклама
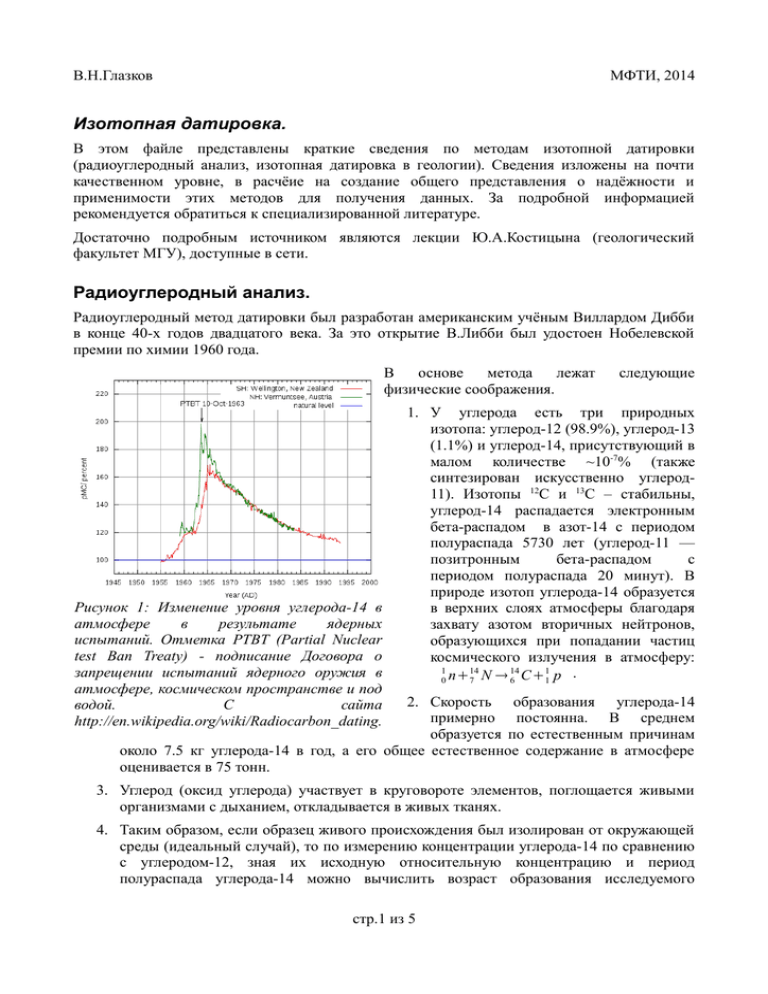
В.Н.Глазков МФТИ, 2014 Изотопная датировка. В этом файле представлены краткие сведения по методам изотопной датировки (радиоуглеродный анализ, изотопная датировка в геологии). Сведения изложены на почти качественном уровне, в расчёие на создание общего представления о надёжности и применимости этих методов для получения данных. За подробной информацией рекомендуется обратиться к специализированной литературе. Достаточно подробным источником являются лекции Ю.А.Костицына (геологический факультет МГУ), доступные в сети. Радиоуглеродный анализ. Радиоуглеродный метод датировки был разработан американским учёным Виллардом Дибби в конце 40-х годов двадцатого века. За это открытие В.Либби был удостоен Нобелевской премии по химии 1960 года. В основе метода лежат физические соображения. Рисунок 1: Изменение уровня углерода-14 в атмосфере в результате ядерных испытаний. Отметка PTBT (Partial Nuclear test Ban Treaty) - подписание Договора о запрещении испытаний ядерного оружия в атмосфере, космическом пространстве и под водой. С сайта http://en.wikipedia.org/wiki/Radiocarbon_dating. следующие 1. У углерода есть три природных изотопа: углерод-12 (98.9%), углерод-13 (1.1%) и углерод-14, присутствующий в малом количестве ~10-7% (также синтезирован искусственно углерод11). Изотопы 12C и 13C – стабильны, углерод-14 распадается электронным бета-распадом в азот-14 с периодом полураспада 5730 лет (углерод-11 — позитронным бета-распадом с периодом полураспада 20 минут). В природе изотоп углерода-14 образуется в верхних слоях атмосферы благодаря захвату азотом вторичных нейтронов, образующихся при попадании частиц космического излучения в атмосферу: 1 14 14 1 . 0 n+ 7 N → 6 C+ 1 p 2. Скорость образования углерода-14 примерно постоянна. В среднем образуется по естественным причинам около 7.5 кг углерода-14 в год, а его общее естественное содержание в атмосфере оценивается в 75 тонн. 3. Углерод (оксид углерода) участвует в круговороте элементов, поглощается живыми организмами с дыханием, откладывается в живых тканях. 4. Таким образом, если образец живого происхождения был изолирован от окружающей среды (идеальный случай), то по измерению концентрации углерода-14 по сравнению с углеродом-12, зная их исходную относительную концентрацию и период полураспада углерода-14 можно вычислить возраст образования исследуемого стр.1 из 5 В.Н.Глазков МФТИ, 2014 образца. Нарушение этих предположений вносит погрешность в метод. Однако к настоящему времени по сравнению с образцами, точно датируемыми другими методами (в частности, по годовым кольцам старых деревьев можно проследить историю на 11000 лет назад, по росту кораллов до еще более древнего периода), получена калибровка метода радиоуглеродного анализа, учитывающая такие эффекты как изменение интенсивности космического излучения, зависимость равновесной концентрации углерода-14 от Рисунок 2: Масс-спектрометр, используемый широты, активизации вулканических для радиоуглеродного анализа. С сайта процессов. http://en.wikipedia.org/wiki/Radiocarbon_dating. Интересно отметить, что с началом промышленной революции в 19 веке началось активное сжигание ископаемого топлива, не содержащего практически углерода-14, что привело к смещению изотопного баланса в сторону от равновесного. Ядерные испытания середины 20 века привели к образованию количества углерода-14, сравнимого с естественным (рисунок 1). Эти рукотворные факторы приводят к тому, что метод радиоуглеродного анализа применим к образцам, полученным в последние 100-200 лет, только с оговорками. В то же время, исследование перемещения произведённого при ядерных испытаниях углерода-14 позволило лучше понять, как перемешивается и связывается углерод — то есть получить дополнительную проверку и калибровку метода. Метод радиоуглеродного анализа применяется к образцам живого происхождения, позволяет достаточно надёжно датировать образцы возрастом от 100-200 лет и до 60-70 тысяч лет в прошлое. Верхний предел связан, в основном с относительно малым (на этом масштабе) периодом полураспада: за 60000 лет проходит около 10 периодов полураспада, то есть концентрация углерода-14 уменьшается в 210≈1000 раз, при том, что и исходная концентрация была ничтожна. Измерение количества углерода-14 производится по активности бета-распадов (образец либо сжигается до образования газа CO2, который помещается в камеру детектора, либо растворяется в сцинцилирующей жидкости) или по масс-спектрометрии, непосредственно измеряющей количество атомов углерода (рисунок 2). стр.2 из 5 В.Н.Глазков МФТИ, 2014 Изотопная датировка в геофизике. В геофизике используются методы изотопной датировки, основанные на использовании более долгоживущих изотопов, так как интересующие «геологические» масштабы времени типично измеряются миллионами, сотнями миллионов и даже миллиардами лет. Основной физический принцип остаётся тем же, что и для радиоуглеродного анализа: необходимо найти связанные распадом изотопы. Тогда по их относительной концентрации можно вычислить сколько образовалось или сколько распалось ядер с момента формирования исследуемой горной породы. При изучении геологических масштабов времени может показаться, что становится невозможным узнать исходное количество изотопов. Однако на самом деле принципиально важным оказывается только достаточно легко выполнимое чтобы исследуемая порода Рисунок 3: Содержание изотопов требования, кислорода в метеоритах разного оказывалась изолированной с момента своего происхождения. Wiechert et.al, Science v.294 формирования — что для твёрдых пород выполняется почти автоматически. p.345 Для того чтобы избавиться от неопределённости с исходным изотопным составом исследуется одновременно несколько образцов из одновременно образовавшихся пород. Несмотря на близость химических свойств изотопов, химическая кинетика и термодинамика изотопов различна, поэтому при формировании пород в несколько различных условиях распределение изотопов в различных образцах будет отличаться (так называемое фракционирование изотопов). Подчеркнём, что в геофизике речь идёт обычно о десятках и сотнях миллионов, а иногда и о миллиардах лет, поэтому промежуток формирования пород в миллион лет является небольшим в этом масштабе, а условия (температура и химическое окружение) за это время конечно могут измениться. Поэтому в ходе формирования исследуемой породы (месторождения, небесного тела) в разных его точках в одних и тех же химических соединениях (например в окислах или солях) окажется разное стартовое соотношение изотопов. Это явление называется фракционированием изотопов. Оно позволяет в частности сразу различить образцы, формирующиеся в существенно разных условиях (см. рисунок 3). Для качественного рассмотрения возьмём упрощённую модель. Пусть есть элемент A и его радиоактивный изотоп A', распадающийся в изотоп (для простоты - стабильный) B: A ' → B с периодом полураспада T 1 /2 . Пусть в начальный момент времени в породах присутствовал естественный изотоп B в количестве N (0) , концентрацию которого мы B примем постоянной (иначе образуются породы другого типа, в которых общее содержание изотопов A и B отлично). Количество изотопа B в момент времени t равно стр.3 из 5 В.Н.Глазков МФТИ, 2014 (0) ( −t /T N B=N (0) B + N A' 1−2 1/2 ) , количество изотопа A' в тот же момент времени −t / T N A ' =N (0) A' 2 1 /2 . Нормируя на неизменную концентрацию N B (t)− N (0) N (t) B = A ' ( 2t /T −1 ) . NA NA стабильного изотопа A, получаем: 1/2 Обратите внимание, что N A , N A ' (t) и N B (t) - это измеренные сейчас количества ядер разного типа. Отношение стартовых количеств изотопов A и A' было различно, поэтому в серии образцов мы получим разные отношения N A ' (t)/ N A и N B (t)/ N A . Если (как это неявно предполагается) стабильный изотоп A доминирует, то различие концентрации изотопа A по серии образцов даст эффект следующего порядка малости. Таким образом, если по серии образцови нормировнаные современные концентрации изотопа B линейно зависят от нормированной современной концентрации изотопа A', то по наклону этой прямой можно определить возраст серии. Сдвиг же прямой зависит от исходной естественной концентрации изотопа B, что, в частности позволяет различить серии образцов разного происхождения. В геохимическом используются различные изотопов, например: анализе системы • K-Ar. Калий-40 распадается (позитронным бета-распадом или К-захватом) в аргон-40 (вероятность около 10%) с периодом полураспада 1.25 млрд. лет. • Rb-Sr. Рубидий-87 распадается в стронций-87 электронным бета распадом с периодом полураспада 48.81 млрд.лет. • Sm-Nd. Самарий-147 Рисунок 4: Изотопный анализ (Rb-Sr) проб распадается в неодим-143 золоторудного месторождения Мурунтау. альфа-распадом с периодом Определённый возраст 273.1 млн.лет. Точки полураспада 106 млрд.лет. полученные на разных сериях образцов ложатся на семейство параллельных прямых с одним наклоном. Из • U-Th-Pb. Это целое семейство лекций Ю.А.Костицына. изотопов, встречающихся одновременно, что позволяет проводить более достоверный анализ. Торий-232 превращается в свинец-208 через цепочку альфа- и бета-распадов с периодом полураспада 14 млрд.лет; уран-238, также через цепочку распадов, превращается в свинец-206, период полураспада равен 4.47 млрд. лет; уран-235 — в свинец-207 с периодом полураспада 0.70 млрд.лет. стр.4 из 5 В.Н.Глазков МФТИ, 2014 Изотопная датировка является одним из главных источников нашего знания о возрасте Земли, Луны и Солнечной системы (рисунки 4, 6, 5, 7). Данные полученные различными методами указывают, на то что самые древние горные породы формировались на Земле около 4 млрд. лет назад. Рисунок 6: Изотопная датировка (Sm-Nd) лунных пород, доставленных экспедицией "Апполон-17". Из лекций Ю.А.Костицына. Рисунок 5: Изотопный анализ (Sm-Nd) возраста метеоритов-хондритов. Прямая соответствует возрасту 4.6 млрд.лет. Из работы Jacobsen S.B., Wasserburg G.J., Sm-Nd isotopic evolution of chondrites. // Earth and Planetary Science Letters, 1980. 50: 139-155. Рисунок 7: Изотопная датировка (Sr-Rb) гнейсов (древних горных пород) Гренландии. Moorbath, S, Allaart, JH, Bridgwater, D and McGregor, VR (1977). "Rb-Sr ages of early Archaean supracrustal rocks and Amitsoq gneisses at Isua." Nature 270: 43-45. стр.5 из 5