Gastro 3_2005.qxd - Сучасна гастроентерологія
реклама
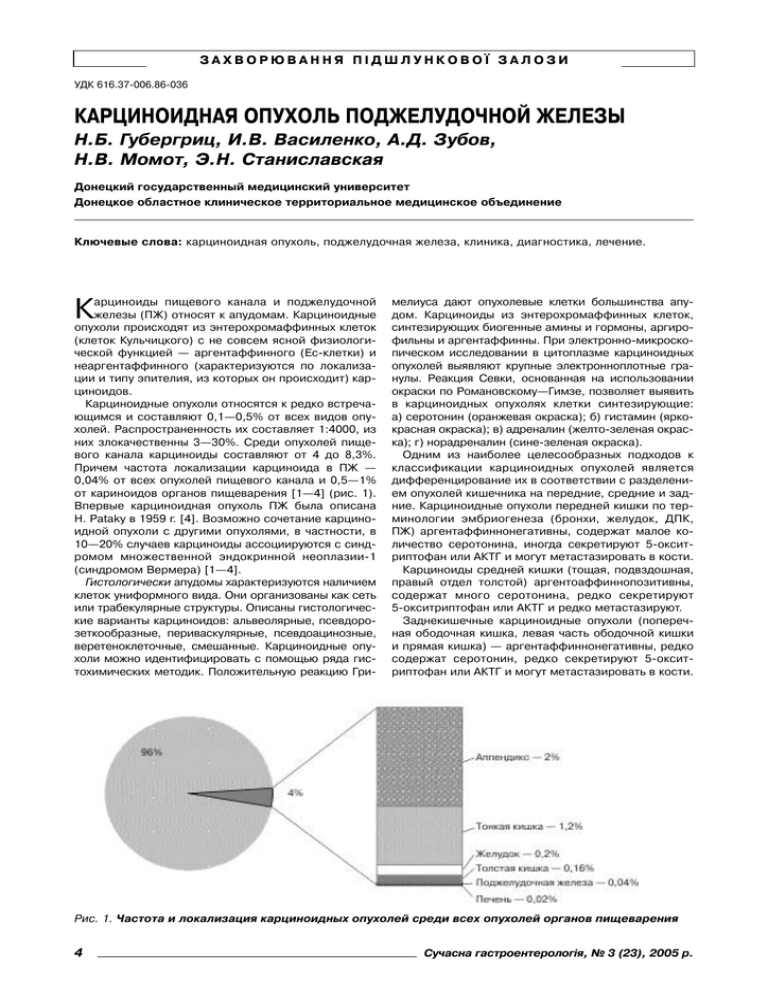
ЗАХВОРЮВАННЯ ПІДШЛУНКОВОЇ ЗАЛОЗИ УДК 616.37!006.86!036 КАРЦИНОИДНАЯ ОПУХОЛЬ ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ Н.Б. Губергриц, И.В. Василенко, А.Д. Зубов, Н.В. Момот, Э.Н. Станиславская Донецкий государственный медицинский университет Донецкое областное клиническое территориальное медицинское объединение Ключевые слова: карциноидная опухоль, поджелудочная железа, клиника, диагностика, лечение. К арциноиды пищевого канала и поджелудочной железы (ПЖ) относят к апудомам. Карциноидные опухоли происходят из энтерохромаффинных клеток (клеток Кульчицкого) с не совсем ясной физиологи! ческой функцией — аргентаффинного (Ес!клетки) и неаргентаффинного (характеризуются по локализа! ции и типу эпителия, из которых он происходит) кар! циноидов. Карциноидные опухоли относятся к редко встреча! ющимся и составляют 0,1—0,5% от всех видов опу! холей. Распространенность их составляет 1:4000, из них злокачественны 3—30%. Среди опухолей пище! вого канала карциноиды составляют от 4 до 8,3%. Причем частота локализации карциноида в ПЖ — 0,04% от всех опухолей пищевого канала и 0,5—1% от кариноидов органов пищеварения [1—4] (рис. 1). Впервые карциноидная опухоль ПЖ была описана H. Pataky в 1959 г. [4]. Возможно сочетание карцино! идной опухоли с другими опухолями, в частности, в 10—20% случаев карциноиды ассоциируются с синд! ромом множественной эндокринной неоплазии!1 (синдромом Вермера) [1—4]. Гистологически апудомы характеризуются наличием клеток униформного вида. Они организованы как сеть или трабекулярные структуры. Описаны гистологичес! кие варианты карциноидов: альвеолярные, псевдоро! зеткообразные, периваскулярные, псевдоацинозные, веретеноклеточные, смешанные. Карциноидные опу! холи можно идентифицировать с помощью ряда гис! тохимических методик. Положительную реакцию Гри! мелиуса дают опухолевые клетки большинства апу! дом. Карциноиды из энтерохромаффинных клеток, синтезирующих биогенные амины и гормоны, аргиро! фильны и аргентаффинны. При электронно!микроско! пическом исследовании в цитоплазме карциноидных опухолей выявляют крупные электронноплотные гра! нулы. Реакция Севки, основанная на использовании окраски по Романовскому—Гимзе, позволяет выявить в карциноидных опухолях клетки синтезирующие: а) серотонин (оранжевая окраска); б) гистамин (ярко! красная окраска); в) адреналин (желто!зеленая окрас! ка); г) норадреналин (сине!зеленая окраска). Одним из наиболее целесообразных подходов к классификации карциноидных опухолей является дифференцирование их в соответствии с разделени! ем опухолей кишечника на передние, средние и зад! ние. Карциноидные опухоли передней кишки по тер! минологии эмбриогенеза (бронхи, желудок, ДПК, ПЖ) аргентаффиннонегативны, содержат малое ко! личество серотонина, иногда секретируют 5!оксит! риптофан или АКТГ и могут метастазировать в кости. Карциноиды средней кишки (тощая, подвздошная, правый отдел толстой) аргентоаффиннопозитивны, содержат много серотонина, редко секретируют 5!окситриптофан или АКТГ и редко метастазируют. Заднекишечные карциноидные опухоли (попереч! ная ободочная кишка, левая часть ободочной кишки и прямая кишка) — аргентаффиннонегативны, редко содержат серотонин, редко секретируют 5!оксит! риптофан или АКТГ и могут метастазировать в кости. Рис. 1. Частота и локализация карциноидных опухолей среди всех опухолей органов пищеварения 4 Сучасна гастроентерологія, № 3 (23), 2005 р. ЗАХВОРЮВАННЯ ПІДШЛУНКОВОЇ ЗАЛОЗИ Клиническая картина карциноидной болезни мно! гообразна и зависит от локализации первичной опу! холи, наличия метастазов и продуцируемых опухо! лью биологически активных веществ. В связи с этим описано несколько вариантов карциноидного синд! рома: ! Cassidy—Sholte; ! Steiner—Voerner; ! Hedinger; ! Biork—Thorson; ! Jules Verne. Классическая триада карциноидного синдрома включает [3]: 1) приступы гиперемии и приливов кро! ви к лицу, туловищу, нередко сопровождающиеся бронхоспазмом и обусловленные периодическим выбросом больших количеств брадикинина, проста! гландинов, 5!гидрокситриптофана; 2) диарею, возни! кающую вследствие гипермоторики кишечника на фоне избыточной секреции серотонина (дефекация у таких больных может быть до 20—30 раз в сутки); 3) развитие эндокардиального фиброза с отложением карциноидных бляшек на створках трехстворчатого клапана, клапана легочной артерии, что приводит к формированию трикуспидальной недостаточности и стенозу легочной артерии (за счет прямого действия серотонина). К часто встречающимся признакам можно отнести стенокардию вследствие спазма ко! ронарных артерий, снижение артериального давле! ния, артропатию, пелагроподобное поражение кожи. В зависимости от клинических проявлений и осо! бенностей диагностики различают три клинических варианта карциноидной болезни: 1) асимптомный — когда опухоль обнаруживают случайно при эндоско! пическом исследовании желудка; 2) карциноид без проявлений карциноидного синдрома с симптомами объемного образования в органах пищевого канала; 3) карциноид с метастазами в печень и проявления! ми карциноидного синдрома с локализацией первич! ного очага опухоли в ПЖ или подвздошной кишке. Частота метастазирования карциноида ПЖ и прояв! лений классического карциноидного синдрома при этом заболевании не превышает по 20% для каждого [4]. То есть течение карциноида ПЖ в большинстве случаев без! или малосимптомное. Описаны клинические наблюдения карциноидов ПЖ, проявляющихся болью и механической желтухой [6], болью и дуоденальной язвой [5], хилезным асци! том и постоянной диареей [11, 13], болью в костях из!за метастазов [9]. Диагностика состоит в выявлении повышенного выделения метаболита серотонина — 5!оксииндол! уксусной кислоты — с мочой (более 150 мг/сут) и увеличенного содержания серотонина, хромограни! на А, 5!окситриптофана в крови. Проводят эхокардио! скопию для верификации трикуспидальной недоста! точности и стеноза легочной артерии. Для визуали! зации опухоли используют УЗИ (особенно эндоско! пическую сонографию), КТ, МРТ, ангиографию, сцин! тиграфию с октреосканом. Наиболее информативно гистологическое исследование, хотя биопсия ПЖ сложна в техническом отношении и небезопасна. Прогноз. Частота 5!летней выживаемости при кар! циноидах ПЖ составляет 20—25% (даже при мета! стазах в печень) [7]. Сучасна гастроентерологія, № 3 (23), 2005 р. Лечение хирургическое. После операции возмож! но развитие криза (сердечно!сосудистая недоста! точность, парез желудка и кишечника и т. д.), кото! рый купируется введением 0,1—0,5 мг сандостатина [1]. Кроме того, для предотвращения такого криза до и после операции необходимо провести инфузи! онную терапию, профилактически ввести сандоста! тин блокаторов Н1! и Н2!гистаминовых рецепторов, α! и β!адреноблокаторы, периферические серото! ниновые антагонисты [8]. Консервативное лечение предусматривает диету с ограничением богатых серотонином продуктов (грецкие орехи, бананы, киви и др.); назначение ан! тагонистов серотонина — ципрогептадина (12—16 мг/сут), метисергида (6—8 мг/сут), сандостатина, блокаторов гистаминовых рецепторов; химиотера! пию (комбинация стрептозоцина с 5!фторурацилом, α!интерферон) [1, 10, 12]. При метастазах в печень лигируют печеночную ар! терию или проводят полную деартериализацию пе! чени [10, 12]. Приводим описание нашего наблюдения за боль! ной с карциноидом ПЖ. Больная О., 55 лет, поступила в гастроэнтерологи! ческое отделение кафедры внутренних болезней До! нецкого мединститута 22.03.93 г. с жалобами на но! ющую боль в левом подреберье после еды, жажду, сухость во рту, похудание на 8 кг за последние 6 мес. Считает себя больной около 3 лет, когда возник приступ резкой боли в области левого подреберья, купированный спазмолитическими средствами. При УЗИ выявлен участок сниженной эхогенности разме! ром 7,6 × 4,4 см в области хвоста ПЖ, увеличение селезенки. При КТ (декабрь 1990 г.) отмечено, что тело и хвост ПЖ увеличены, бугристые, структура негомогенная; спленомегалия. Поставлен диагноз рака ПЖ, рекомендовано симптоматическое лече! ние. Однако больная чувствовала себя удовлетвори! тельно, продолжала работать. Лишь изредка беспо! коила ноющая боль в левом подреберье. Состояние ухудшилось в конце 1992 г., когда появилась жажда, начала худеть. Диагностирован сахарный диабет. В связи с длительностью заболевания диагноз рака ПЖ был отвергнут, и больную направили в клинику с предположительным диагнозом: «псевдотуморозный панкреатит». При поступлении состояние больной удовлетвори! тельное, достаточного питания. Кожа и видимые сли! зистые оболочки обычной окраски. Язык обложен у корня белым налетом. Периферические лимфатичес! кие узлы не увеличены. В легких дыхание везикуляр! ное. Тоны сердца ритмичны, приглушены на верхуш! ке. Пульс 78 в 1 мин, обычный. Живот при поверхнос! тной пальпации безболезненный, мягкий. При глубо! кой пальпации отрезки толстой кишки без особен! ностей. В левой половине надчревья пальпируется плотное бугристое безболезненное образование. Пе! чень на 3 см ниже края реберной дуги, плотная, край заострен, безболезненный, неровный. Селезенка на 2 см ниже края реберной дуги, безболезненная. Общий анализ крови: эр. — 4,8 × 1012 /л.; Hb — 154 г/л; ц. п. — 0,9; л. — 4,3 × 109 /л.; э. — 2%, п. — 4%, с. — 66%, лимф. — 22%, мон. — 6%; СОЭ — 10 мм/ч. Глюкоза — 12,4 ммоль/л. Амилаза крови (биохимичес! 5 ЗАХВОРЮВАННЯ ПІДШЛУНКОВОЇ ЗАЛОЗИ кий анализатор фирмы «KONE») — 18 U/l (при норме 0—96 U/l); амилаза мочи — 82 U/l (при норме 36—360 U/l). Иммунореактивный трипсин — 24 нг/мл (наборы фирмы «CIS»; норма 32—58 нг/мл). Липаза крови — 1 ед. по Титцу (норма 0,5—1,5 ед.). Инсулин сыворот! ки крови — 4 мкед/мл (норма 3—25 мкед/мл); С!пеп! тид — 0,4 пмоль/л (наборы фирмы «CIS», норма 0,6— 1,2 пмоль/л). СЕА — 5,5 нг/мл, СА 19!9 — 5,9 Е/мл. УЗИ: печень увеличена, контур неровный, структу! ра неоднородная, эхогенность повышена. Селезенка увеличена (16 × 8 см). Портальная вена не расшире! на. ПЖ увеличена: поражение тела и хвоста. Контуры неровные, структура неоднородная за счет образо! вания с неровными краями и наличием участков по! вышенной эхогенности. Образование (размером 9,8 × 7,8 см) выходит за контур железы (рис. 2). КТ: по сравнению с ранее проведенным исследо! ванием стала толще ПЖ, но парапанкреатические лимфатические узлы не увеличены (рис. 3). Фиброгастродуоденоскопия: хронический гастро! дуоденит. Рентгенологическое исследование желуд! ка: органических изменений нет. Сканирование пече! ни: диффузное поражение печени по типу цирроза с гиперплазией и активизацией ретикулоэндотелиаль! ной системы селезенки. Рис. 2. Сонограмма больной О. Объемное обра= зование тела и хвоста ПЖ Рис. 3. Компьютерная томограмма брюшной полости и забрюшинного пространства больной О. Объемное образование тела и хвоста ПЖ 6 В связи с неясностью диагноза произведена одно! моментная чрескожная биопсия образования ПЖ под контролем УЗИ. Гистологическое и цитологическое исследование биоптата: злокачественный серотонин! продуцирующий карциноид. После получения заклю! чения определены уровни серотонина и гистамина в крови — 622 нмоль/л (при норме 230—460 нмоль/л) и 986 нмоль/л (норма 180—900 нмоль/л). Эхокардиог! рафия — уплотнение створок аортального клапана. Больная переведена в хирургическое отделение. При лапаротомии выявлено больших размеров буг! ристое каменистой плотности опухолевидное обра! зование, занимающее тело и хвост ПЖ с распрост! ранением на ворота селезенки и брюшную аорту. Печень увеличена, бугристая. Видимых метастазов нет. После биопсии образования ПЖ и печени опу! холь определена как неоперабельная. Гистологическое заключение (рис. 4): в ПЖ лока! лизован доброкачественный карциноид с участками озлокачествления, в печени — перипортальный фиб! роз, жировая дистрофия, что характерно для пора! жения печени при карциноиде. Больная направлена в онкологический диспансер для проведения химио! и рентгенотерапии. Из данного клинического наблюдения, на наш взгляд, следует извлечь следующие уроки: ! отсутствие классических клинических проявлений карциноидного синдрома не исключает возможности карциноида ПЖ; ! важное значение гистологического исследования ПЖ (чрескожного или интраоперационного) при псевдотуморозном панкреатите, образованиях ПЖ неясного происхождения; ! необходимость постоянного контроля за состоя! нием пациентов с опухолями ПЖ, даже если на пер! вый взгляд они неоперабельны; ! определение уровней серотонина в крови и 5!ок! сииндолуксусной кислоты в моче, проведение эхо! кардиоскопии у больных с медленно растущими опу! холями ПЖ; ! при гепатолиенальном синдроме гепатомегалия и спленомегалия могут развиваться вследствие принципиально различных механизмов. Рис. 4. Доброкачественный карциноид (вероятно, серотонинпродуцирующий) с участками озлокачествления; построен из трабекулярных, местами железистоподобных структур с небольшим количеством стромы. Окраска гематоксилином и эозином. Ув. 200 Сучасна гастроентерологія, № 3 (23), 2005 р. ЗАХВОРЮВАННЯ ПІДШЛУНКОВОЇ ЗАЛОЗИ СПИСОК ЛИТЕРАТУРЫ 1. Калинин А.В. Клиническая картина, диагностика и ле! чение опухолей АПУД!системы // Росс. журн. гастроэнте! рол., гепатол., колопроктол.— 1997.— № 3.— С. 36—41. 2. Кузин Н.М., Егоров А.В. Нейроэндокринные опухоли поджелудочной железы.— М.: Медицина, 2001.— 208 с. 3. Симоненко В.Б., Маканин М.А., Дулин П.А. Карцино! идные опухоли желудочно!кишечного тракта // Росc. журн. гастроэнтерол., гепатол., колопроктол.— 1998.— №5.— С. 93—98. 4. Burgos A., Noack M.M., Jaffe B.M. Carcinoid Tumors of the Pancreas and Biliary Tract / In: The Pancreas / Ed. H.G. Be! ger et al.— Oxford et al.: Blackwell Science Ltd., 1998.— Vol. 2.— P. 1220—1227. 5. Carcinoid tumor of the pancreas: ultrastructure observati! ons of a lymph node metastasis and comparison with bronchial carcinoid / A.S. Patchefsky, G. Gordon, W.V. Harrer, W.S. Hoch // Cancer.— 1974.— Vol. 33.— P. 1349—1353. 6. Characterization of a human pancreatic carcinoid in vitro: morphology, amine and peptide storage, and secretion / D. Pare! parech, J. Ishizuka, C.M. Townsend et al. // Pancreas.— 1994.— Vol. 9.— P. 83—90. 7. Clinical features, diagnosis, and location of carcinoid tu! mors, and there management / A.L. Vinik, M.K. McLeod, L.M. Fig et al. // Gastroenterol. Clin. North Am.— 1989.— Vol. 18.— P. 865—896. 8. Debas H.T., Mulvihill S.J. Neuroendocrine gut neoplasms: important lessons from uncommon tumors // Arch. Surg.— 1994.— Vol. 129.— P. 965—972. 9. Lands R.H., Karnad A. Pancreatic carcinoid with extensive osteolytic bone disease // J. Tenn. Med. Assoc.— 1991.— Vol. 84.— P. 176—177. 10. Moertel C.G. Treatment of the carcinoid tumor and the malignant carcinoid syndrome // J. Clin. Oncol.— 1983.— Vol. 1.— P. 727—740. 11. Mortensen R.M., Medoff J., Feldman J.M. Case report: chylous ascites and carcinoid tumors: possible association of two rare disorders // Am. J. Med. Sci.— 1988.— Vol. 296.— P. 272— 274. 12. A phase II trial of alfa!interferon and 5!fluorouracil in pati! ents with advanced carcinoid and islet cell tumors / L. Saltz, N. Kemeny, G. Schwartz, D. Kelsen // Cancer.— 1994.— Vol. 74.— P. 958—961. 13. Varma J.S. Acute chylous ascites with carcinoid of pancre! as // Scot. Med. J.— 1985.— Vol. 30.— P. 111. КАРЦИНОЇДНА ПУХЛИНА ПІДШЛУНКОВОЇ ЗАЛОЗИ Н.Б. Губергріц, І.В. Василенко, О.Д. Зубов, Н.В. Момот, Е.М. Станіславська У статті описано сучасні уявлення про частоту, клінічні вияви, діагностику і лікування карциноїдних пухлин під! шлункової залози. Крім того, наводиться клінічне спостереження за хворою з карциноїдною пухлиною під! шлункової залози, виділено особливості її перебігу й визначено уроки, які варто винести з нього. PANCREAS CARCINOID TUMOR N.B. Gubergrits, I.V. Vasilenko, A.D. Zubov, N.V. Momot, E.N. Stanislavskaya The article presents modern conceptions on frequency, clinical manifestations, diagnosis and treatment of pancreas carcinoid tumors. Moreover clinical observations of a patient with pancreas carcinoid tumor have been presented, peculiarities of its course have been described and lessons that should be concluded from this case have been indi! cated. Сучасна гастроентерологія, № 3 (23), 2005 р. 7


