ссылка на учебник
реклама
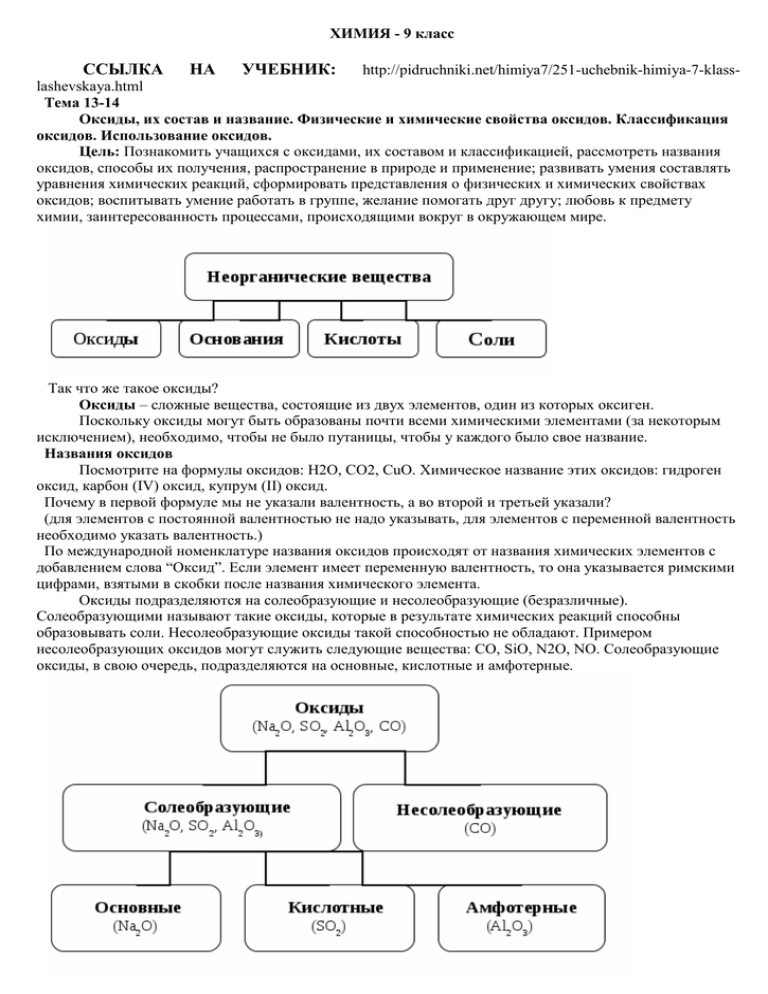
ХИМИЯ - 9 класс ССЫЛКА НА УЧЕБНИК: http://pidruchniki.net/himiya7/251-uchebnik-himiya-7-klass- lashevskaya.html Тема 13-14 Оксиды, их состав и название. Физические и химические свойства оксидов. Классификация оксидов. Использование оксидов. Цель: Познакомить учащихся с оксидами, их составом и классификацией, рассмотреть названия оксидов, способы их получения, распространение в природе и применение; развивать умения составлять уравнения химических реакций, сформировать представления о физических и химических свойствах оксидов; воспитывать умение работать в группе, желание помогать друг другу; любовь к предмету химии, заинтересованность процессами, происходящими вокруг в окружающем мире. Так что же такое оксиды? Оксиды – сложные вещества, состоящие из двух элементов, один из которых оксиген. Поскольку оксиды могут быть образованы почти всеми химическими элементами (за некоторым исключением), необходимо, чтобы не было путаницы, чтобы у каждого было свое название. Названия оксидов Посмотрите на формулы оксидов: H2O, CO2, CuO. Химическое название этих оксидов: гидроген оксид, карбон (IV) оксид, купрум (II) оксид. Почему в первой формуле мы не указали валентность, а во второй и третьей указали? (для элементов с постоянной валентностью не надо указывать, для элементов с переменной валентность необходимо указать валентность.) По международной номенклатуре названия оксидов происходят от названия химических элементов с добавлением слова “Оксид”. Если элемент имеет переменную валентность, то она указывается римскими цифрами, взятыми в скобки после названия химического элемента. Оксиды подразделяются на солеобразующие и несолеобразующие (безразличные). Солеобразующими называют такие оксиды, которые в результате химических реакций способны образовывать соли. Несолеобразующие оксиды такой способностью не обладают. Примером несолеобразующих оксидов могут служить следующие вещества: СО, SiO, N2O, NO. Солеобразующие оксиды, в свою очередь, подразделяются на основные, кислотные и амфотерные. Даем определение кислотным оксидам: Оксиды неметаллов называют кислотными оксидами. ? Почему эти оксиды названы кислотными? Т.к. при взаимодействии с водой они образуют кислоты, например: CO2 + H2O = H2CO3 карбоновая кислота SO3 + H2O = H2SO4 серная кислота Оксиды, которым соответствуют кислоты (независимо от того, реагируют они с водой или не реагируют) называют кислотными. Оксиды металлов ( например СаО, MgO, K2O и т.д.) называют основными оксидами. Что означает слово основные пока не понятно. Если кальций оксид (негашеная известь) соединить с водой, то получиться новое вещество состава Са(ОН)2 – основание. Его используют весной в садах, парках, скверах для побелки деревьев. CaO+H2O= Са(ОН)2 это основание, т.е. соединение в состав которого входит гидроксильная группа (ОН) Теперь, когда мы познакомились с основаниями, становится понятным название – основной оксид. Оксиды, которым соответствуют основания (независимо от того, реагируют они с водой или не реагируют) называют основными. Существуют амфотерные элементы. Амфотерность – способность элементов и веществ проявлять двойственные свойства. Амфотерными являются Be, Zn, Al и некоторые другие элементы. Их оксиды и гидроксиды реагируют как с кислотами, так и со щелочами, образуя соли. Информация о распространении оксидов в природе и их значении. А знаете ли вы, друзья, что территория Днепропетровской области и большая часть Украины, в период так называемого миоцена (около 23,5 – 25 млрд. лет назад) находилась глубоко под водой. Когда дно поднималось, вода спадала, а от останков разных морских животных оставалась масса костей и ракушек. Все эти вещества имеют химическую формулу СаСО3 и образуются при соединении двух оксидов: кальций оксида СаО, содержащийся в костях и карбон (IV) оксида CO2 , входящего в состав воздуха, где его объем составляет 0,03%. Богата Украина кварцевыми песками и глиной, в состав которых входят такие оксиды как силиций (IV) оксид SiO2 и алюминий оксид. Плиний считал, что горный хрусталь “рождается из небесной влаги и чистейшего снега”. Однако состав его иной: оксид кремния (IV) SiO2. Кварц, кремень, горный хрусталь, аметист, яшма, опал — все это оксид кремния (IV). Один из распространенных оксидов – диоксид углерода CO2. Он содержится в составе вулканических газов. Сухой лед – тоже CO2. В отличие от водяного льда плотный. Он тонет в воде, резко охлаждая ее. Горящий бензин можно быстро потушить, бросив в пламя несколько кусочков сухого льда. Главное применение сухого льда — хранение и перевозка продуктов: рыбы, мяса, мороженого. Ценность сухого льда заключается не только в его охлаждающем действии, но и в том, что продукты в углекислом газе не плесневеют, не гниют. Оксид хрома(III) – Cr2O3 –кристаллы зеленого цвета, нерастворимые в воде. Cr2O3 используют как пигмент при изготовлении декоративного зеленого стекла и керамики. Оксид цинка – используется для приготовления белой масляной краски (цинковые белила) Физические свойства оксидов. Физические и химические свойства оксидов очень отличаются. При комнатной температуре большинство оксидов являются твердыми веществами, например, меди (II) оксид CuO черного цвета, кальций оксид CaO белого цвета, хром (III) оксид Cr2O3 темно-зеленого цвета. Некоторые оксиды являются жидкостями, например, водород оксид (вода) H2O и Cl2O7 являются бесцветными жидкостями, а некоторые - газообразными веществами, например карбон (IV) оксид CO2 является газом без цвета, а азот (IV) оксид NO2 являются бурым газом. Некоторые оксиды являются веществами с молекулярным строением, другие имеют ионную строение. Получение оксидов: Мы уже встречались с оксидами, при изучении темы “Кислород”. При взаимодействии разных веществ с кислородом получают оксиды. Вспомните, из каких веществ можно получить оксиды. (оксиды получают при взаимодействии кислорода с простыми веществами. ) 1. Взаимодействие простых веществ с кислородом. ? Дайте определение простым веществам. На какие группы можно разделить простые вещества? (на металлы и неметаллы) Самостоятельная работа учащихся (записать в свою тетрадь) Записать уравнения реакций взаимодействия металлов с кислородом и неметаллов с кислородом, назвать продукты ? Какие еще вещества, кроме простых веществ вам известны? ? Дайте определения сложным веществам ? Как горят сложные вещества? 2. Взаимодействие сложных веществ с кислородом Самостоятельная работа учащихся (записать в свою тетрадь) Записать уравнение реакции взаимодействия метана с кислородом, назвать продукты CH4+O2→.....+...... Получения оксидов. 1. Разложение оснований Mg(OH)2 = MgO + H2O 2. Разложение кислот H2CO3 = H2O + CO2 Самостоятельная работа учащихся (записать в свою тетрадь) Проверим свои знания - тест 1. При нормальных условиях оксиды - это вещества: а) только газообразные б) только жидкие в) газообразные, жидкие и твердые г) только твердые 2. Оксиды – это: а) вещества, в состав которых входит гидроген б) вещества, в состав которых входит оксиген в) вещества, в состав которых входят металлы 3. Как называется оксид SO2? а) сульфур оксид б) сульфур (II) оксид в) сульфур (IV) оксид г) сульфур (VI) оксид 4. Какие вещества получим при разложении CaCO3? а) СаО и СО2 б) Са и О2 в) Са и СО2 г) С и СаО Ссылка на видео урок: http://interneturok.ru/ru/school/chemistry/8-klass/undefined/klassifikatsiya-ihimicheskie-svoystva-oksidov Домашнее задание: выучить §7, 12-14, читать (пока как общее ознакомление) §8-11 Схемы на стр. 64 и 65 (две) выписать в свою тетрадь и выучить наизусть! Ответы присылайте по адресу: dosh5858@mail.ru Для Халанской Г.Н. Консультации в школе с 8.00 до 12.00 по вторникам и четвергам